
【题目】下列说法正确的是
A. 化学反应的反应热与反应过程有密切的关系
B. 化学反应的反应热取决于反应体系的始态和终态
C. 盖斯定律只是一条简单的自然规律,其实际作用不大
D. 有的化学反应过程没有能量变化
 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源: 题型:
【题目】下列有关物质分离说法正确的是
A. 乙酸乙酯与乙醇的分离可用分液操作
B. 滴定管、容量瓶、分液漏斗等仪器,在使用前均须冼净并检查是否漏水
C. 碘洒中加CCl4振荡睁置后,上层几乎为无色,下层为紫色
D. 蒸馏、分馏和干馏都是利用物质沸点不同而将物质分离的方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胶体区别于其他分散系的本质特征是 ( )
A.光束穿过胶体时形成一条光亮的“通路”
B.胶体粒子大小在l nm—l00 nm 之间
C.胶体粒子可以透过滤纸
D.胶体粒子不能透过半透膜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示。下列说法正确的是( )
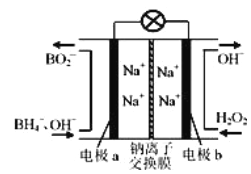
A. 电池放电时Na+从b极区移向a极区
B. 每消耗3molH2O2,转移的电子为3mol
C. 电极a采用MnO2,MnO2既作电极材料又有催化作用
D. 该电池的负极反应为:BH4-+8OH--8e-═BO2-+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列反应均为放热反应,其中反应热最小的是
A. 2A(l) + B(l) = 2C (g) △H1
B. 2A(g) + B(g) = 2C(g) △H2
C. 2A (g) + B ( g ) = 2C(l) △H3
D. 2A (l) + B(l)= 2C(l) △H4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6)。[来
(1)丙烷脱氢可得丙烯。
已知:C3H8(g)→CH4(g)+HC≡CH(g)+H2(g)ΔH1=+156.6 kJ·mol-1
CH3CH=CH2(g)→CH4(g)+HC≡CH(g)ΔH2=+32.4 kJ·mol-1
则相同条件下,反应C3H8(g)→CH3CH==CH2(g)+H2(g)的ΔH_______kJ·mol-1。
(2)以丙烷为燃料制作新型燃料电池,电池的正极通入O2和CO2,负极通入丙烷,电解质是熔融碳酸盐。电池反应方程式为________________;放电时,CO32—移向电池的________(填“正”或“负”)极。
(3)碳氢化合物完全燃烧生成CO2和H2O。常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.60,c(H2CO3)=1.5×10-5 mol·L-1。若忽略水的电离及H2CO3的二级电离,则H2CO3![]() HCO3—+H+的平衡常数K1=__________。(已知:10-5.60=2.5×10-6)
HCO3—+H+的平衡常数K1=__________。(已知:10-5.60=2.5×10-6)
(4)常温下,0.1 mol·L-1 NaHCO3溶液的pH大于8,则溶液中c(H2CO3)_____________c(CO32—)(填“>”、“=”或“<”),原因是___________________(用离子方程式和必要的文字说明)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值,下列有关说法正确的是( )
A. 常温下,7.8g固体Na2O2中,含有的阴阳离子总数为0.4NA
B. 标准状况下,22.4 L的CCl4中C—Cl键数为4NA
C. 1mol N5+ 含有的电子数为34NA
D. 4℃时,18g2H216O中含有共用电子对数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,向密闭恒容容器中加入1.0 mol·L-1X,发生反应:2X(g) ![]() Y(g)+Z(g) △H<0,反应到8min时达到平衡;在14min时改变体系的温度, 16min时建立新平衡。X的物质的量浓度变化如图所示。下列有关说法正确的是
Y(g)+Z(g) △H<0,反应到8min时达到平衡;在14min时改变体系的温度, 16min时建立新平衡。X的物质的量浓度变化如图所示。下列有关说法正确的是
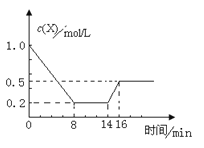
A.0~8min用Y表示该反应速率为0.1mol·L-1·min-1
B.8min时达到平衡,该反应的平衡常数为K= 0.5
C.14min时,改变的反应条是降低了温度
D.16min时的正反应速率比8min时的正反应速率大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com