
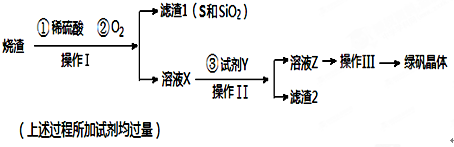
���� ���᳧���������ᡢ������Ӧ�����˷���õ���ҺX�Ͳ�����I��S����������ȣ�����ҺX��ҪΪFe2��SO4��3��H2SO4�ȣ�����������������������Һ�����ɳ�ȥδ��Ӧ�����ᣬ���˳�ȥδ��Ӧ��Fe����ҺΪ����������Һ����ͨ��Ũ����������ȴ�ᾧ�õ��̷���
��1�����ղ�����ǰ������ʱ仯����֪�������ǹ��ˣ�
��2������Fe��Fe3+��ԭΪFe2+�����ɳ�ȥδ��Ӧ�����
��3���������Ǵ���Һ�л�þ��壻
��4����������Һ����ȻҪ�õ�����ƿ��Ӧ��ע������ƿ�Ĺ��
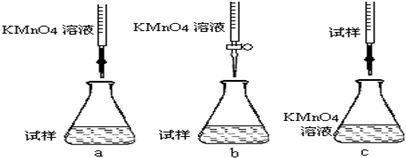
�ڸ��������Һ����ǿ�����ԣ��������ܣ�Ӧ������ʽ�ζ��ܣ�ע�����������������
�۸��������Һ�������Ϻ�ɫ����������ָʾ����������Һ��ɫ�ж��յ㣻�ζ��յ��ȡ�ζ��̶ܿ�ʱ������KMnO4��ҺҺ�棬Һ���ڿ̶����·����������������Һ�����ƫС��
�ܸ������ĸ�����ؼ���n��Fe2+������n��FeSO4•7H2O��=n��Fe2+��������������Ʒ��FeSO4•7H2O������������
��� �⣺���᳧���������ᡢ������Ӧ�����˷���õ���ҺX�Ͳ�����I��S����������ȣ�����ҺX��ҪΪFe2��SO4��3��H2SO4�ȣ�����������������������Һ�����ɳ�ȥδ��Ӧ�����ᣬ���˳�ȥδ��Ӧ��Fe����ҺΪ����������Һ����ͨ��Ũ����������ȴ�ᾧ�õ��̷���
��1���������ǽ��������ܵĹ�����Һ����룬��֪�������ǹ��ˣ�
�ʴ�Ϊ�����ˣ�
��2������Fe��Fe3+��ԭΪFe2+�����ɳ�ȥδ��Ӧ�����ᣬ��Ӧ���ӷ���ʽΪ��Fe+2Fe3+�T3Fe2+��Fe+2H+�TFe2++H2����
�ʴ�Ϊ��Fe+2Fe3+�T3Fe2+��Fe+2H+�TFe2++H2����
��3���������Ǵ���Һ�л�þ��壬��������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ�����õ����壬
�ʴ�Ϊ������Ũ����
��4����������Һ����ȻҪ�õ�����ƿ����Ҫ1000mL����ƿ��
�ʴ�Ϊ��1000mL����ƿ��
�ڸ��������Һ����ǿ�����ԣ��������ܣ�Ӧ������ʽ�ζ��ܣ�cװ��������Ӵ��Ƚϴ��ױ�������������ѡ��b��
�۸��������Һ�������Ϻ�ɫ����������ָʾ�����μ����һ��KMnO4��Һʱ����Һ�����ɫ�Ұ���Ӳ�����ɫ��˵����Ӧ�����յ㣬
�ζ��յ��ȡ�ζ��̶ܿ�ʱ������KMnO4��ҺҺ�棬Һ���ڿ̶����·����������������Һ�����ƫС���ⶨ���ƫ�ͣ�
�ʴ�Ϊ���μ����һ��KMnO4��Һʱ����Һ�����ɫ�Ұ���Ӳ�����ɫ��ƫ�ͣ�
��25mL��Һ���ĸ������Ϊ0.02L��0.01mol/L=0.0002mol����5Fe2++MnO4-+8H+�T5Fe3++Mn2++4H2O����֪11.5g�̷���Ʒ��n��Fe2+��=5��0.0002mol��$\frac{1000mL}{25mL}$=0.04mol����n��FeSO4•7H2O��=n��Fe2+��=0.004mol����Ʒ��FeSO4•7H2O����������Ϊ$\frac{0.04mol��278g/mol}{11.5g}$��100%=96.7%��
�ʴ�Ϊ��96.7%��
���� ���⿼�����ʵ��Ʊ���Ϊ�߿��������ͣ��漰���ʵķ����ᴿ����Һ���ơ�������ԭ��Ӧ�ζ������ʺ����ⶨ�ȣ���Ŀ�Ѷ��еȣ��ؼ�����ȷ�Ʊ�ԭ������ѧʵ�����������


 ��ʦ����ָ���ο�ʱϵ�д�
��ʦ����ָ���ο�ʱϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| ����ǰ������ | ���Ⱥ������ | ||
| W1�������� | W2������+���壩 | W3������+��ˮ����ͭ�� | |
| ��һ�� | 15.688g | 17.668g | 16.962g |
| �ڶ��� | 15.688g | 17.744g | 17.033g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢܢ� | B�� | �ڢۢޢ� | C�� | �ڢݢޢ� | D�� | �٢ۢޢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ݢܢ٢ۢ� | B�� | �ܢ٢ڢݢ� | C�� | �ڢݢܢ٢� | D�� | �٢ܢڢݢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Cl | B�� | O | C�� | KMnO4 | D�� | HCl |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com