
【题目】芳香族化合物A(C9H11Br)常用于药物及香料的合成,A有如图转化关系(部分反应条件略去):

已知:①A是芳香族化合物且分子侧链上的氢原子只有1种化学环境;
② +CO2
+CO2
(1)I中含氧官能团的名称为___和___。
(2)由A生成B的化学方程式为___。
(3)C→I的反应类型为___。
(4)根据已知信息分析,![]() 在酸性KMnO4溶液作用下所得有机产物的结构简式是___。
在酸性KMnO4溶液作用下所得有机产物的结构简式是___。
(5)写出符合下列条件的G的一种同分异构体的结构简式:___。
①属于芳香族化合物,且核磁共振氢谱有4个峰;
②能发生水解反应和银镜反应,且能与FeCl3溶液发生显色反应
(6)康叉丙酮(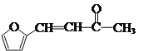 )是一种重要的医药中间体,写出以
)是一种重要的医药中间体,写出以![]() 和
和![]() 为原料制备康叉丙酮的合成路线图___(无机试剂及有机溶剂任用,合成路线图示例见本题题干)。
为原料制备康叉丙酮的合成路线图___(无机试剂及有机溶剂任用,合成路线图示例见本题题干)。
【答案】羟基 羰基 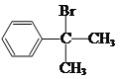 +NaOH
+NaOH![]()
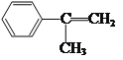 +NaBr+H2O 加成反应 CH3COCH3
+NaBr+H2O 加成反应 CH3COCH3 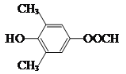 或
或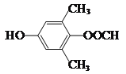
![]()
【解析】
由B的结构简式![]() 结合A的分子式及信息(A是芳香族化合物且分子侧链上的氢原子只有1种化学环境),可逆推出A的结构简式为
结合A的分子式及信息(A是芳香族化合物且分子侧链上的氢原子只有1种化学环境),可逆推出A的结构简式为 ;B 与Br2发生加成反应生成D的结构简式为
;B 与Br2发生加成反应生成D的结构简式为![]() ,水解生成E的结构简式为
,水解生成E的结构简式为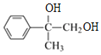 ,氧化生成F的结构简式为
,氧化生成F的结构简式为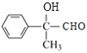 ,再氧化生成G的结构简式为
,再氧化生成G的结构简式为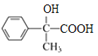 ,发生缩聚反应生成H的结构简式为
,发生缩聚反应生成H的结构简式为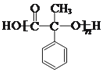 。依此分析进行解题。
。依此分析进行解题。
(1)I的结构简式为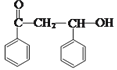 ,分子中含氧官能团的名称为羟基和羰基。答案为:羟基;羰基;
,分子中含氧官能团的名称为羟基和羰基。答案为:羟基;羰基;
(2)由 生成
生成![]() ,则在NaOH的醇溶液中加热,发生卤代烃的消去反应,化学方程式为
,则在NaOH的醇溶液中加热,发生卤代烃的消去反应,化学方程式为 +NaOH
+NaOH![]()
![]() +NaBr+H2O。答案为:
+NaBr+H2O。答案为: +NaOH
+NaOH![]()
![]() +NaBr+H2O;
+NaBr+H2O;
(3)![]() +
+ ![]() →
→ ,反应类型为加成反应。答案为:加成反应;
,反应类型为加成反应。答案为:加成反应;
(4)根据已知信息分析,![]() 在酸性KMnO4溶液作用下,将碳碳双键断开,双键碳原子被氧化为羰基和H2CO3,H2CO3为无机物,所得有机产物的结构简式是
在酸性KMnO4溶液作用下,将碳碳双键断开,双键碳原子被氧化为羰基和H2CO3,H2CO3为无机物,所得有机产物的结构简式是![]() 。答案为:
。答案为:![]() ;
;
(5)符合下列条件:“①属于芳香族化合物,且核磁共振氢谱有4个峰;②能发生水解反应和银镜反应,且能与FeCl3溶液发生显色反应”的有机物,分子内应含有酚羟基、-OOCH、2个连在苯环上且位置对称的-CH3,结构简式为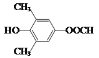 或
或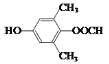 。答案为:
。答案为: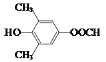 或
或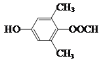 ;
;
(6)由流程图中C→I→J可得出,要合成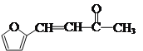 ,需将
,需将![]() 转化为
转化为![]() ,再与
,再与![]() 发生加成反应,产物再发生消去反应。从而得出制备康叉丙酮的合成路线图为
发生加成反应,产物再发生消去反应。从而得出制备康叉丙酮的合成路线图为![]() 。答案为:
。答案为:![]() 。
。


科目:高中化学 来源: 题型:
【题目】向100 mL NaOH溶液中通入一定量的CO2气体,充分反应后,再向所得溶液中逐滴加入0.2 mol/L的盐酸,产生CO2的体积与所加盐酸体积之间关系如下图所示。下列判断正确的是( )

A. 原NaOH溶液的浓度为0.1 mol·L-1
B. 通入CO2的体积为448 mL
C. 所得溶液的溶质成分的物质的量之比为n(NaOH)∶n(Na2CO3)=1∶3
D. 所得溶液的溶质成分的物质的量之比为n(NaHCO3)∶n(Na2CO3) = 2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验装置及原理正确的是( )
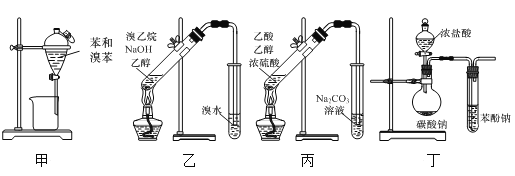
A.用图甲装置分离苯和溴苯的混合物
B.用图乙装置检验溴乙烷的消去产物
C.用图丙装置制取并收集乙酸乙酯
D.用图丁装置验证酸性:碳酸>苯酚
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲胺铅碘(CH3NH3PbI3)可用作全固态钙钛矿敏化太阳能电池的敏化剂,由CH3NH2、PbI2及HI为原料合成,回答下列问题:
(1)制取甲胺的反应为CH3OH(g)+NH3(g)![]() CH3NH2(g)+H2O(g) ΔH。已知该反应中相关化学键的键能数据如下:
CH3NH2(g)+H2O(g) ΔH。已知该反应中相关化学键的键能数据如下:
共价键 | C—O | H—O | N—H | C—N |
键能/(kJ/mol) | 351.5 | 463 | 393 | 293 |
则该反应的ΔH=________kJ/mol。
(2)上述反应中所需的甲醇工业上利用水煤气合成,反应为CO(g)+2H2(g) ![]() CH3OH(g) ΔH<0。在一定条件下,将1 mol CO和2 mol H2通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,CH3OH的体积分数φ(CH3OH)变化趋势如图所示:
CH3OH(g) ΔH<0。在一定条件下,将1 mol CO和2 mol H2通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,CH3OH的体积分数φ(CH3OH)变化趋势如图所示:

①下列说法不能判断该反应达到化学平衡状态的是________。
A.体系中气体的密度保持不变
B.CO的消耗速率与CH3OH的消耗速率相等
C.体系中CO的转化率和H2的转化率相等
D.体系中CH3OH的体积分数保持不变
②平衡时,M点CH3OH的体积分数为10%,则CO的转化率为________。
③某同学认为上图中Y轴表示温度,你认为他判断的理由是______________________。
(3)实验室可由四氧化三铅和氢碘酸反应制备难溶的PbI2,同时生成I2,写出发生的化学反应方程式__________________。
(4)HI的制备:将0.8molI2(g)和1.2molH2(g)置于某1L密闭容器中,在一定温度下发生反应:I2(g)+H2(g)![]() 2HI(g)并达到平衡。HI的体积分数随时间的变化如表格所示:
2HI(g)并达到平衡。HI的体积分数随时间的变化如表格所示:
时间(min) | 1 | 2 | 3 | 4 | 5 | 6 | 7/span> |
HI体积分数 | 26% | 42% | 52% | 57% | 60% | 60% | 60% |
①该反应的平衡常数K=_____________。
②反应达到平衡后,在7min时将容器体积压缩为原来的一半,请在图中画出c(HI)随时间变化的曲线_______________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.![]() Cl表示中子数为18的氯元素的一种核素
Cl表示中子数为18的氯元素的一种核素
B.乙酸乙酯(CH3COOCH2CH3)和硬脂酸甘油酯(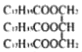 )互为同系物
)互为同系物
C.![]() 的名称为2﹣乙基丁烷
的名称为2﹣乙基丁烷
D.CH3(CH2)2CH3和CH(CH3)3互为同素异形体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】250C时,有c(CH3COOH)+c(CH3COO-)=0.1mol·L-1的一组醋酸、醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO-)与pH 的关系如图7 所示。下列有关溶液中离子浓度关系的叙述正确的是

A. pH="5." 5 的溶液中: c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-)
B. W 点所表示的溶液中: c(Na+)+c(H+)= c(CH3COOH)+c(OH-)
C. pH =" 3." 5 的溶液中: c(Na+) +c(H+) -c(OH-) +c(CH3COOH)=0.1mol·L-1
D. 向W 点所表示的1.0L 溶液中通入0.05mol HCl 气体(溶液体积变化可忽略): c(H+)= c(CH3COOH)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.利用石灰乳和硝酸工业的尾气(含NO、NO2)反应,既能净化尾气,又能获得应用广泛的Ca(NO2)2,其部分工艺流程如下:

(1)一定条件下,NO与NO2存在下列反应:NO(g) + NO2(g) ![]() N2O3(g),其平衡常数表达式为K = ____。
N2O3(g),其平衡常数表达式为K = ____。
(2)吸收时,尾气从吸收塔底进入,石灰乳从吸收塔顶喷淋,好处是____。
(3)为提高Ca(NO2)2的产率及纯度,则n(NO)∶n(NO2)应控制为____。
(4)生产中溶液需保持弱碱性,在酸性溶液中Ca(NO2)2会发生分解,产物之一是NO,其反应的离子方程式为___。
II.铝是地壳中含量最高的金属元素,其单质及合金在生产生活中的应用日趋广泛。
(1)真空碳热还原—氯化法可实现由铝土矿制备金属铝,相关的热化学方程式如下:
Al2O3(s) + AlCl3(g) + 3C(s) =3AlCl(g) + 3CO(g) △H = a kJ·mol—1
3AlCl (g)=2Al(l) + AlCl3(g) △H = bkJ·mol—1
则Al2O3(s) + 3C(s) =2Al(l) + 3CO(g) △H = __kJ·mol—1(用含a、b的代数式表示)。
(2)铝电池性能优越,Al—AgO电池可用作水下动力电源,其原理如图所示。该电池反应的化学方程式为____。
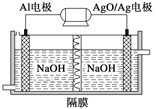
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KMnO4是中学常见的强氧化剂,用固体碱熔氧化法制备KMnO4的流程和反应原理如图:

反应原理:
反应I:3MnO2+KClO3+6KOH![]() 3K2MnO4+KCl+3H2O
3K2MnO4+KCl+3H2O
反应Ⅱ:3K2MnO4+2CO2═2KMnO4+MnO2↓+2K2CO3
(墨绿色) (紫红色)
已知25℃物质的溶解度g/100g水
K2CO3 | KHCO3 | KMnO4 |
111 | 33.7 | 6.34 |
请回答:
(1)下列操作或描述正确的是___
A.反应Ⅰ在瓷坩埚中进行,并用玻璃棒搅拌
B.步骤⑥中可用HCl气体代替CO2气体
C.可用玻璃棒沾取溶液于滤纸上,若滤纸上只有紫红色而无绿色痕迹,则反应Ⅱ完全
D.步骤⑦中蒸发浓缩至溶液表面有晶膜出现再冷却结晶:烘干时温度不能过高
(2)___(填“能”或“不能”)通入过量CO2气体,理由是___(用化学方程式和简要文字说明)。
(3)步骤⑦中应用玻璃纤维代替滤纸进行抽滤操作,理由是___。
草酸钠滴定法分析高锰酸钾纯度步骤如下:
Ⅰ.称取1.6000g高锰酸钾产品,配成100mL溶液
Ⅱ.准确称取三份0.5025g已烘干的Na2C2O4,置于锥形瓶中,加入少量蒸馏水使其溶解,再加入少量硫酸酸化;
Ⅲ.锥形瓶中溶液加热到75~80℃,趁热用I中配制的高锰酸钾溶液滴定至终点。
记录实验数据如表
实验次数 | 滴定前读数/mL | 滴定后读数/mL |
1 | 2.65 | 22.67 |
2 | 2.60 | 23.00 |
3 | 2.58 | 22.56 |
已知:MnO4﹣+C2O42﹣+H+→Mn2++CO2↑+H2O(未配平)
则KMnO4的纯度为___(保留四位有效数字);若滴定后俯视读数,结果将___(填“偏高”或“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常用铁碳混合物处理含Cu2+废水获得金属铜。当保持铁屑和活性炭总质量不变时,测得废水中Cu2+浓度在不同铁碳质量比(x)条件下随时间变化的曲线如下图所示。
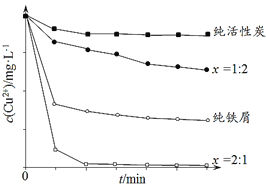
下列推论不合理的是
A. 活性炭对Cu2+具有一定的吸附作用
B. 铁屑和活性炭会在溶液中形成微电池,铁为负极
C. 增大铁碳混合物中铁碳比(x),一定会提高废水中Cu2+的去除速率
D. 利用铁碳混合物回收含Cu2+废水中铜的反应原理:Fe+Cu2+=Fe2++Cu
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com