
【题目】工业上常用铁碳混合物处理含Cu2+废水获得金属铜。当保持铁屑和活性炭总质量不变时,测得废水中Cu2+浓度在不同铁碳质量比(x)条件下随时间变化的曲线如下图所示。
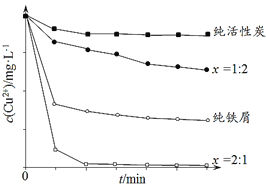
下列推论不合理的是
A. 活性炭对Cu2+具有一定的吸附作用
B. 铁屑和活性炭会在溶液中形成微电池,铁为负极
C. 增大铁碳混合物中铁碳比(x),一定会提高废水中Cu2+的去除速率
D. 利用铁碳混合物回收含Cu2+废水中铜的反应原理:Fe+Cu2+=Fe2++Cu
【答案】C
【解析】
A、由图可知纯的活性炭铜离子的浓度减小;
B、铁与活性炭形成原电池,铁比炭活泼;
C、由图可知纯铁时去除铜离子的速率,没铁碳比为2:1时的速率快;
D、利用铁碳混合物回收含Cu2+废水中铜的反应原理是铁与铜离子发生自发的氧化还原反应。
A项,活性炭具有许多细小微孔,且表面积巨大,具有很强的吸附能力,由图像可知,Cu2+在纯活性炭中浓度减小,表明活性炭对Cu2+具有一定的吸附作用,故不选A项;
B项,铁屑和活性炭在溶液中形成微电池,其中铁具有较强的还原性,易失去电子形成Fe2+,发生氧化反应,因此铁作负极,故不选B项;
C项,由图像可知,随着铁碳混合物中铁含量的增加至x=2:1,Cu2+的去除速率逐渐增加;但当铁碳混合物变为纯铁屑时,Cu2+的去除速率降低。当铁碳混合物中铁的含量过大时,正极材料比例降低,铁碳在废液中形成的微电池数量减少,Cu2+的去除速率会降低,因此增大铁碳混合物中铁碳比(x),不一定会提高废水中Cu2+的去除速率,故选C项;
D项,在铁碳微电池中,碳所在电极发生还原反应,Cu2+得到电子生成铜单质;因此该微电池的总反应方程式为Fe+Cu2+=Fe2++Cu,故不选D项。
综上所述,本题正确答案为C。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】芳香族化合物A(C9H11Br)常用于药物及香料的合成,A有如图转化关系(部分反应条件略去):

已知:①A是芳香族化合物且分子侧链上的氢原子只有1种化学环境;
② +CO2
+CO2
(1)I中含氧官能团的名称为___和___。
(2)由A生成B的化学方程式为___。
(3)C→I的反应类型为___。
(4)根据已知信息分析,![]() 在酸性KMnO4溶液作用下所得有机产物的结构简式是___。
在酸性KMnO4溶液作用下所得有机产物的结构简式是___。
(5)写出符合下列条件的G的一种同分异构体的结构简式:___。
①属于芳香族化合物,且核磁共振氢谱有4个峰;
②能发生水解反应和银镜反应,且能与FeCl3溶液发生显色反应
(6)康叉丙酮(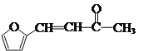 )是一种重要的医药中间体,写出以
)是一种重要的医药中间体,写出以![]() 和
和![]() 为原料制备康叉丙酮的合成路线图___(无机试剂及有机溶剂任用,合成路线图示例见本题题干)。
为原料制备康叉丙酮的合成路线图___(无机试剂及有机溶剂任用,合成路线图示例见本题题干)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向含有0.2 mol氢氧化钠和0.1 mol氢氧化钙的溶液中,持续稳定地通入二氧化碳气体,通入气体为6.72 L(标准状况)时,立即停止,则这一过程中,溶液中离子数目与通入二氧化碳气体体积的关系正确的是(不考虑气体的溶解)
A.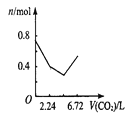 B.
B.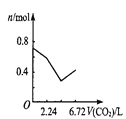 C.
C.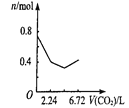 D.
D.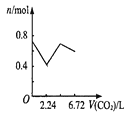
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )


A. 图①中ΔH1=ΔH2+ΔH3
B. 图②在催化剂条件下,反应的活化能等于E1+E2
C. 图③表示醋酸溶液滴定 NaOH溶液和氨水混合溶液的电导率变化曲线
D. 图④可表示由CO(g)生成CO2(g)的过程中要放出566 kJ 热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示2个甲分子反应生成1个丙分子和3个乙分子,下列判断不正确的是
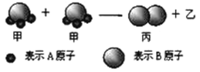
A.1个乙分子中含有2个A原子
B.该反应类型是分解反应
C.相对分子质量:Mr(甲)=Mr(乙)+Mr(丙)
D.该反应一定属于氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下向20 mL 0.1 mol·L-1 Na2CO3溶液中逐滴加入0.1 mol·L-1 HCl溶液40 mL,溶液中含碳元素的各种微粒(CO2因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如图所示。
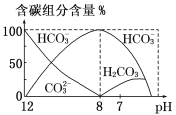
下列说法正确的是
A. 在同一溶液中,H2CO3、HCO3—、CO32—不能大量共存
B. 当pH=7时,溶液中各种离子(CO32—除外)的物质的量浓度的大小关系为:c(Cl-)>c(Na+)>c(HCO3-)>c(H+)=c(OH-)
C. 0.1 mol/L Na2CO3溶液中c(OH-)-c(H+)=c(H2CO3)+c(HCO3-)
D. 当 pH=8时,NaHCO3溶液的物质的量浓度为0.1 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:还原性强弱:I- >Fe2+>Br-,向仅含Fe2+、I-、Br-的溶液中通入适量氯气,溶液中这三种离子的物质的量随消耗氯气物质的量的变化如图所示。下列说法中正确的是
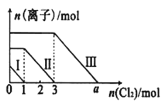
A.a值等于6
B.线段Ⅰ代表Br-的变化情况
C.线段Ⅲ代表Fe2+的变化情况
D.原混合溶液中n(FeBr2)=4mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在室温下,下列五种溶液:①0.1 mol·L-1 NH4Cl溶液 ②0.1 mol·L-1 CH3COONH4溶液 ③0.1 mol·L-1 NH4HSO4溶液 ④0.1 mol·L-1氨水 ⑤0.1 mol·L-1 NH3·H2O和0.1 mol·L-1 NH4Cl混合液
请根据要求填写下列空白:
(1)溶液①呈_______(填“酸”、“碱”或“中”)性,其原因是___________(用离子方程式表示)。
(2)上述5中溶液中,其中水的电离程度最大的是_______(填序号)
(3)在上述①、②、③、④溶液中c(NH4+)浓度由大到小的顺序是_____________。(填序号)
(4) 室温下,测得溶液②的pH=7,则CH3COO-与NH4+浓度的大小关系是c(CH3COO-)______c(NH4+)(填“>”、“<”或“=”)。
(5)用标准盐酸溶液滴定未知浓度的氨水实验。滴定可选用的指示剂为_______(填“甲基橙”或 “酚酞”)。上述滴定开始时滴定管尖嘴处无气泡,完成时滴定管尖嘴处留有气泡,则会导致滴定结果______(填“偏高”或 “偏低”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值。下列说法正确的是
A. 常温常压下,124 g P4中所含P—P键数目为4NA
B. 100 mL 1mol·L1FeCl3溶液中所含Fe3+的数目为0.1NA
C. 标准状况下,11.2 L甲烷和乙烯混合物中含氢原子数目为2NA
D. 密闭容器中,2 mol SO2和1 mol O2催化反应后分子总数为2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com