
【题目】向一定量的NaOH溶液中逐滴加入AlCl3溶液,生成沉淀Al(OH)3的物质的量随AlCl3加入量的变化关系如图所示。则下列离子组在对应的溶液中一定能大量共存的是( )

A. a点对应的溶液中:Na+、Mg2+、![]() 、
、![]()
B. b点对应的溶液中:Na+、K+、![]() 、Cl-
、Cl-
C. c点对应的溶液中:Ag+、Ca2+、![]() 、Cl-
、Cl-
D. d点对应的溶液中:K+、![]() 、
、![]() 、
、![]()
【答案】B
【解析】
向一定量的NaOH溶液中逐滴加入AlCl3溶液,反应开始阶段(b点之前),发生的反应为4OH-+Al3+=AlO2-+2H2O;OH-反应完全后(b~c段),继续加入AlCl3溶液,发生反应:3 AlO2-+ Al3++6H2O=4Al(OH)3↓;AlO2-反应完全后(c点之后),继续加入 AlCl3溶液,Al(OH)3的物质的量保持不变,结合以上分析解答。
向一定量的NaOH溶液中逐滴加入AlCl3溶液,反应开始阶段(b点之前),发生的反应为4OH-+Al3+=AlO2-+2H2O;OH-反应完全后(b~c段),继续加入AlCl3溶液,发生反应:3 AlO2-+ Al3++6H2O=4Al(OH)3↓;AlO2-反应完全后(c点之后),继续加入 AlCl3溶液,Al(OH)3的物质的量保持不变;
A、向NaOH溶液中逐渐加入AlCl3溶液时发生Al3++4OH-=AlO2-+2H2O,3AlO2-+6H2O+Al3+=4Al(OH)3↓,a点时溶液中有大量OH-,与Mg2+、HCO3-不能大量共存,故A错误;
B、b点时溶质为NaCl和NaAlO2,所有离子可以大量共存,故B正确;
C、c点时溶质为NaCl,与Ag+不能大量共存,故C错误;
D、d点时溶质为NaCl和AlCl3,Al3+和CO32-发生双水解而不能大量共存,故D错误;
综上所述,本题选B。


科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
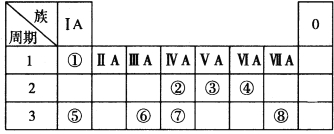
(1)地壳中含量居于第二位的元素在周期表中的位置是____。
(2)②的最高价氧化物的分子式为_____;⑦的最高价氧化物对应水化物的分子式为__。
(3)①、④、⑤三种元素可形成既含离子键又含共价键的离子化合物,该化合物的电子式为_____。
(4)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是___(填字母,双选)。
A.最高正化合价为+6
B.气态氢化物比H2S稳定
C.最高价氧化物对应水化物的酸性比硫酸弱
D.单质在常温下可与氢气化合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关热化学方程式书写与对应表述均正确的是
A. 稀硫酸与0.1 mol/L NaOH 溶液反应:H+(aq)+OH-(aq)= H2O(l) △H = +57.3 kJ·mol1
B. 已知 2C(s)+O2(g)=2CO(g)△H= -221 kJ·mol-1,则C的燃烧热为△H =- 110.5 kJ·mol1
C. 25℃、30MPa 下,将 0.5mol N2 和 1.5molH2 置于密闭的容器中充分反应生成NH3(g),放热 19.3kJ, 其热化学方程式为:N2(g) + 3H2(g) ![]() 2NH3(g) △H= -38.6kJ·mol1
2NH3(g) △H= -38.6kJ·mol1
D. 密闭容器中,0.3mol 硫粉与 0.2mol 铁粉混合加热生成硫化亚铁 0.2mol 时,放出 19.12 kJ 热量, 则 Fe(s)+S(s)=FeS(s)△H= - 95.6 kJ·mol1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(Ⅰ)下图是常见仪器的部分结构。

(1)写出仪器名称A__________,B__________,C__________,D__________。
(2)使用前需检查是否漏水的仪器有____________(填字母)。
(Ⅱ)已知常温下氢氧化铜的Ksp=2×10-20。
(3)某硫酸铜溶液里c(Cu2+)=0.02mol/L,若要生成Cu(OH)2沉淀,应调整溶液pH使之大于_________。
(4)要使0.2mol/ LCuSO4溶液中Cu2+沉淀较为完全(Cu2+浓度降至原来的千分之一),则应向溶液里加入NaOH溶液使溶液pH为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅及其化合物的应用范围很广。下列说法正确的是
A.硅是人类将太阳能转换为电能的常用材料
B.粗硅制备单晶硅不涉及氧化还原反应
C.反应Si+2NaOH+H2O=Na2SiO3+2H2↑中,Si为氧化剂
D.硅能与氢氟酸反应,则硅可以与盐酸反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究化学能与热能的转化,某实验小组设计了如图所示的三套实验装置:
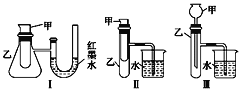
(1)上述3个装置中,不能证明“铜与浓硝 酸反应是吸热反应还是放热反应”的是(不能用手触摸和使用温度计)___________。
(2)某同学选用装置Ⅰ进行实验(实验前U形管里液面左右相平),在甲试管里加入 适量氢氧化钠溶液与稀盐酸,U形管中可观察到的现象是______________,说明该反应属于_____ (填“吸热”或“放热”)反应。
(3)为定量测定(2)中反应的反应热,使50 mL 0.50 mol·L-1盐酸与50 mL0.55 mol·L-1NaOH溶液在简易量热计中进行中和反应.回答下列问题:
①该实验中NaOH的浓度大于HCl的浓度的作用是_________________________。
②实验中若改用60 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1NaOH溶液进行反应,与上述实验相比,所求中和热_________ (填“相等”或“不相等”)。
(4)已知一些化学键的键能数据如表所示:
化学键 | C—H | C—F | H—F | F—F |
键能/kJ·mol-1 | 414 | 489 | 565 | 155 |
请根据键能数据估算CH4(g)和F2(g)反应生成CF4(g)和HF(g)的热化学方程式:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列图像的说法正确的是

A. 图 1 表示:密闭容器中发生的反应 NH2COONH4(s) 2NH3(g)+CO2(g),NH3的体积分数 ψ(NH3)与时间(t)的关系
B. 图 2 表示:一定量饱和氯水中加入 CaCO3 固体,溶液中的 c(Cl-)与加入 CaCO3 物 质的量关系
C. 图3表示:NH4HSO4溶液中加入NaOH固体,溶液中的c(NH4+)与加入NaOH质量 的关系
D. 图4表示:25℃时,Na2S溶液加水稀释,溶液中的c(H+)与加入水的体积的关系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为达到预期的实验目的,下列操作中正确的是( )
A.用玻璃棒蘸取待测液滴在润湿的pH试纸上,测得其pH为12
B.用待测液润洗滴定用的锥形瓶
C.中和热测定的实验中使用的玻璃仪器只有3种
D.在滴定时,左手操作锥形瓶,右手操作滴定管开关
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com