
【题目】铝土矿的主要成分是Al2O3,含有杂质SiO2、Fe2O3、MgO。工业上从铝土矿中提取铝可采用如下工艺流程:

请回答下列问题:
(1)沉淀B的成分是____________(填化学式,下同);
(2)沉淀C的成分是__________;
(3)沉淀F转化为物质M的化学方程式为__________;
(4)由物质M制取铝的化学方程式为____________________;
(5)溶液D中通入过量CO2生成沉淀F的离子方程式为____________________。
【答案】 SiO2 Fe(OH)3、Mg(OH)2 2Al(OH)3![]() Al2O3+3H2O 2Al2O3(熔融)
Al2O3+3H2O 2Al2O3(熔融)![]() 4Al+3O2↑ AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
4Al+3O2↑ AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
【解析】Al2O3、SiO2、Fe2O3、MgO中,Al2O3、SiO2与NaOH溶液反应,MgO、Fe2O3不与NaOH溶液反应;除SiO2不与盐酸反应外,Al2O3、Fe2O3、MgO均与盐酸反应;加入过量盐酸,溶液A为AlCl3、MgCl2、FeCl3,沉淀B为SiO2,加入过量烧碱,沉淀C为Fe(OH)3和Mg(OH)2,溶液D为NaAlO2,通入过量二氧化碳,溶液E为NaHCO3,沉淀F为Al(OH)3,加热分解得到M为Al2O3,经电解可得到Al。
(1)由以上分析可知沉淀B的成分是SiO2,故答案为:SiO2;
(2)沉淀C为Fe(OH)3和Mg(OH)2, 故答案为: Fe(OH)3和Mg(OH)2;
(3)沉淀F为Al(OH)3,加热分解得到M为Al2O3,方程式为2Al(OH)3![]() Al2O3+3H2O,故答案为:2Al(OH)3
Al2O3+3H2O,故答案为:2Al(OH)3![]() Al2O3+3H2O;
Al2O3+3H2O;
(4)Al2O3经电解可得到Al,方程式为2Al2O3(熔融)![]() 4Al+3O2↑,故答案为:2Al2O3(熔融)
4Al+3O2↑,故答案为:2Al2O3(熔融)![]() 4Al+3O2↑;
4Al+3O2↑;
(5)溶液NaAlO2中通入过量CO2生成Al(OH)3沉淀,反应的离子方程式为CO2+AlO2-+2H2O═Al(OH)3↓+HCO3-,故答案为:CO2+AlO2-+2H2O═Al(OH)3↓+HCO3-。


科目:高中化学 来源: 题型:
【题目】已知:H2O(g)===H2O(l) ΔH=Q1 kJ·mol1
C2H5OH(g)===C2H5OH(l) ΔH=Q2 kJ·mol1
C2H5OH(g)+3O2(g)===2CO2(g)+3H2O(g) ΔH=Q3 kJ·mol1
若使46 g酒精液体完全燃烧,最后恢复到室温,则放出的热量为
A.(Q1+Q2+Q3) kJ B.0.5(Q+Q2+Q3) kJ
C.(0.5Q11.5Q2+0.5Q3) kJ D.(3Q1Q2+Q3) kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学对一无色透明溶液进行分析得出该溶液中含有下列某组离子,你认为该组离子应该是
A. Ca2+、H+、HCO3-、Na+ B. Al3+、NO3-、K+、SO42-
C. OH-、CO32-、Cu2+、SO42- D. Fe3+、Mg2+、NO3-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用生石灰(CaO)、纯碱(Na2CO3)和食盐(NaCl)按一定比例混合可制得一种腌制原料,某同学为了探究该原料成份做了以下实验:
该同学取一定量的样品溶于水,主要发生的化学方程式有:____________________________, _____________________________________。
(2)该同学认为(1)过滤后所得的滤液中肯定含有大量的NaOH、NaCl溶质,还可能含有Ca(OH)2或Na2CO3 ,为了探究所得滤液中可能含有的物质是否存在,请你帮他完善实验方案。
实验方案设计如下表所示:
实 验 步 骤 | 实 验 现 象 | 实 验 结 论 | 用离子方程式解释 |
①取少量滤液,滴加适量K2CO3溶液 | 若出现白色沉淀 | 滤液中含Ca(OH)2 | Ⅰ:________________ |
若无白色沉淀 | 滤液中无Ca(OH)2 |
| |
②取少量滤液,______________________________________________ | ⅰ:若出___________ | 滤液中含Na2CO3 | Ⅱ:_______________ |
ⅱ:若无___________ | 滤液中无Na2CO3 |
|
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物在生活及工业生产中有着重要应用。请回答以下问题:
(1)下图是N2(g)、H2(g)与NH3(g)之间转化的能量关系图,则:
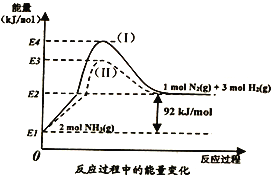
①N2(g)与H2(g)反应生成NH3(g)的热化学方程式为__________________________。
②过程(I)和过程(Ⅱ)的反应热__________(填“相同”或“不同”),原因是_______________。
③一定温度下,在容积为1L的密闭容器中充入1 mol N2(g)、3molH2(g),达到平衡时,混合气体的总量为2.8 mol,则该条件下反应 N2(g)+3H2(g)![]() 2NH3(g)的平衡常数为__________,H2的平衡转化率为__________________________。
2NH3(g)的平衡常数为__________,H2的平衡转化率为__________________________。
(2)用NH3可以消除氮氧化物的污染,已知:
反应I:4NH3(g)+3O2(g)![]() 2N2(g)+6H2O(g) △H1= a kJ/mol
2N2(g)+6H2O(g) △H1= a kJ/mol
反应Ⅱ:N2(g)+O2(g)![]() 2NO(g) △H2= b kJ/mol
2NO(g) △H2= b kJ/mol
反应Ⅲ:4NH3(g)+6NO(g)![]() 5N2(g)+6H2O(g) △H3= c kJ/mol
5N2(g)+6H2O(g) △H3= c kJ/mol
则:反应Ⅱ中的b=______ kJ/mol(用含a、c的代数式表示),反应Ⅲ中的△S________0(填“>”“<”或“=”)。
(3)在恒容的密闭容器中,充入一定量的NH3和NO进行上述反应Ⅲ,测得不同温度下反应体系中NH3的转化率(α)与压强p的关系如图:

①分析得P1_________P2 (填“>”“<”或“=”)。
②下列叙述中,不能判断反应Ⅲ己经达到平衡状态的标志是__________(填序号)。
a. N2的浓度不再改变 b.断裂6molN-H键的同时,有6molH-O键形成
C.容器中压强不再变化 d.混合气体的密度保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质用途的说法中,正确的是
①SiO2可用来制造半导体材料 ②Si可用于制造光导纤维
③Al(OH)3可用于治疗胃酸过多 ④SiO2、Na2CO3和CaCO3可用于制玻璃
A. ①③ B. ③④ C. ①②③ D. ②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环保部门每天通过新闻媒体向社会发布以污染物浓度为标准确定空气质量的信息。这些污染物是( )
A.二氧化硫、氮氧化物、悬浮微粒 B.二氧化硫、氮氧化物、二氧化碳
C.三氧化硫、氮氧化物、悬浮微粒 D.稀有气体、氮氧化物、悬浮微粒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学方程式为3MnO2+6KOH+KClO3![]() 3K2MnO4+KCl+3H2O,下列说法中正确的( )
3K2MnO4+KCl+3H2O,下列说法中正确的( )
A. 反应中MnO2是氧化剂 B. 该反应属于复分解反应
C. KClO3在反应中失去电子 D. 反应中每生成lmol K2MnO4,氧化剂得到2mol电子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com