
【题目】2009年3月1日,“嫦娥一号”卫星准确落于月球东经52.36°、南纬1.50°的预定撞击点。“嫦娥一号”担负的四大科学目标之一是探测下列元素的含量和分布情况:K、Th(钍)、U(铀)、O、Si、Mg、Al、Sb(锑)、Fe、Ti(钛)、Na、I、Cr(铬)、Gd(钆);其中属于主族元素的有( )
A. 7种 B. 8种 C. 9种 D. 10种
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】计算填空
(1)标准状况下,密度为0.75g·L-1的NH3与CH4组成的混合气体中,NH3的体积分数为__________,该混合气体对氢气的相对密度为_________。
(2)19g某二价金属氯化物(ACl2)中含有0.4molCl-,则ACl2的摩尔质量是___;A的相对原子质量是______;ACl2的化学式是_________。
(3)已知agA和bgB恰好完全反应生成0.2molC和dgD,则C的摩尔质量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、根据分子中所含官能团可预测有机化合物的性质。
(1)下列化合物中,常温下易被空气氧化的是______(填字母)。
a.苯 b.甲苯 c.苯甲酸 d.苯酚
(2)苯乙烯是一种重要为有机化工原料。
①苯乙烯的分子式为______。
②苯乙烯在一定条件下能和氢气完全加成,加成产物的一溴取代物有______种。
Ⅱ、按要求写出下列反应的化学方程式:
(1)(CH3)2C(OH)CH(OH)CH2OH发生催化氧化反应:___________________。
(2)1,2-二溴丙烷发生完全的消去反应:_______________________________。
(3)![]() 发生银镜反应:_______________________________。
发生银镜反应:_______________________________。
Ⅲ. 水杨酸的结构简式为: ,用它合成的阿司匹林的结构简式为:
,用它合成的阿司匹林的结构简式为:
(1)请写出将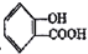 转化为
转化为![]() 的化学方程式__________________。
的化学方程式__________________。
(2)阿司匹林与足量NaOH溶液发生反应的化学方程式___________________。
(3)水杨酸与无水乙醇发生酯化反应的化学方程式_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】连二亚硫酸钠(Na2S2O4)俗称保险粉,是一种强还原剂。工业常用惰性电极电解亚硫酸氢钠的方法制备连二亚硫酸钠,原理装置如图所示,下列说法正确的是
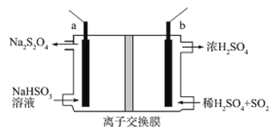
A. b电极应该接电源的负极
B. 装置中所用离子交换膜为阴离子交换膜
C. 电路中每转移1mole-消耗SO2的体积为11.2L
D. a电极的电极反应式为:2HSO3-+2e-+2H+=S2O42-+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下向1L pH=2的醋酸溶液中加入2L pH=2的盐酸,则混合溶液的pH约为(假设混合后溶液体积不变,室温下醋酸的电离平衡常数为1.8×10-5)
A. 2 B. 1.7 C. 2.3 D. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知钠、氯及其化合物间有如下转化关系,
请按要求填空:
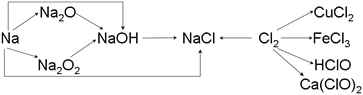
(1)实验室中金属钠通常保存在_______中,一小块金属钠投入水中反应的化学方程式是________________。
(2)Na2O2常用于呼吸面具中,有关反应的化学方程式为_____________________________,_________________________________。
(3)新制的氯水滴入紫色石蕊试液中,观察到的现象是___________________________。
请写出氯气与水反应的化学方程式_______________________________。
(4)工业上用氯气和石灰乳反应制漂白粉,其化学方程式为_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案不可行或结论不正确的是
A. 用湿润的pH试纸测定饱和Na2CO3溶液的pH
B. 通过观察如图中导管水柱的变化,验证铁钉生锈的主要原因是吸氧腐蚀
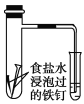
C. 向Mg(OH)2悬浊液中滴加FeCl3溶液,出现红褐色沉淀,说明溶解度:Fe(OH)3<Mg(OH)2
D. 向同pH、同体积的醋酸和盐酸溶液中加入足量镁粉,通过完全反应后收集到的H2体积,比较两种酸的电离程度:醋酸<盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳、氮元素及其化合物与人类的生产生活密切相关,试回答下列有关问题:
(1)NH3极易溶于水,其水溶液俗称氨水。用水稀释0.1molL-1的氨水,溶液中随着水量的增加而减小的是___________(填序号)。
A.![]() B.
B.![]() C.c(H+)c(OH-) D.
C.c(H+)c(OH-) D.![]()
(2)NO2可用氨水吸收生成NH4NO3。25℃时,将amolNH4NO3溶于水,溶液显酸性,原因是______________(用离子方程式表示)。向该溶液中滴加bL氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将________(填“正向”“不”或“逆向”)移动,所滴加氨水的浓度为________mol/L-1。(NH3·H2O的电离平衡常数为Kb=2×10-5)
(3)以甲烷为燃料的新型电池的成本大大低于以氢气为燃料的传统燃料电池,下图是目前研究较多的一类固体氧化物燃料电池的工作原理示意图。

①B电极的反应式为_______________________。
②若用该燃料电池作电源,用石墨作电极电解100 mL 1 mol·L-1的硫酸铜溶液,当两极收集到的气体体积相等时,理论上消耗甲烷的体积为_________(标准状况)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值。下列说法正确的是
A. 密闭容器中,2 mol NO和1molO2充分反应后分子总数为2NA
B. 标准状况下,2.24L甲醇在足量O2中完全燃烧,生成CO2的分子数为0.1NA
C. 常温常压下,28gCO含有的质子数为14NA
D. 常温常压下,30g乙烷含有的共价键数目为6NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com