
【题目】Ⅰ、根据分子中所含官能团可预测有机化合物的性质。
(1)下列化合物中,常温下易被空气氧化的是______(填字母)。
a.苯 b.甲苯 c.苯甲酸 d.苯酚
(2)苯乙烯是一种重要为有机化工原料。
①苯乙烯的分子式为______。
②苯乙烯在一定条件下能和氢气完全加成,加成产物的一溴取代物有______种。
Ⅱ、按要求写出下列反应的化学方程式:
(1)(CH3)2C(OH)CH(OH)CH2OH发生催化氧化反应:___________________。
(2)1,2-二溴丙烷发生完全的消去反应:_______________________________。
(3)![]() 发生银镜反应:_______________________________。
发生银镜反应:_______________________________。
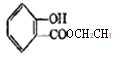
Ⅲ. 水杨酸的结构简式为: ,用它合成的阿司匹林的结构简式为:
,用它合成的阿司匹林的结构简式为:
(1)请写出将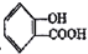 转化为
转化为![]() 的化学方程式__________________。
的化学方程式__________________。
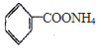
(2)阿司匹林与足量NaOH溶液发生反应的化学方程式___________________。
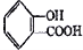
(3)水杨酸与无水乙醇发生酯化反应的化学方程式_____________________。
【答案】d C8H8 6 (CH3)2C(OH)CH(OH)CH2OH+O2![]() (CH3)2C(OH)COCHO+2H2O CH3-CHBr-CH2Br+2NaOH
(CH3)2C(OH)COCHO+2H2O CH3-CHBr-CH2Br+2NaOH![]() CH3-C≡CH↑+2NaBr+2H2O
CH3-C≡CH↑+2NaBr+2H2O ![]() +2Ag(NH3)2OH
+2Ag(NH3)2OH![]()
 +2Ag↓+3NH3+H2O
+2Ag↓+3NH3+H2O 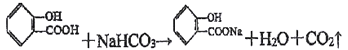
![]()
 +CH3CH2OH
+CH3CH2OH![]()
 +H2O
+H2O
【解析】
Ⅰ(1)苯、甲苯、苯甲酸结构比较稳定,而苯酚具有强还原性,常温下,能够被氧气氧化;
(2)①根据苯乙烯的组成确定苯乙烯的分子式;
②苯环和碳碳双键均能与氢气发生加成反应,生成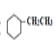 ;该结构共有6种等效氢,据此判断该有机物的一溴取代物的种类;
;该结构共有6种等效氢,据此判断该有机物的一溴取代物的种类;
Ⅱ、(1)在铜作催化剂下,醇羟基被氧化为醛基或羰基,据此写出反应方程式;
(2)1,2-二溴丙烷在氢氧化钠的醇溶液加热,发生消去反应生成不饱和烃,据此写出反应方程式;
(3)![]() 与银氨溶液水浴加热,发生银镜反应,据此写出反应方程式;
与银氨溶液水浴加热,发生银镜反应,据此写出反应方程式;
Ⅲ.(1)酸性:苯甲酸>碳酸>苯酚>HCO3-,所以苯酚与碳酸氢钠溶液不反应,而苯甲酸能够与碳酸氢钠溶液反应生成二氧化碳气体;据此写出反应方程式;
(2)在碱性环境下,羧基与氢氧化钠反应,酯基与氢氧化钠溶液反应,据此写出反应的化学方程式;
(3)羧基与醇羟基能够发生酯化反应,据此写出反应的化学方程式。
Ⅰ(1)苯、甲苯、苯甲酸结构比较稳定,常温下,不能被氧气氧化;而苯酚具有强还原性,常温下,能够被氧气氧化,d正确;综上所述,本题选d。
(2)①苯乙烯的分子式为C8H8 ;综上所述,本题答案是:C8H8。
②苯乙烯在一定条件下能和氢气完全加成,苯环和碳碳双键均能加成,加成产物为 ,该结构共有6种等效氢,如图
,该结构共有6种等效氢,如图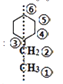 ,所以该有机物的一溴取代物有6种;综上所述,本题答案是:6。
,所以该有机物的一溴取代物有6种;综上所述,本题答案是:6。
Ⅱ、(1)在铜作催化剂下,醇羟基被氧化为醛基和羰基,反应方程式为:(CH3)2C(OH)CH(OH)CH2OH+O2![]() (CH3)2C(OH)COCHO+2H2O;综上所述,本题答案是:(CH3)2C(OH)CH(OH)CH2OH+O2
(CH3)2C(OH)COCHO+2H2O;综上所述,本题答案是:(CH3)2C(OH)CH(OH)CH2OH+O2![]() (CH3)2C(OH)COCHO+2H2O。
(CH3)2C(OH)COCHO+2H2O。
(2)1,2-二溴丙烷在氢氧化钠的醇溶液加热,发生消去反应生成不饱和烃,反应方程式为:CH3-CHBr-CH2Br+2NaOH![]() CH3-C≡CH↑+2NaBr+2H2O;综上所述,本题答案是:CH3-CHBr-CH2Br+2NaOH
CH3-C≡CH↑+2NaBr+2H2O;综上所述,本题答案是:CH3-CHBr-CH2Br+2NaOH![]() CH3-C≡CH↑+2NaBr+2H2O。
CH3-C≡CH↑+2NaBr+2H2O。
(3)![]() 与银氨溶液水浴加热,发生银镜反应,反应方程式为:
与银氨溶液水浴加热,发生银镜反应,反应方程式为: ![]() +2Ag(NH3)2OH
+2Ag(NH3)2OH![]()
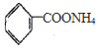 +2Ag↓+3NH3+H2O ;综上所述,本题答案是:
+2Ag↓+3NH3+H2O ;综上所述,本题答案是: ![]() +2Ag(NH3)2OH
+2Ag(NH3)2OH![]()
 +2Ag↓+3NH3+H2O 。
+2Ag↓+3NH3+H2O 。
Ⅲ.(1)苯酚、苯甲酸、碳酸的酸性:苯甲酸>碳酸>苯酚>HCO3-,所以羧基能够与碳酸氢钠溶液反应而酚羟基不反应,将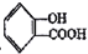 转化为
转化为![]() ,应选择碳酸氢钠溶液;反应的化学方程式:
,应选择碳酸氢钠溶液;反应的化学方程式: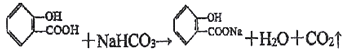 ;综上所述,本题答案是:
;综上所述,本题答案是: 。
。
(2)阿司匹林的结构为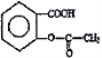 ,在碱性环境下,羧基与氢氧化钠反应,酯基与氢氧化钠溶液反应,反应的化学方程式:
,在碱性环境下,羧基与氢氧化钠反应,酯基与氢氧化钠溶液反应,反应的化学方程式: ![]() ;综上所述,本题答案是:
;综上所述,本题答案是:![]() 。
。
(3)水杨酸结构简式为: ,与乙醇发生酯化反应生成酯,化学方程式:
,与乙醇发生酯化反应生成酯,化学方程式: +CH3CH2OH
+CH3CH2OH![]()
 +H2O;综上所述,本题答案是:
+H2O;综上所述,本题答案是:  +CH3CH2OH
+CH3CH2OH![]()
 +H2O。
+H2O。


 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 1mol萘(![]() )含有5mol碳碳双键
)含有5mol碳碳双键
B. CH3CH=CHCH2OH属于不饱和烃
C. 可用溴水鉴别苯、四氯化碳、酒精
D. 尿素[CO(NH2)2]的含氮质量分数比碳酸氢铵的低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度为T时,向2.0 L恒容密闭容器中充入1.0 mol PCl5,发生反应PCl5(g)![]() PCl3(g)+Cl2(g),经过一段时间后达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是
PCl3(g)+Cl2(g),经过一段时间后达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是
t / s | 0 | 50 | 150 | 250 | 350 |
n(PCl3) / mol | 0 | 0. 16 | 0. 19 | 0. 20 | 0. 20 |
A. 反应在前50 s 的平均速率ν(Cl2)= 0. 0032 mol·L-1·s-1
B. 保持其他条件不变,升高温度,平衡时c(PCl3)= 0. 13 mol·L-1,则反应的ΔH<0
C. 相同温度下,起始时向容器中充入1. 0 mol PCl5、0. 20 mol PCl3 和0. 20 mol Cl2 ,反应达到平衡前ν(正)<ν(逆)
D. 相同温度下,起始时向容器中充入2. 0 mol PCl3 和2. 0 mol Cl2 ,达到平衡时,PCl3 的转化率大于80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,A是可用来对自来水进行消毒的黄绿色单质气体,A、B、C、D、E都含X元素,其转化关系如图所示:

(1)请分别写出下列物质的化学式(如为溶液请填溶质的化学式):
A________、 B________、 D________、E________。
(2)写出下列反应的化学方程式(请注明反应条件):
A+H2O: ____________________;
A → D: ____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在150℃时使NH4HCO3分解,将所产生的气体依次通过Na2O2和浓H2SO4,则Na2O2增重ag,浓H2SO4增重bg;若将上述气体先通过浓H2SO4,则使酸液增重dg,再通过Na2O2,则使之增重cg。设气体皆完全被吸收,a、b、c、d质量由大到小的排列顺序正确的是
A.d a c bB.b c a dC.a c b dD.d c b a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镇痛药物J的合成方法如下:

已知:

(1)B的名称为_________________;F的结构简式为_______________。
(2)C中含氧官能团名称为_______________;②的反应类型为____________反应。
(3)③的化学方程式为_______________________________ 。
(4)有机物K分子组成比F少两个氢原子,符合下列要求的K的同分异构体有________种。
A.遇FeCl3显紫色 B.苯环上有三个取代基
(5)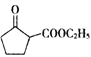 是一种重要的化工中间体。以环已醇(
是一种重要的化工中间体。以环已醇(![]() )和乙醇为起始原料,结合己知信息选择必要的无机试剂,写出
)和乙醇为起始原料,结合己知信息选择必要的无机试剂,写出 的合成路线____________________。(已知:RCH=CHR’
的合成路线____________________。(已知:RCH=CHR’![]() RCOOH+R’COOH,R、R'为烃基。用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)
RCOOH+R’COOH,R、R'为烃基。用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2009年3月1日,“嫦娥一号”卫星准确落于月球东经52.36°、南纬1.50°的预定撞击点。“嫦娥一号”担负的四大科学目标之一是探测下列元素的含量和分布情况:K、Th(钍)、U(铀)、O、Si、Mg、Al、Sb(锑)、Fe、Ti(钛)、Na、I、Cr(铬)、Gd(钆);其中属于主族元素的有( )
A. 7种 B. 8种 C. 9种 D. 10种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com