
【题目】【化学——选修3:物质结构与性质】
X、Y、Z、W为前四周期元素且原子序数依次增大,X的电子层数等于核外电子数,Y元素基态原子核外未成对电子数为2且X与Y形成的化合物在常温下为常见的液体R,Z元素原子最外电子层上s、p电子数相等,W基态原子3d轨道的电子数是4s轨道电子数的3倍。请回答下列问题:
(1)Y基态原子的价电子排布图为 ,其第一电离能在同周期元素中由大到小排第 位。
(2)W的元素名称为 ,其基态原子核外有 种空间运动状态不同的电子。
(3)R的中心原子采取的杂化方式为 ,写出R的一个等电子体: 。(填化学式)。
(4)Z与Y在一定条件下可形成高硬度的化合物,该化合物的晶体类型为 ,其由Z、Y构成的最小环为 元环。
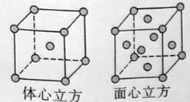
(5)W的单质在900℃以下为α型体心立方晶胞,910℃以上W转变为γ型面心立方晶胞,晶胞结构分别如图所示。两种晶体中距离最近的铁原子间距离相同。则在800℃和1000℃下,铁的密度之比为 。
【答案】(1)![]() 4
4
(2)铁;26;
(3)sp3;H2S(或NH等合理答案);
(4)原子晶体;12;
(5)0.92︰1(或![]() ︰8)。
︰8)。
【解析】
试题分析:根据题目信息可推断:X为H元素,Y为O元素,R为H2O,Z为Si元素,W为Fe元素。
(1)O原子的价电子排布图为![]() ,根据同周期元素第一电离能的变化规律可知,第二周期元素第一电离能由大到小的顺序为Ne>F>N>O>C>Be>B>Li,所以O元素的第一电离能在同一周期中排第4位;
,根据同周期元素第一电离能的变化规律可知,第二周期元素第一电离能由大到小的顺序为Ne>F>N>O>C>Be>B>Li,所以O元素的第一电离能在同一周期中排第4位;
(2)W元素为铁,其原子核外有26个电子,每个电子的运动状态均不同,则有26种空间运动状态不同的电子;
(3)R为H2O,其中心原子的杂化方式为sp3,其等电子体有H2S、NH2-等;
(4)Si与O在一定条件下形成的高硬度的化合物为SiO2,其晶体类型为原子晶体,其结构中由Si、O构成的最小环中有12个原子,即12元环;
(5)在1个体心立方晶胞中,实际含有Fe原子个数是1+8×1/8=2个,距离最近的Fe原子为顶角与体心的Fe原子,设其距离为a,则晶胞边长为![]() 。又设一个Fe原子的质量为m,则其密度为ρ(体心)
。又设一个Fe原子的质量为m,则其密度为ρ(体心)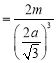 。在1个面心立方晶胞中,实际含有Fe原子的个数是8×1/8+6×1/3=4个,距离最近的Fe原子为顶角与面心的Fe原子,其距离也为a,所以晶胞边长是
。在1个面心立方晶胞中,实际含有Fe原子的个数是8×1/8+6×1/3=4个,距离最近的Fe原子为顶角与面心的Fe原子,其距离也为a,所以晶胞边长是![]() ,密度为ρ(面心)
,密度为ρ(面心)![]() ,故
,故![]() 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种元素的原子序数依次递增。已知:
①F的原子序数为29,其余均为短周期主族元素;
②A的内层电子总数是最外层电子数的一半;
③C、E同主族且C原子最外层电子数是次外层电子数的3倍;
④D是金属性最强的短周期元素。完成下列问题
(1)F在元素周期表的位置______________。
(2)B、C、D、E的原子半径由小到大顺序是_________ (用元素符号表示)。
(3)已知D在C的单质中燃烧生成淡黄色的固体化合物甲,甲的化学式为_______________,电子式为_______,甲中的化学键类型为____________________。
(4)A的单质与E的最高价含氧酸反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】正丁醛经催化加氢可制备1-丁醇。为提纯含少量正丁醛杂质的1-丁醇,现设计如下路线:
![]()
已知:①正丁醛与饱和NaHSO3溶液反应可生成沉淀;②乙醚的沸点是34℃,难溶于水,与1-丁醇互溶;③1-丁醇的沸点是118℃。则操作1~4分别是( )
A.萃取、过滤、蒸馏、蒸馏 B.过滤、分液、蒸馏、萃取
C.过滤、蒸馏、过滤、蒸馏 D.过滤、分液、过滤、蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质的晶体中,化学键类型相同、晶体类型也相同的是( )
A. CO2和H2O B. CCl4和KCl C. NaCl和HCl D. SO2和SiO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在密闭容器中进行如下反应:2SO2(g)+O2(g)![]() 2SO3(g)。当SO2、O2、SO3的浓度不再改变时,下列说法正确的是
2SO3(g)。当SO2、O2、SO3的浓度不再改变时,下列说法正确的是
A.SO2、O2完全转化为SO3
B.正、逆反应速率相等且等于零
C.反应已达到化学平衡状态
D.SO2、O2、SO3的浓度一定相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
步骤 | 实验过程 | 实验用品 |
I | 将干海带灼烧灰化 |
|
II | 将海带灰溶解、过滤 |
|
III | 氧化滤液中的I-,反应的离子方程式为 ② |
|
IV | 取少量III中反应后溶液于试管中,加入少量CCl4并振荡后静置,观察到 ③ ,说明海带中含有碘元素 |
|
(2)利用新制氨水、1mol/L NaBr溶液、淀粉液、以及II中所得溶液,验证卤素单质氧化性的相对强弱。
V分别取5mL 1mol/L NaBr溶液于两支小试管中
VI向两支试管中分别滴加5滴新制氯水,溶液均变为黄色
VII向其中一支试管中继续滴加新制氯水,直至溶液变为棕红色
VIII……
④请写出步骤VI中反应的离子方程式 ;为验证溴的氧化性强于碘,步骤VIII的操作和现象是: ,溶液变为黄色。再加入 ,溶液变为蓝色。
⑤步骤VII的目的是 。
⑥氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下, ,得电子能力逐渐减弱,非金属性减弱。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分类或归类正确的是:①铝热剂、纯净矿泉水、冰水混合物均为混合物 ②NaOH、HD、H2O均为化合物③明矾、烧碱、硫酸均为强电解质④C60、金刚石、石墨均为碳的同素异形体⑤碘酒、淀粉溶液、水雾、纳米材料均为胶体
A.①③③⑤ B.③④⑤ C.②④⑤ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是原子序数依次增大的同一短周期元素,W、X是金属元素,Y、Z是非金属元素。请回答下列问题:
(1)W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为 。
(2)W与Y可形成化合物W2Y,该化合物的电子式为 。
(3)Y在周期表中的位置是 。
(4)比较W、X、Y、Z四种元素简单离子的半径大小(用化学式表示,下同): > > > ;比较Y、Z的气态氢化物稳定性强弱: > 。
(5)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为: 。
(6)Z的最高价氧化物为无色液体,0.25mol该物质与一定量水混合得到一种稀溶液,并放出Q kJ的热量,写出该反应的热化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝铁合金在微电机中有广泛应用,某兴趣小组为利用废弃的铝铁合金设计了如下实验流程制备聚合硫酸铁和明矾:
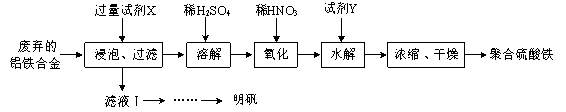
(1)聚合硫酸铁是一种无毒无害、化学性质稳定、能与水混溶的新型絮凝剂,微溶于乙醇,其化学式可表示为[Fe2(OH)x(SO4)y]n。
①聚合硫酸铁可用于净水的原理是 。
②有人认为上述流程中的“氧化”设计存在缺陷,请提出改进意见: ;浓缩时向其中加入一定量的乙醇,加入乙醇的目的是 。
③加入试剂Y的目的是调节pH,所加试剂Y为 ;溶液的pH对[Fe2(OH)x(SO4)y]n 中x的值有较大影响(如图1所示),试分析pH过小(pH<3)导致聚合硫酸铁中x的值减小的原因: 。
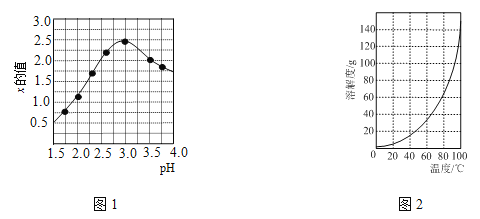
(2)明矾是一种常见铝钾硫酸盐。
①为充分利用原料, 试剂X应为 。
②请结合图2所示的明矾溶解度曲线,补充完整由滤液Ⅰ制备明矾晶体的实验步骤(可选用的试剂:废弃的铝铁合金、稀硫酸、NaOH溶液和酒精):向滤液Ⅰ中加入足量的含铝废铁屑至不再有气泡产生,过滤, 。将溶液 、 、过滤、并用酒精洗涤、干燥,最终得到明矾晶体。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com