
设NA为的值,下列叙述正确的是
A.常温下,1L 0.1mol·L-1的NH4NO3溶液中氮原子数为0.2NA
B.1 mol羟基中电子数为10 NA
C.在反应KIO3 + 6HI = KI + 3I2 + 3H2O中,每生成3 mol I2 转移的电子数为6 NA
D.常温常压下,22.4L乙烯中C--H键数为4 NA
 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:高中化学 来源:2015-2016学年山西省太原市高一上学期阶段测化学试卷(解析版) 题型:选择题
下列试剂中需要张贴右图标志的是

A.HNO3 B.CuO C.NaCl D.C2H5OH
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高二上学期期中(理)化学试卷(解析版) 题型:选择题
用CH4催化还原NOx,可以消除氮氧化物的污染。例如:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH=-1 160 kJ·mol-1
下列说法不正确的是
A.若用标准状况下4.48 L CH4还原NO2生成N2和水蒸气,放出的热量为173.4 kJ
B.由反应①可推知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(l) ΔH<-574 kJ·mol-1
C.反应①和②生成等物质的量的CO2时转移的电子数相同
D.反应②中当4.48 L CH4反应完全时转移的电子总数为1.60 mol
查看答案和解析>>
科目:高中化学 来源:2016届浙江省东阳市高三上学期12月月考化学试卷(解析版) 题型:实验题
聚合硫酸铁又称聚铁,化学式为[Fe2(OH)n(SO4)3-0.5n]m, 广泛用于污水处理。实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁和绿矾(FeSO4·7H2O),过程如下:
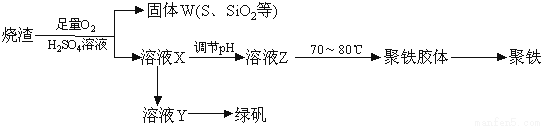
验证固体W焙烧后产生的气体含有SO2的方法是:
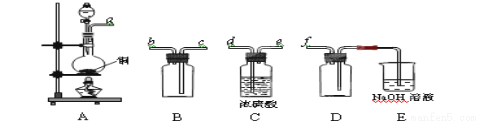
(2)实验室制备、收集干燥的SO2,所需仪器如下。装置A产生SO2,按气流方向连接各仪器接口,顺序为a→____→____→____→____→f。装置A中发生反应的化学方程式为_________________。
(3)制备绿矾时,向溶液X中加入过量__________,充分反应后,经过滤操作得到溶液Y,再经浓缩、结晶等步骤得到绿矾。过滤所需的玻璃仪器有_______________
(4)欲测定溶液Y中Fe2+的浓度,需要用容量瓶配制KMnO4标准溶液,用KMnO4标准溶液滴定时应选用________滴定管(填“酸式”或“碱式”)。
(5)溶液Z的pH影响聚铁中铁的质量分数。若溶液Z的pH偏小,将导致聚铁中铁的质量分数______(填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源:2016届浙江省东阳市高三上学期12月月考化学试卷(解析版) 题型:选择题
下列各组物质相互混合反应后,最终有白色沉淀生成的是
①金属钠投入到FeCl3溶液中;②过量Ba(OH)2溶液和明矾溶液混合;③少量Ca(OH)2投入过量NaHCO3溶液中;④向NaAlO2溶液中通入过量CO2;⑤向饱和Na2CO3溶液中通入足量CO2
A.①③④⑤ B.只有①②⑤ C.只有①④⑤ D.只有②③④⑤
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省高二上学期期中理综化学试卷(解析版) 题型:选择题
右图是模拟电化学反应的装置图。下列有关叙述中,不正确的是

A.X为铜棒,Y为CuSO4溶液,开关K置于M处,铜棒质量将增加,此时外电路中的电子向铜电极移动
B.X为铜棒,Y为CuSO4溶液,开关K置于N处,铁棒质量将增加,溶液中Cu2+浓度将减小
C.X为碳棒,Y为NaCl溶液,开关K置于N处,溶液中的阳离子向铁电极移动
D.X为锌棒,Y为NaCl溶液,开关K置于M处,可减缓铁的腐蚀,这种方法称为牺牲阳极的阴极保护法
查看答案和解析>>
科目:高中化学 来源:2016届四川省资阳市高三上学期第一次诊断性测试理综化学试卷(解析版) 题型:选择题
下列实验操作或结论正确的是
A.鉴别乙烷与乙烯或除去乙烷中的少量乙烯杂质都可用高锰酸钾酸性溶液
B.某同学需用480 mL 2.0 moI·L-1氢氧化钠溶液进行实验,则配制该溶液时他称取氢氧化钠固体质量一定是38.4 g
C.向含Fe3+的溶液中加入KSCN溶液时一定有红褐色沉淀产生
D.硝酸钾和稀硫酸的混合溶液中加入铜粉后,溶液会慢慢变蓝
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省贵阳市新天学校高一上学期期中测试化学试卷(解析版) 题型:填空题
标出Zn + H2SO4 === ZnSO4 +H2↑氧化还原反应的电子转移情况,并指出氧化剂和还原剂。
(1)氧化剂是______________;
(2)还原剂是______________.
(3)电子转移情况如下:______________
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省高二上学期期中测试化学试卷(解析版) 题型:填空题
在2L密闭容器内,800℃时反应2NO(g)+O2(g)
 2NO2(g)△H=a KJ·mol-1体系中,n(NO)随时间变化如下表:
2NO2(g)△H=a KJ·mol-1体系中,n(NO)随时间变化如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)写出该反应的平衡常数表达式:K= 。已知:K(300℃)>K(350 ℃),
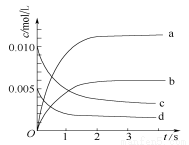 则a 0(填>,<或=)。
则a 0(填>,<或=)。
(2)用NO表示从0~2 s内该反应的平均速率v(NO)= 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com