
某研究小组为了探究一种无机矿物盐X(仅含四种元素)的组成和性质,设计并完成了如下实验:
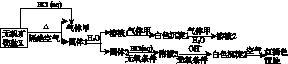
另取10.80 g X在惰性气流中加热至完全分解,得到6.40 g固体1。请回答如下问题:
(1)画出白色沉淀1中金属元素的原子结构示意图:________________。写出气体甲的电子式:________。
(2)X的化学式是________,在惰性气流中加热X至完全分解的化学方程式为__________________________________________________________。
(3)白色沉淀2在空气中变成红褐色沉淀的原因是______________________________(用化学反应方程式表示)。
(4)一定条件下,气体甲与固体1中的某种成分可能发生氧化还原反应,写出一个可能的化学反应方程式:_____________________________________________________,并设计实验方案验证该反应的产物:__________________________________________________
________________________________________________________________________。
(1)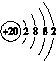
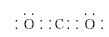
(2)CaFe(CO3)2 CaFe(CO3)2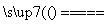 CaO+FeO+2CO2↑
CaO+FeO+2CO2↑
(3)4Fe(OH)2+2H2O+O2===4Fe(OH)3
(4)2FeO+CO2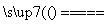 Fe2O3+CO
Fe2O3+CO
检测Fe2O3:将固体用稀盐酸溶解,加入KSCN溶液若显红色,表明产物中有Fe(Ⅲ)
检测CO:将气体通过灼热CuO,黑色固体变红色
[解析] 由白色沉淀在空气中可转化为红褐色沉淀知X中含有铁元素,由X与盐酸反应生成气体甲,甲又能与溶液1反应生成白色沉淀且该白色沉淀又可在水中继续与甲反应,故甲是CO2。由实验过程知X中含有+2价的铁、还含有CO ,另一种金属可能是+2价的钙,故X的化学式为CaFe(CO3)2,X分解得到CO2、CaO、FeO。高温下FeO与CO2反应生成CO,另一种产物可能是Fe2O3。将反应后所得到的固体用稀硫酸溶解,然后用KSCN溶液检验是否含有Fe3+,将气体产物通过热的CuO固体,根据固体变红色可确定CO2中有CO。
,另一种金属可能是+2价的钙,故X的化学式为CaFe(CO3)2,X分解得到CO2、CaO、FeO。高温下FeO与CO2反应生成CO,另一种产物可能是Fe2O3。将反应后所得到的固体用稀硫酸溶解,然后用KSCN溶液检验是否含有Fe3+,将气体产物通过热的CuO固体,根据固体变红色可确定CO2中有CO。


 全程金卷系列答案
全程金卷系列答案 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:
关于下图所示的原电池,下列说法正确的是( )

A、电子从锌电极通过检流计流向铜电极
B、盐桥中的阴离子向硫酸铜溶液中迁移
C、锌电极发生还原反应,铜电极发生氧化反应
D、铜电极上发生的电极反应是:2H++2e-===H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
KMnO4溶液常用做氧化还原反应滴定的标准液,由于KMnO4的强氧化性,它的溶液易被空气中或水中某些少量还原性物质还原,生成难溶性物质MnO(OH)2,因此精确配制KMnO4标准溶液的操作是:
(1)称取稍多于所需量的KMnO4固体溶于水,将溶液加热并保持微沸l h;
(2)用微孔玻璃漏斗过滤除去难溶的MnO(OH)2;
(3)过滤得到的KMnO4溶液贮存于棕色试剂瓶放在暗处:
(4)利用氧化还原滴定方法,在70℃-80℃条件下用基准试剂(纯度高、稳定性好的物质如:草酸)溶液测定其浓度。
回答下列问题:
(1)为什么要称取稍多于所需的KMnO4固体? 。
(2)通常使用的酸性高锰酸钾溶液,是在高锰酸钾溶液滴入 (填试剂名称)使溶液呈酸性。
(3)若准确称取W g草酸晶体(H2C2O4·2H2O)溶于水配成500 mL水溶液,取25.00 mL置于锥形瓶中,用高锰酸钾溶液滴定至终点,消耗高锰酸钾溶液V mL。
①配制高锰酸钾溶液必须用到的玻璃仪器除了烧杯和玻璃棒外还有
②写出滴定过程中对应的离子方程式
KMnO4溶液的物质的量浓度为________________mol/L;
③若滴定前平视,滴定后俯视,则测得的浓度值将________(填“偏高”或“偏低”)
④达到滴定终点的现象为
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应过程中,同时有离子键、极性共价键和非极性共价键的断裂和形成的反应是
A.NH4Cl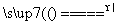 NH3↑+HCl↑
NH3↑+HCl↑
B.NH3+CO2+H2O===NH4HCO3
C.2NaOH+Cl2===NaCl+NaClO+H2O
D.2Na2O2+2CO2===2Na2CO3+O2
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E、F六种短周期主族元素,原子序数依次增大。其中B的单质在常温下为双原子分子,它与A的单质可形成气态分子X,X的水溶液呈碱性;D的简单阳离子与X具有相同电子数,且D是同周期元素中原子半径最大的元素;E元素的原子最外层比次外层少两个电子,C、F两种元素的原子最外层共有13个电子。则
(1)B的原子结构示意图为______________________________________;
X的化学名称为________。
(2)B单质的结构式为________;E的气态氢化物的结构式为________;C与D形成的两种化合物中,其中一种物质含有两种类型的化学键,分别为________,该物质属于________(填“离子化合物”或“共价化合物”)。
(3)B、C、E分别与A形成的化合物中最稳定的是____________(写化学式)。
(4)D是同周期简单阳离子中离子半径最________的元素。
(5)F的单质在反应中常作________剂(填“氧化”或“还原”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
根据原子结构及元素周期律的知识,下列推断正确的是( )
A.同主族元素含氧酸的酸性随核电荷数的增加而减弱
B.核外电子排布相同的微粒化学性质也相同
C.Cl-、S2-、Ca2+、K+半径逐渐减小
D. 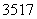 Cl与
Cl与 Cl得电子能力相同
Cl得电子能力相同
查看答案和解析>>
科目:高中化学 来源: 题型:
元素周期表中第ⅦA族元素的单质及其化合物的用途广泛。
(1)与氯元素同族的短周期元素的原子结构示意图为________。
(2)能作为氯、溴、碘元素非金属性(原子得电子能力)递变规律的判断依据是________(填序号)。
a.Cl2、Br2、I2的熔点
b.Cl2、Br2、I2的氧化性
c.HCl、HBr、HI的热稳定性
d.HCl、HBr、HI的酸性
(3)工业上,通过如下转化可制得KClO3晶体:
NaCl溶液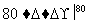 NaClO3溶液
NaClO3溶液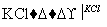 KClO3晶体①完成Ⅰ中反应的总化学方程式:
KClO3晶体①完成Ⅰ中反应的总化学方程式:
 NaCl+
NaCl+ H2O===
H2O=== NaClO3+
NaClO3+ ________。
________。
②Ⅱ中转化的基本反应类型是________________,该反应过程能析出KClO3晶体而无其他晶体析出的原因是____________________________________。
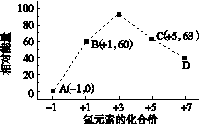
(4)一定条件下,在水溶液中1 mol Cl-、ClO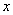 (x=1,2,3,4)的能量(kJ)相对大小如右图所示。
(x=1,2,3,4)的能量(kJ)相对大小如右图所示。
①D是________(填离子符号)。
②B→A+C反应的热化学方程式为________________(用离子符号表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素W、X、Y、Z的原子序数依次增大,其简单离子都能破坏水的电离平衡的是
A. W2-、X+ B. X+、 Y3+
C. Y3+、 Z2- D. X+、 Z2-
查看答案和解析>>
科目:高中化学 来源: 题型:
在t℃下,某反应达到平衡,平衡常数K=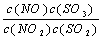 。恒容时,温度升高,NO浓度减小。下列说法正确的是 ( )
。恒容时,温度升高,NO浓度减小。下列说法正确的是 ( )
A.该反应的焓变为正值
B.K表达式中,C(SO3)指反应在该条件下达到化学平衡时SO3的物质的量浓度
C.升高温度,逆反应速率减小
D.该反应化学方程式为:NO+SO3 NO2+SO2
NO2+SO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com