
关于下图所示的原电池,下列说法正确的是( )

A、电子从锌电极通过检流计流向铜电极
B、盐桥中的阴离子向硫酸铜溶液中迁移
C、锌电极发生还原反应,铜电极发生氧化反应
D、铜电极上发生的电极反应是:2H++2e-===H2↑
科目:高中化学 来源: 题型:
[物质结构与性质]原子序数依次增大的X、Y、Z、Q、E五种元素中,X元素原子核外有三种不同的能级且各个能级所填充的电子数相同,Z是地壳内含量(质量分数)最高的元素,Q原子核外的M层中只有两对成对电子,E元素原子序数为29。请用元素符号或化学式回答下列问题:
(1)X、Y、Z的第一电离能由小到大的顺序为 ▲ ;
(2)已知YZ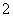 与XQ2互为等电子体,则1 mol YZ
与XQ2互为等电子体,则1 mol YZ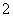 中含有π键数目为____▲___;
中含有π键数目为____▲___;
(3)Z的气态氢化物沸点比Q的气态氢化物高的多,其原因是 ▲ ;
 (4)X、Z与氢元素可形成化合物H2X2Z4,常用作工业除锈剂。H2X2Z4分子中X的杂化方式为 ▲ ;
(4)X、Z与氢元素可形成化合物H2X2Z4,常用作工业除锈剂。H2X2Z4分子中X的杂化方式为 ▲ ;
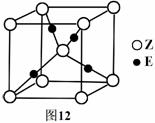
(5)E原子的核外电子排布式为 ▲ ;E有可变价态,它的某价态的离子与Z的阴离子形成晶体的晶胞如图12所示,该晶体的化学式为 ▲ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
若某原子在处于能量最低状态时,外围电子排布式为4d15s2,则下列说法正确的是
A.该元素原子最外层共有3个电子
B.该元素位于第五周期ⅡA族
C.该元素原子核外第N层上共有9个不同状态的电子
D.该元素原子第四电子层上有5个空轨道
查看答案和解析>>
科目:高中化学 来源: 题型:
要从苯酚的乙醇溶液中回收苯酚,有下列操作:
①蒸馏;②过滤;③静置分液;④加入足量金属钠;⑤通入过量CO2;⑥加入足量NaOH溶液;⑦加入足量FeCl3溶液;⑧加入乙酸与浓H2SO4混合加热,合理的步骤是( )
A.④⑤③ B.⑥①⑤③
C.⑧① D.⑧②⑤③
查看答案和解析>>
科目:高中化学 来源: 题型:
最近科学家获得了一种稳定性好、抗氧化能力强的活性化合物A,其结构如下:
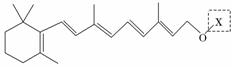
在研究其性能的过程中,发现结构片段X对化合物A的性能起了重要作用。为了研究X的结构,将化合物A在一定条件下水解只得到B(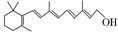 )和C。经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生。
)和C。经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生。
请回答下列问题:
(1)化合物B能发生下列哪些类型的反应________。
A.取代反应 B.加成反应
C.缩聚反应 D.氧化反应
(2)写出化合物C所有可能的结构简式_______________________________。
(3)化合物C能经下列反应得到G(分子式为C8H6O2,分子内含五元环):
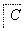
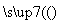

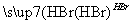

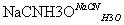
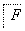
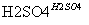
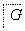
已知:RCOOH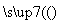 RCH2OH,RX
RCH2OH,RX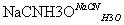 RCOOH
RCOOH
①确认化合物C的结构简式为_______________________________________。
②F→G反应的化学方程式为________________。
③化合物E有多种同分异构体,1H核磁共振谱图表明,其中某些同分异构体含有苯环,且苯环上有两种不同化学环境的氢,写出这些同分异构体中任意三种的结构简式________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中不正确的是( )
A、电解池的阳极发生氧化反应,阴极发生还原反应
B、原电池跟电解池连接后,电子从原电池负极流向电解池阳极
C、电镀时,电镀池里的阳极材料发生氧化反应
D、电解饱和食盐水时,阴极得到氢氧化钠溶液和氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
我国首创以铝—空气—海水电池作为能源的新型海水标志灯,它以海水为电解质溶液,靠空气中的氧气使铝不断氧化而产生电流。只要把灯放入海水中数分钟,就会发生耀眼的白光。则该电源负极材料为____________,正极材料为____________,正、负极反应分别是________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究小组为了探究一种无机矿物盐X(仅含四种元素)的组成和性质,设计并完成了如下实验:
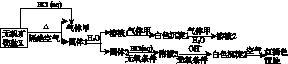
另取10.80 g X在惰性气流中加热至完全分解,得到6.40 g固体1。请回答如下问题:
(1)画出白色沉淀1中金属元素的原子结构示意图:________________。写出气体甲的电子式:________。
(2)X的化学式是________,在惰性气流中加热X至完全分解的化学方程式为__________________________________________________________。
(3)白色沉淀2在空气中变成红褐色沉淀的原因是______________________________(用化学反应方程式表示)。
(4)一定条件下,气体甲与固体1中的某种成分可能发生氧化还原反应,写出一个可能的化学反应方程式:_____________________________________________________,并设计实验方案验证该反应的产物:__________________________________________________
________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com