
【题目】下列化学用语的表达正确的是( )
A. 原子核内有10个中子的氧原子:![]() O
O
B. 氯原子的结构示意图:![]()
C. Fe3+的最外层电子排布式:3s23p63d5
D. 基态铜原子的外围电子轨道表示式:![]()
 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:
【题目】化学兴趣小组对某品牌牙膏中摩擦剂成分及其含量进行以下探究:
查得资料:该牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其它成分遇到盐酸时无气体生成。
I.摩擦剂中氢氧化铝的定性检验取适量牙膏样品,加水充分搅拌、过滤。
(1)往滤渣中加入过量NaOH溶液,过滤。氢氧化铝与NaOH溶液反应的离子方程式是_______。
(2)往(1)所得滤液中先通入过量二氧化碳,再加入过量稀盐酸。观察到的现象是________。
II.牙膏样品中碳酸钙的定量测定
利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数。

依据实验过程回答下列问题:
(3)实验过程中需持续缓缓通入空气。其作用除了可搅拌B、C中的反应物外,还有:________。
(4)D装置的作用是_________。
(5)C中反应的离子方程式是____________。
(6)下列各项措施中,不能提高测定准确度的是________(填标号)。
①在加入盐酸之前,应排净装置内的CO2气体②滴加盐酸不宜过快③在A-B之间增添盛有浓H2SO4的洗气装置④在B-C之间增添盛有饱和NaHCO3溶液的洗气装置
(7)实验中准确称取10.00g样品三份,进行三次测定,测得BaCO3平均质量为3.94g。则样品中碳酸钙的质量分数为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)反应3Fe(S)+4H2O(g)=Fe3O4(s)+4H2(g)在一可变的容积的密闭容器中进行,试回答:
①增加Fe的量,其正反应速率的变化是_______(填增大、不变、减小,以下相同)
②将容器的体积缩小一半,其正反应速率________
③保持体积不变,充入N2使体系压强增大,其正反应速率________。
④保持压强不变,充入N2使容器的体积增大,其正反应速率_______。
(2)将等物质的量的A和B,混合于2 L的密闭容器中,发生如下反应:
3A(g)+B(g) xC(g)+2D(g),5 min后测得c(D)=0.5 mol·L-1,c(A)∶c(B)=3∶5,C的反应速率是0.1 mol·L-1·min-1。
①A在5 min末的浓度是___________。② v(B) =___________。 ③ x=_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备 1,2 —二溴乙烷的反应原理如下:①CH3CH2OH在浓硫酸170℃条件下生成CH2=CH2②CH2=CH2与Br2反应生成BrCH2CH2Br。现用少量溴和50gCH3CH2OH制备1,2 —二溴乙烷。回答下列问题:
(1)制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是_______。
A 加快反应速度 B 引发反应 C 防止乙醇挥发 D 减少副产物乙醚生成
(2)判断该制备反应已经结束的最简单方法是___________________。
(3)将 1,2 —二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在_____层。
(4)若产物中有少量副产物乙醚,可用____________的方法除去。
(5)若最终得到纯净1,2 —二溴乙烷94g,本实验的产率是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列我国科研成果所涉及材料中,主要成分为同主族元素形成的无机非金属材料的是
|
|
|
|
A.4.03米大口径碳化硅反射镜 | B.2022年冬奥会聚氨酯速滑服 | C.能屏蔽电磁波的碳包覆银纳米线 | D.“玉兔二号”钛合金筛网轮 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】M(NO3)2热分解的化学方程式为:2M(NO3)2 ![]() 2MO+4NO2↑+O2↑。加热29.6 g M(NO3)2使其完全分解,在标准状况下收集11200 mL的气体,那么M的摩尔质量是( )
2MO+4NO2↑+O2↑。加热29.6 g M(NO3)2使其完全分解,在标准状况下收集11200 mL的气体,那么M的摩尔质量是( )
A.64 g·mol-1B.24 g·mol-1
C.65 g·mol-1D.40 g·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W原子序数依次增大,它们原子的最外层电子数之和为14。X与Z同主族,Y与W同主族,且X的原子半径小于Y。下列叙述正确的是( )
A.原子半径:Y<Z<W
B.Z在化合物中呈+1价
C.Y与W可形成离子化合物
D.W的单质能在Y的单质中燃烧生成WY3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+3B(g)![]() 2C(g)+2D(g),在四种不同情况下用不同物质表示的反应速率分别如下,其中反应速率最大的是( )
2C(g)+2D(g),在四种不同情况下用不同物质表示的反应速率分别如下,其中反应速率最大的是( )
A. v(A)=0.15mol/(Lmin)
B. v(B)=0.04mol/(Ls)
C. v(C)=0.03mol/(Ls)
D. v(D)=0.4mol/(Lmin)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将100mL稀硝酸和稀硫酸的混合酸溶液平均分成两份。向其中一份中逐渐加入铜粉最多能溶解9.6g(假设此时硝酸只被还原为NO,下同);向另一份中逐渐加入铁粉,产生气体的量随铁粉质量的变化如图所示。则下列判断中错误的是( )
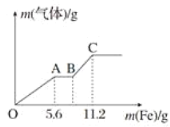
A.原混合酸溶液中H2SO4的浓度为2.0molL-1B.A点对应消耗NO3-物质的量为0.1mol
C.B点对应消耗铁粉的质量为8.4gD.OA段产生的气体是NO,BC段产生的气体是H2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com