
| 电离能/(kJ·mol-1) | I1 | I2 | I3 | I4 |
| A | 932 | 1 821 | 15 390 | 21 771 |
| B | 738 | 1 451 | 7 733 | 10 540 |
 ,每个COCl2分子内含有________个σ键,________个π键,其中心原子采取________杂化轨道方式。
,每个COCl2分子内含有________个σ键,________个π键,其中心原子采取________杂化轨道方式。

 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:高中化学 来源:不详 题型:填空题
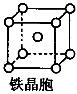
 3Na2O+2Fe+9N2↑。
3Na2O+2Fe+9N2↑。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 离能(kJ·mol-1) | I1 | I2 | I3 | I4 |
| A | 932 | 1 821 | 15 390 | 21 771 |
| B | 738 | 1 451 | 7 733 | 10 540 |
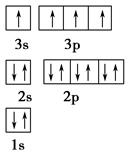
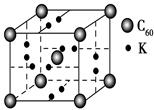
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.离子键 | B.共价键 | C.金属键 | D.配位键 E.氢键 F. 键 键 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
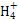 立体构型是 ,其中心原子的杂化方式为 。
立体构型是 ,其中心原子的杂化方式为 。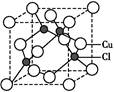
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 ”表示相关元素的原子中除去最外层电子的剩余部分,“
”表示相关元素的原子中除去最外层电子的剩余部分,“ ”表示氢原子,小黑点“
”表示氢原子,小黑点“ ”表示没有形成共价键的最外层电子,短线表示共价键。
”表示没有形成共价键的最外层电子,短线表示共价键。
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 4NaCl+O2;2CaO+2Cl2
4NaCl+O2;2CaO+2Cl2 2CaCl2+O2;SiO2+2CCl4
2CaCl2+O2;SiO2+2CCl4 SiCl4+2COCl2;Cr2O3+3CCl4
SiCl4+2COCl2;Cr2O3+3CCl4 2CrCl3+3COCl2。
2CrCl3+3COCl2。
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素 | 性质或结构信息 |
| A | 单质常温下为固体,难溶于水易于溶CS2。能形成2种二元含氧酸。 |
| B | 原子的M层有1个未成对的p电子。核外p电子总数大于7。 |
| C | 单质曾被称为“银色的金子”。与锂形成的合金常用于航天飞行器。单质能溶强酸和强碱。 |
| D | 原子核外电子层上s电子总数比p电子总数少2个。单质和氧化物均为空间网状晶体,具有很高的熔、沸点。 |
| E | 其氧化物是汽车尾气的主要有害成分之一,也是空气质量预报的指标之一;该元素在三聚氰胺中含量较高。 |
| F | 周期表中电负性最大的元素 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com