
| ��� | ʵ����� | ʵ��۲죨��Ҫ���� | ���ӷ���ʽ | ��������� |
| �� | �������е� ��ϡ���� | �����ܽ⣬��Һ���� ɫ���dz��ɫ������ ɫ��ζ�ĵ��������� | Fe +2H��= H2��+ Fe2�� | Fe���л�ԭ�� |
| �� | �Ȼ�������Һ�е���KSCN��Һ���ټ�����ˮ | ����KSCN��Һ���� �Ա仯��������ˮ�� �����Ѫ��ɫ | | |
| �� | �Ȼ�������Һ�� ��пƬ | | Fe2��+ Zn =" Fe" + Zn 2+�� | |
| �� | | | | Fe3������������ |


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
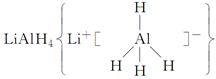 ��LiH���ǽ���������������л��ϳ��еij����Լ�����ˮ���ܾ��ҷ�Ӧ�ų�H2��LiAlH4��125 ��ֽ�ΪLiH��H2��Al������˵���в���ȷ���� (����)��
��LiH���ǽ���������������л��ϳ��еij����Լ�����ˮ���ܾ��ҷ�Ӧ�ų�H2��LiAlH4��125 ��ֽ�ΪLiH��H2��Al������˵���в���ȷ���� (����)��| A��LiH��D2O��Ӧ������������Ħ������Ϊ4 g��mol��1 |
| B��1 mol LiAlH4��125 ����ȫ�ֽ⣬ת��3 mol���� |
| C��LiAlH4��������ˮ����ɫ��Һ����ѧ����ʽ�ɱ�ʾΪLiAlH4��2H2O=LiAlO2��4H2�� |
| D��LiAlH4����ȩ���������Ҵ���LiAlH4����ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��������Ӧ�Ƿ��ȷ�Ӧ |
| B��������ɫ������ԭ�������ɵ�P2O5��ɫ����С�������̣���ˮ�Ժ�ǿ�����տ����е�ˮ�֣���������СҺ�Σ����� |
| C���÷�Ӧ�������뻹ԭ�����ʵ���֮��Ϊ6:5 |
| D��������Ӧ������3molPʱ��ת�Ƶ��ӵ����ʵ���Ϊ15mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��PbO2Ϊ��ԭ�������л�ԭ�� |
| B�����������뻹ԭ��������ʵ���֮��Ϊ5:2 |
| C������1 mol��Pb2+��ת�Ƶĵ�����Ϊ 5 mol |
| D�����Ի�����PbO2 ��������ǿ�ڵ�MnO4�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 ��������
�������� �ں���3molNaHSO3����Һ����μ���KIO3��Һ������KIO3������I2�����ʵ����Ĺ�ϵ��ͼ��ʾ��������˵���������( )
�ں���3molNaHSO3����Һ����μ���KIO3��Һ������KIO3������I2�����ʵ����Ĺ�ϵ��ͼ��ʾ��������˵���������( )
| A��a��ʱNaHSO3���� |
| B��b��ʱ��ԭ����Ϊ������ |
| C��b�㵽c�㣬KIO3��NaHSO3��Ӧ���ɵ��ʵ� |
| D�������KIO3Ϊ0.4mol��1.12molʱ����Ӧ����Һ�е����Ӿ�Ϊ0.4mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Fe2+��S2O32�����ǻ�ԭ�� |
| B��x=6 |
| C��1mol Fe2+������ʱ����Fe2+��ԭ��O2�����ʵ���Ϊ1/3mol |
| D��ÿ����1mol Fe3O4����Ӧת�Ƶĵ�������Ϊ3mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���٢� | B���ڢ� | C���ۢ� | D���٢� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��MnO4-��H+����������Fe2+�ǻ�ԭ�� |
| B��H2O���������������ǻ�ԭ���� |
| C��ÿ����1molˮ��ת��1.2 mol�ĵ��� |
| D��Fe2+�Ļ�ԭ��ǿ��Mn2+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 N2O��+2H2O
N2O��+2H2O K2MnO4+MnO2+O2 �� ��S+2KNO3+3C
K2MnO4+MnO2+O2 �� ��S+2KNO3+3C K2S+N2��+3CO2��
K2S+N2��+3CO2�� Hg+SO2
Hg+SO2| A��NH4NO3��N2+O2+H2O | B��NH4NO3��NH3+HNO3 |
| C��NH4NO3��O2+HNO3+H2O | D��NH4NO3��N2+HNO3+H2O |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com