
【题目】将一定量铜与足量浓硝酸充分反应,可以得到6.72L NO2气体(气体体积在标准状况下测定)。
(1)若反应后溶液体积为100mL,则所得溶液中Cu2+的物质的量浓度是多少?
(2)若改用排水法收集气体,则可收集到气体的体积为多少?
科目:高中化学 来源: 题型:
【题目】在A、B、C三个烧杯中分别盛有相同浓度的稀硫酸,如图所示:
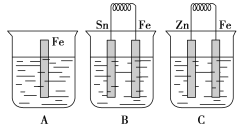
(1)A中反应的离子方程式为_____________________________。
(2)B中Sn极的电极反应式为____________________________,Sn极附近溶液的pH________(填“增大”、“减小”或“不变”)。C中被腐蚀的金属是________,总反应的离子方程式为________________,比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分析离子反应 xR2++yH++O2═mR3++nH2O,下列说法中正确的是( )
A.n=2,H2O是氧化产物
B.x=y=m=4
C.该反应中R2+得到电子,被氧化为R3+
D.任何氧化还原反应中氧化剂失电子总数都等于还原剂得电子总数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】非金属单质A经下图所示的过程转化为含氧酸D,已知D为强酸,请回答下列问题:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体。
①D的化学式是________;
②在工业生产中,大量排放的B气体被雨水吸收后形成了________而污染环境。
(2)若A在常温下为气体,C是红棕色气体。
①A、C的化学式分别是:A________;C________。
②D的稀溶液在常温下可与铜反应并生成B气体,请写出该反应的化学方程式______________,该反应中还原剂和氧化剂之比为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 反应AlCl3+4NaOH===NaAlO2+3NaCl+2H2O,可以设计成原电池
B. Zn和稀硫酸反应时,加入少量CuSO4溶液能加快产生H2的速率
C. 把Fe片和Cu片放入稀硫酸中,并用导线把二者相连,观察到Cu片上产生大量气泡,说明Cu与H2SO4能发生反应而Fe被钝化
D. Zn-Cu原电池工作过程中,溶液中H+向负极作定向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g) + O2(g)![]() 2SO3(g) ΔH = a kJ·mol-1,反应能量变化如图所示。下列说法中,不正确的是
2SO3(g) ΔH = a kJ·mol-1,反应能量变化如图所示。下列说法中,不正确的是

A.a<0
B.过程II可能使用了催化剂
C.使用催化剂可以提高SO2的平衡转化率
D.反应物断键吸收能量之和小于生成物成键释放能量之和
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 下列有关电解质的说法中,不正确的是( )
A. 25℃时,任何水溶液中的Kw=1.0×10-14
B. 在0.1 mol·L-1的醋酸溶液中加入少量冰醋酸,电离平衡正向移动,醋酸的电离程度增大
C. 将pH=2的盐酸稀释10倍,所得溶液的pH=3
D. 25℃时,pH=12的氨水中,OH-的物质的量浓度为0.010 mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com