
【题目】根据原子结构、元素周期表和元素周期律的知识回答下列问题:
(1)A元素次外层电子数是最外层电子数的![]() ,其外围电子轨道表示式是__。
,其外围电子轨道表示式是__。
(2)B是1~36号元素原子核外电子排布中未成对电子数最多的元素,B元素的名称是__,在元素周期表中的位置是__,位于周期表___区,写出基态B原子的核外电子排布式___。
(3)C、N、O、F四种元素第一电离能由大到小的顺序为___,电负性由大到小的顺序为___。
(4)基态Fe2+核外电子排布式为__,Sm的价层电子排布式为4f66s2,Sm3+的价层电子排布式为__。
(5)根据元素As在周期表中的位置预测As的氢化物分子的空间构型为__,其沸点比NH3的__(填“高”或“低”),其判断理由是__。
【答案】![]() 铬 第四周期第ⅥB族 d 1s22s22p63s23p63d54s1或[Ar]3d54s1 F>N>O>C F>O>N>C 1s22s22p63s23p63d6 或[Ar]3d6 4f5 三角锥形 低 氨气分子间含有氢键
铬 第四周期第ⅥB族 d 1s22s22p63s23p63d54s1或[Ar]3d54s1 F>N>O>C F>O>N>C 1s22s22p63s23p63d6 或[Ar]3d6 4f5 三角锥形 低 氨气分子间含有氢键
【解析】
(1)A元素次外层电子数是最外层电子数的![]() ,A元素只能是Ne,则其外围电子轨道表示式是
,A元素只能是Ne,则其外围电子轨道表示式是![]() ,故答案为
,故答案为![]() ;
;
(2) B是1~36号元素原子核外电子排布中未成对电子数最多的元素,B元素是铬,其名称是24号元素铬,在元素周期表中的位置是第四周期第ⅥB族,位于周期表d区,基态Cr原子的核外电子排布式为1s22s22p63s23p63d54s1或[Ar]3d54s1,故答案为:铬;第四周期第ⅥB族;d;1s22s22p63s23p63d54s1或[Ar]3d54s1;
(3) C、N、O、F四种元素中,原子半径r(C)> r(N) >r(O) >r(F),而N原子核外处于2p3半充满状态,更稳定,所以第一电离能F>N>O>C,电负性F>O>N>C,故答案为:F>N>O>C;F>O>N>C;
(4) Fe是26号元素,核外有26个电子,失去两个电子得到Fe2+,基态Fe2+核外电子排布式为1s22s22p63s23p63d6 或[Ar]3d6,Sm的价层电子排布式为4f66s2,失去三个电子得到Sm3+,Sm3+的价层电子排布式为4f5,故答案为:1s22s22p63s23p63d6 或[Ar]3d6;4f5;
(5) As的氢化物分子AsH3与NH3为同一主族的氢化物,结构相似,故AsH3的空间构型为三角锥形,因为NH3分子间含有氢键,所以AsH3的沸点低于氨气,故答案为:三角锥形;低;氨气分子间含有氢键。


科目:高中化学 来源: 题型:
【题目】原子核外p能级、d能级等原子轨道上电子排布为“全空”“半满”“全满”的时候一般更加稳定,称为洪特规则的特例。下列事实不能作为这个规则的证据的是( )
A.硼元素的第一电离能小于铍元素的第一电离能
B.磷元素的第一电离能大于硫元素的第一电离能
C.基态铜原子的核外电子排布式为![]() 而不是
而不是![]()
D.某种激发态碳原子的核外电子排布式为![]() 而不是
而不是![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数依次增大,X的原子半径是所有短周期主族元素中最大的,W的核外电子数与X、Z的最外层电子数之和相等,Y的原子序数是Z的最外层电子数的2倍,由W、X、Y三种元素形成的化合物M的结构如图所示。下列叙述正确的是( )
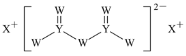
A.元素非金属性强弱的顺序为W>Y>Z
B.Y单质的熔点高于X单质
C.W分别与X、Y、Z形成的二元化合物均只有一种
D.化合物M中W不都满足8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废弃物的综合利用既有利于节约资源,又有利于保护环境。某工厂对工业污泥中Cr(III)回收与再利用工艺流程如图(硫酸浸取液中金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+、Mg2+):
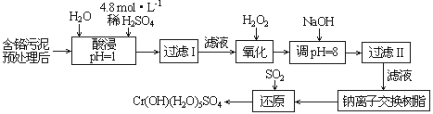
已知:常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH(开始沉淀的pH按金属阳离子浓度为1.0mol·L-1计算)和完全沉淀时溶液的pH,见下表:
阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cu2+ | Cr3+ |
开始沉淀时的pH | 1.9 | 7.5 | —— | —— | 4.7 | —— |
沉淀完全时的pH | 3.2 | 9.7 | 11.1 | 8 | 6.7 | 9(>9溶解) |
重铬酸根离子(Cr2O72-)在溶液中存在如下平衡:2CrO42-+2H+![]() Cr2O72-+H2O
Cr2O72-+H2O
(1)该工厂对工业污泥中Cr(+3价)回收与再利用工艺流程中,其中一步存在氢氧化铁的沉淀溶解平衡:Fe(OH)3(s)![]() Fe3+(aq)+3OH-(aq),其溶度积常数表达式为Ksp=__。
Fe3+(aq)+3OH-(aq),其溶度积常数表达式为Ksp=__。
(2)酸浸时,为了提高浸取率可采取的措施是__(至少答一点)。
(3)加入H2O2的作用是__。调节溶液的pH=8是为了除去__离子。
(4)钠离子交换树脂的原理为:Mn++nNaR→MRn+nNa+,被交换的的杂质离子是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A.ns电子的能量可能低于(n-1)p电子的能量
B.6C的电子排布式1s22s22p![]() ,违反了洪特规则
,违反了洪特规则
C.电子排布式(21Sc)1s22s22p63s23p63d3违反了能量最低原理
D.电子排布式(22Ti)1s22s22p63s23p10违反了泡利不相容原理
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化钠主要用于皮革、毛纺、高档纸张、染料等行业。生产硫化钠大多采用无水芒硝(Na2SO4)—炭粉还原法,其流程示意图如下:

(1)若煅烧所得气体为等物质的量的CO和CO2,写出煅烧时发生的总的化学反应方程式为____。
(2)上述流程中采用稀碱液比用热水更好,理由是___________。
(3)常温下,取硫化钠晶体(含少量NaOH)加入到硫酸铜溶液中,充分搅拌。若反应后测得溶液的pH=4,则此时溶液中c( S2-)=___mol·L-1。
(已知:常温时CuS、Cu(OH)2的Ksp分别为8.8×10-36、2.2×10-20)
(4)①皮革工业废水中的汞常用硫化钠除去,汞的去除率与溶液的pH和x(x代表硫化钠的实际用量与理论用量的比值)有关(如图所示)。为使除汞效果最佳,应控制的条件是:x=___,pH控制在___范围。

②某毛纺厂废水中含0.001 mol·L-1的硫化钠,与纸张漂白后的废水(含0.002 mol·L-1NaClO)按1:2的体积比混合,能同时较好处理两种废水,处理后的废水中所含的主要阴离子有_____。
(5)常温下利用Fe2+、Fe3+的相互转化,可将SO2转化为SO42-而实现SO2的处理(总反应为2SO2+O2+2H2O=2H2SO4)。已知,含SO2的废气通入含Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2+ + O2+ 4H+ =4Fe3+ + 2H2O,则另一反应的离子方程式为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法正确的是
A.![]() 的同分异构体中含有苯环且属于羧酸的有14种
的同分异构体中含有苯环且属于羧酸的有14种
B.葡萄糖与果糖、淀粉与纤维素均互为同分异构体
C.2,2-二甲基丙烷可以由烯烃通过加成反应制得
D.汽油、柴油、植物油都是碳氢化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】美托洛尔可用于治疗各类型高血压及心绞痛,其一种合成路线如下:

已知:①CH3COCH2R![]() CH3CH2CH2R
CH3CH2CH2R
② B- F苯环上均只有两个取代基
回答下列问题:
(1)A的化学名称是___,C中含氧官能团的名称是___
(2)E→F的反应类型是___,G的分子式为___。
(3)D的结构简式为___。
(4)反应B→C的化学方程式为___
(5)芳香族化合物W是G的同分异构体,W能发生水解反应,核磁共振氢谱有4组峰,峰面积之比为9:3:2:2,写出一种符合要求的W的结构简式:___.
(6)4一苄基苯酚(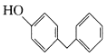 )是一种药物中间体,请设计以苯甲醇和苯酚为原料制备4-苄基苯酚的合成路线:______(无机试剂任用)。
)是一种药物中间体,请设计以苯甲醇和苯酚为原料制备4-苄基苯酚的合成路线:______(无机试剂任用)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有人设想合成具有以下结构的四种烃分子,下列有关说法不正确的是( )

A. 1 mol甲分子内含有10 mol共价键
B. 由乙分子构成的物质不能发生氧化反应
C. 丙分子的二氯取代产物只有三种
D. 分子丁是不可能合成的
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com