
【题目】在通常条件下,NO2和SO2可以很容易发生反应生成NO和SO3 . 现将碳跟浓硫酸共热产生的气体X和碳跟浓硝酸共热产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是( ) 
A.洗气瓶中产生的沉淀是碳酸钡
B.洗气瓶中产生的沉淀是硫酸钡
C.在Z导管出来的气体中无二氧化碳
D.反应一段时间后洗气瓶中溶液的酸性减弱
 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:
【题目】某学生应用如图所示意的方法研究物质的性质,其中,气体A的主要成分是氯气,杂质是空气和水蒸气.请回答下列问题:
(1)该项研究(实验)的主要目的是
(2)浓硫酸的作用是 .
(3)从物质性质的方面来看,这样的实验设计还存在事故隐患,事故表现是 . 则要克服该事故隐患应在上图的D处连接的装置是(填序号).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含有重金属离子的废水直接排入水体,会导致水生动物中毒,毒性的表现与离子浓度和染毒时间正相关。为了验证铅离子对鲫鱼肝胰脏细胞内过氧化氢酶活性的影响,请根据以下提供的材料和用具,完善实验思路,预测实验结果并进行分析。
材料与用具:鲫鱼、铅染毒溶液、匀浆器、试管、H2O2磷酸缓冲液等。
(要求和说明:H2O2磷酸缓冲液由H2O2和磷酸缓冲液组成,其中的H2O2含量可用光电比色法测定,具体检测过程不要求写出)
请回答:
(1)实验思路:
①染毒饲养:取3个水族箱,分别加入等量铅浓度为0、20、40mg/L的铅染毒溶液,每个水族箱饲养20尾鲫鱼。
②制备酶液:染毒开始时及过程中每隔24小时,每组捕捉4尾鲫鱼,取每尾鱼的肝胰脏 0.5g打成匀浆,并制备成酶提取液。
③测酶活性:取试管加入 和 ,反应3分钟立即测定试管中的 。
④ 。
(2)预测实验结果:(在坐标系中用柱状图表示第1次、第5次的实验结果)

(3)分析与讨论:
① 下列关于将肝胰脏制备成酶提取液的叙述错误的是 。
A.将肝胰脏打成匀浆有利于提取酶
B.应该将0.5g克肝胰脏制备成等体积的酶液
C.提取的酶液应该加入磷酸缓冲液并低温保存
D.直接使用匀浆进行实验对实验结果没有影响
② 将H2O2配制成H2O2磷酸缓冲液是为了保证反应过程中的 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,下列描述不正确的是( )
A.C的成分是气体E与二氧化碳的混和气体
B.浓热的D溶液能把碳单质氧化为二氧化碳
C.气体E遇空气会被氧化成红棕色的气体
D.溶液G是蓝色的硫酸铜溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有四种短周期元素,它们的结构、性质等信息如下表所述:
元素 | 结构、性质等信息 |
A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂 |
B | B与A同周期,其最高价氧化物的水化物呈两性 |
C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
请根据表中信息填写:
(1)A原子的核外电子排布式为 .
(2)B元素在周期表中的位置为;离子半径:BA(填“大于”或“小于”).
(3)C原子的电子排布图是 , 其原子核外有个未成对电子,能量最高的电子为轨道上的电子,其轨道呈形.
(4)D原子的电子排布式为 , D﹣的结构示意图是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由1分子的磷酸、碱基m和化合物a构成了化合物b,如下图所示。下列相关叙述中正确的是
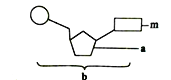
A. 若m为胸腺嘧啶,则b肯定为脱氧核糖
B. 若b为组成核糖体的成分,则b只有4种
C. 若ATP水解可形成b,则a为核糖核苷酸
D. 若a为核糖,则a和磷酸交替排列构成了DNA的基本骨架
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有前四周期原子序数依次递增的五种元素A、B、C、D、E. A、D元素基态原子中成对电子数是未成对电子数的3倍,且D元素基态原子中有6个未成对电子;B的基态原子核外只有7个原子轨道填充了电子,B、C元素基态原子的3p能级上均有1个未成对电子;E元素排在周期表的15列.
(1)B元素基态原子核外电子有种运动状态,电子占据的最高能层符号为 , 该能层具有的原子轨道数为、电子数为 .
(2)C、E两元素可以形成化合物EC3 , 此化合物的VSEPR模型为 , 是分子(填“极性”、“非极性”).
(3)写出D基态原子的外围电子排布图 .
(4)B、C两元素也可以形成共价化合物BC3 , 但BC3经常以二聚(B2C6)的形式存在,二聚分子具有配位键,分子中原子间成键的关系如图所示.请将图中,你认为是配位键的斜线上加上箭头. 
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com