
【题目】在容积为2 L密闭容器中,保持体系内温度800℃不变,将一定量的NO和O2混合发生反应:2NO+O2![]() 2NO2。其中NO的物质的量[n(NO)]随时间的变化如下表:
2NO2。其中NO的物质的量[n(NO)]随时间的变化如下表:
时间/s | 0 | 10 | 20 | 30 | 40 | 50 |
n(NO)/mol | 0.2 | 0.1 | 0.08 | 0.07 | 0.07 | 0.07 |
请回答下列问题:
(1)用O2表示达到平衡(假设30 s刚刚达到平衡)时反应速率________,0~10 s与10~20 s的反应速率之比为________。
(2)根据上述数据,能否计算800℃时该反应的平衡常数K________,“能”则计算K,“否”则说明缺少的数据:________。
(3)若升高反应体系的温度,使反应重新达到平衡,此时体系中n(NO)=n(NO2),则该反应是________热反应(选填“吸”或“放”)。
(4)在800 ℃时,若缩小容器的体积,达新平衡时n(NO)________(选填“>”、“=”或“<”)0.07 mol,NO的转化率________(选填“增大”、“不变”或“减小”)。
【答案】0.001 1 mol/(L·s) 5∶1 否 因为缺少初始氧气物质的量(或浓度) 放 < 增大
【解析】
本小题考查的是化学反应速率的计算、平衡常数、平衡移动。
(1)30s达到平衡,NO的物质的量减少0.2mol-0.07mol=0.13mol,v(NO)= ![]() ;反应速率之比等于化学计量数之比,则v(O2)=0.0022mol/(L·s)×1/2=0.0011 mol/(L·s),相同时间段内,体积相同的容器,则物质的量的变化量之比等于反应速率之比,可知0~10 s与10~20 s的反应速率之比为(0.2-0.1):(0.1-0.08)=5:1;
;反应速率之比等于化学计量数之比,则v(O2)=0.0022mol/(L·s)×1/2=0.0011 mol/(L·s),相同时间段内,体积相同的容器,则物质的量的变化量之比等于反应速率之比,可知0~10 s与10~20 s的反应速率之比为(0.2-0.1):(0.1-0.08)=5:1;
(2)缺少加入的氧气的量,不能确定平衡时体系中氧气的浓度,故不能计算该反应的平衡常数;
(3)根据氮原子守恒,当体系中n(NO)=n(NO2)=0.1mol,升高温度,NO的量增加,说明平衡向逆反应方向移动,说明正反应为放热反应;
(4)在800 ℃时,若缩小容器的体积,压强增大,平衡向正反应方向移动,NO的转化率增大,新平衡时n(NO)小于0.07 mol。据此解答。
(1)30s达到平衡,NO的物质的量减少0.2mol-0.07mol=0.13mol,v(NO)= ![]() ;反应速率之比等于化学计量数之比,则v(O2)=0.0022mol/(L·s)×1/2=0.0011 mol/(L·s),相同时间段内,体积相同的容器,则物质的量的变化量之比等于反应速率之比,可知0~10 s与10~20 s的反应速率之比为(0.2-0.1):(0.1-0.08)=5:1。本小题答案为:0.001 1 mol/(L·s); 5∶1。
;反应速率之比等于化学计量数之比,则v(O2)=0.0022mol/(L·s)×1/2=0.0011 mol/(L·s),相同时间段内,体积相同的容器,则物质的量的变化量之比等于反应速率之比,可知0~10 s与10~20 s的反应速率之比为(0.2-0.1):(0.1-0.08)=5:1。本小题答案为:0.001 1 mol/(L·s); 5∶1。
(2)缺少加入的氧气的量,不能确定平衡时体系中氧气的浓度,故不能计算该反应的平衡常数。本小题答案为:否;因为缺少初始氧气物质的量(或浓度)。
(3)根据氮原子守恒,当体系中n(NO)=n(NO2)=0.1mol,升高温度,NO的量增加,说明平衡向逆反应方向移动,说明正反应为放热反应。本小题答案为:放。
(4)在800 ℃时,若缩小容器的体积,压强增大,平衡向正反应方向移动,NO的转化率增大,新平衡时n(NO)小于0.07 mol。本小题答案为:<;增大。


科目:高中化学 来源: 题型:
【题目】现有五种可溶性物质A、B、C、D、E,它们所含的阴、阳离子互不相同,分别含有五种阳离子Al3+、Fe3+、Cu2+、Ba2+、K+和五种阴离子NO![]() 、OH-、Cl-、CO32—、Xn-(n=1或2)中的一种。
、OH-、Cl-、CO32—、Xn-(n=1或2)中的一种。
(1)某同学通过比较分析,认为无须检验就可判断其中必有的两种物质是____和______。
(2)物质C中含有离子Xn-。为了确定Xn-,现将(1)中的两种物质记为A和B,当C与A的溶液混合时产生蓝色沉淀,向该沉淀中滴入足量稀HNO3,沉淀部分溶解,剩余白色固体(无气体生成),则C为___。(填名称)
(3)将38.4g Cu投入装有足量D溶液的试管中,Cu不溶解,再滴加稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现,则物质D为_________(化学式),写出Cu溶解的离子方程式_______,若要将Cu完全溶解,至少加入H2SO4的物质的量是_________。
(4)足量E溶液与氢碘酸反应时可生成使淀粉变蓝的物质,该反应的化学方程式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,单质A、B、C分别为固体、黄绿色气体、无色气体.在合适反应条件下,它们可以按下面框图进行反应;又知D溶液为黄色,E溶液为无色.请回答:
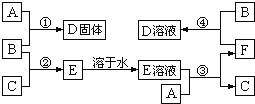
(1)B是_____,F是_____(请填写化学式);
(2)反应③的离子方程式_____;
(3)反应④的离子方程式_____.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向FeCl3溶液中滴加2滴KSCN溶液,发生反应达到平衡Ⅰ。保持温度不变,仅改变某一个条件达到平衡Ⅱ,两次平衡时各物质的浓度如下:
Fe3+(aq)+3SCN-(aq)![]() Fe(SCN)3(aq)
Fe(SCN)3(aq)
平衡Ⅰ/(mol·L-1) a b c
平衡Ⅱ/(mol·L-1) x y z
下列叙述不正确的是( )
A. 存在关系式:c/ab3=z/xy3
B. 存在关系式:(a-x)∶(b-y)∶(z-c)=1∶3∶1
C. 向溶液中加入少量铁粉,溶液颜色变浅
D. 当溶液中c(SCN-)保持不变时达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,不属于四大基本反应类型,但属于氧化还原反应的是
A. 2Na+2H2O===2NaOH+H2↑
B. Cl2+H2O===HCl+HClO
C. CaCO3![]() CaO+CO2↑
CaO+CO2↑
D. Ca(ClO)2+2HCl===CaCl2+2HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常用水钴矿(主要成分为Co2O3,还含少量Fe2O3、 Al2O3、MgO、CaO等杂质) 制备钴的氧化物,其制备工艺流程如下:
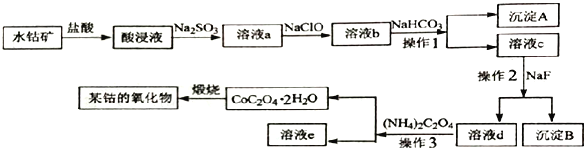
回答下列问题:
(1)在加入盐酸进行“酸浸”时,能提高“酸浸”速率的方法有______________(任写一种)。
(2)“酸浸”后加入Na2SO3,钴的存在形式为Co2+,写出产生Co2+反应的离子方程式_______________________________。
(3)溶液a中加入NaClO的作用为_______________________________。
(4)沉淀A 的成分为__________________。操作2的名称是___________________。
(5)已知: Ksp (CaF2)=5.3×10-9,Ksp(MgF2)=5.2×10-12,若向溶液c 中加入NaF溶液,当Mg2+恰好沉淀完全即溶液中c(Mg2+)=1.0×10-5moI/L,此时溶液中c(Ca2+)最大等于_________mol·L-1。
(6)在空气中煅烧CoC2O4 生成钴的某种氧化物和CO2,测得充分煅烧后固体质量为12.05 g,CO2的体积为6.72 L(标准状况),则此反应的化学方程式为_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生欲配制6.0mol/L的H2SO4 1000 mL,实验室有三种不同浓度的硫酸:
①480mL 0.5mol/L 的硫酸;②150mL 25%的硫酸(ρ=1.18g/mL);③足量的18mol/L的硫酸。有三种规格的容量瓶:250mL、500mL、1000mL。老师要求把①②两种硫酸全部用完,不足的部分由③来补充。
请回答下列问题:
(1)实验所用25%的硫酸的物质的量浓度为______mol/L(保留1位小数)。
(2)配制该硫酸溶液应选用容量瓶的规格为______mL。
(3)配制时,该同学的操作顺序如下,请将操作步骤B、D补充完整。
A.将①②两溶液全部在烧杯中混合均匀;
B.用量筒准确量取所需的18mol/L的浓硫酸____mL,沿玻璃棒倒入上述混合液中。并用玻璃棒搅拌,使其混合均匀;
C.将混合均匀的硫酸沿玻璃棒注入所选的容量瓶中;
D._________________________________________________________________________________________________________________________________
E.振荡,继续向容量瓶中加水,直到液面接近刻度线1~2cm处;
F.改用胶头滴管加水,使溶液的凹液面恰好与刻度线相切;
G.将容量瓶盖紧,振荡,摇匀。
(4)如果省略操作D,对所配溶液浓度有何影响?________(填“偏大”、“偏小”或“无影响”)。
(5)进行操作C前还需注意____________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数用NA表示,气体摩尔体积用Vm表示,物质的质量用m表示,请回答下列问题:
(1)n=![]() =
=![]() =
=![]() ,①②③处分别补充为___、___、___。
,①②③处分别补充为___、___、___。
(2)一个铜原子的质量为m’g,铜的相对原子质量为M’,则阿伏加德罗常数NA=___mol-1。(列出表达式,下同)
(3)常温下20滴水约为1mL,水的密度为1g·mL-1,每滴水中约含a个水分子,则阿伏加德罗常数NA=___mol-1。
(4)bgH2中含N个氢分子,则阿伏加德罗常数NA=___mol-1。
(5)在标准状况下,VLO2中含有N个氧原子,则阿伏加德罗常数NA=___mol-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列试剂的保存或使用正确的是( )
A.漂白粉比氯水稳定,可露置在空气中
B.实验室的氯水需要保存在棕色试剂瓶中
C.用饱和Na2CO3溶液除去CO2中含有的少量HCl
D.金属钠可保存在煤油、四氯化碳(密度大于水)等有机溶剂中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com