
【题目】新型锂离子电池在新能源的开发中占有重要地位,可用作节能环保电动汽车的动力电池。 磷酸亚铁锂(LiFePO4)是新型锂离子电池的首选电极材料,它的制备方法如下:
【方法一】 将一定浓度的磷酸二氢铵、氯化锂混合溶液作为电解液,以铁棒为阳极,石墨为阴极,电解析出磷酸亚铁锂沉淀。沉淀经过滤、洗涤、干燥,在800℃左右、惰性气体氛围中煅烧制得晶态磷酸亚铁锂。
【方法二】 将碳酸锂、乙酸亚铁[(CH3COO)2Fe]、磷酸二氢铵按一定比例混合、充分研磨后,在800℃左右、惰性气体氛围中煅烧制得晶态磷酸亚铁锂,同时生成的乙酸及其他产物均以气体逸出。
【方法三】 以铁红、锂辉石LiAl (SiO3)2 (含少量Ca2+、Mg2+的盐)、碳粉等原料来生产磷酸亚铁锂。其主要工艺流程如下:
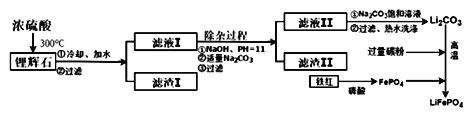
己知: 2LiAl (SiO3) 2+ H2SO4(浓)=Li2SO4+ Al2O3·4SiO2·H2O↓
溶解度/℃ | 20 | 40 | 60 | 80 |
溶解度(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
溶解度(Li2SO4) /g | 34.2 | 32.8 | 31.9 | 30.5 |
(1) 在方法一中,阳极生成磷酸亚铁锂的电极反应式为______________________________。
(2)在方法二中,除生成磷酸亚铁锂、乙酸外,还有H2O、________(填化学式)生成。
(3)方法一与方法二中,制备磷酸亚铁锂的过程都必须在惰性气体氛围中进行。其原因是________________。
(4)在方法三中从滤渣I中可分离出Al2O3,如下图所示。请写出生成沉淀的离子方程式________________。
![]()
(5)向滤液II中加入饱和Na2CO3溶液,过滤后,用“热水洗涤”的原因是___________________________。(6) 写出在高温下生成磷酸亚铁锂的化学方程式______________________________________。
(7)磷酸铁锂锋动力电池(简称LFP) 是一种高效、超长寿命的二次电池。其工作原理为:
C6Li+FePO4![]() C6Li(1-x)+ (1-x) FePO4+xLiFePO4充电时,写出阴极反应方程式____________________。
C6Li(1-x)+ (1-x) FePO4+xLiFePO4充电时,写出阴极反应方程式____________________。
【答案】 Fe+H2PO4-+Li+-2e-=LiFePO4+2H+ CO2、NH3 为了防止亚铁化合物被氧化 Al3++3NH3·H2O=Al(OH)3↓+3NH4+ Li2CO3的溶解度随温度升高而减小,热水洗涤可减少Li2CO3的损失 2FePO4+ Li2CO3+2C![]() 2LiFePO4+3CO↑ C6Li(1-x)+xLi++xe-═C6Li
2LiFePO4+3CO↑ C6Li(1-x)+xLi++xe-═C6Li
【解析】试题分析:(1)阳极铁失电子生成磷酸亚铁锂;(2)根据元素守恒分析产物;(3).亚铁离子易被氧化;(4)含有Al3+的溶液加入氨水可以生成氢氧化铝沉淀;(5)Li2CO3的溶解度随温度升高而减小;(6)Li2CO3、C、FePO4高温条件下生成LiFePO4和CO;(7)放电时的负极,充电时做阴极;
解析:(1)阳极铁失电子生成磷酸亚铁锂,电极反应式是Fe+H2PO4-+Li+-2e-=LiFePO4+2H+;(2)将碳酸锂、乙酸亚铁[(CH3COO)2Fe]、磷酸二氢铵按一定比例混合、充分研磨后,在800℃左右、惰性气体氛围中煅烧制得晶态磷酸亚铁锂,根据元素守恒可知,同时生成的乙酸、H2O、CO2、NH3等气态物质;(3).亚铁离子易被氧化,为了防止亚铁化合物被氧化,所以方法一与方法二中,制备磷酸亚铁锂的过程都必须在惰性气体氛围中进行;(4)含有Al3+的溶液加入氨水可以生成氢氧化铝沉淀,反应离子方程式是Al3++3NH3·H2O=Al(OH)3↓+3NH4+;(5) 向滤液II中加入饱和Na2CO3溶液生成Li2CO3沉淀,Li2CO3的溶解度随温度升高而减小,热水洗涤可减少Li2CO3的损失;(6)Li2CO3、C、FePO4高温条件下生成LiFePO4和CO,反应方程式是2FePO4+ Li2CO3+2C![]() 2LiFePO4+3CO↑;(7)放电时的负极,充电时做阴极,阴极发生还原反应,电极反应式是C6Li(1-x)+xLi++xe-═C6Li;
2LiFePO4+3CO↑;(7)放电时的负极,充电时做阴极,阴极发生还原反应,电极反应式是C6Li(1-x)+xLi++xe-═C6Li;


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分。表中所列的字母分别代表某一种化学元素。

下列说法正确的是( )
A. 沸点 A2D<A2X
B. CA3 分子是非极性分子
C. B、C、D 形成的气态氢化物互为等电子体
D. C 形成的常见单质中 σ 键与 π 键个数之比为 1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中不正确的是
A. C60与石墨是同素异形体 B. H(氕)、D(氘)、T(氚)互为同位素
C. 甲烷和戊烷是同系物 D. 异丁烷与丁烷是同一种物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学按下图进行实验,在A中放的是干燥的红色纸条,B中放的是湿润的红色纸条,C中盛放的是氢氧化钠溶液。请回答下列问题。
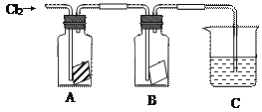
(1)通入Cl2一段时间后,A、B装置中,红色纸条的现象和结论为:
装置 | 现象 | 结论 |
A | ______________ | 潮湿的氯气______(填能或不能)使红色纸条褪色,因为反应生成的____________具有漂白性 |
B | ______________ |
(2)C装置的作用是__________________________
写出装置C中反应的化学方程式:_________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家模拟足贝类足丝蛋白的功能,合成了一种对云母、玻璃、二氧化硅等材料具有良好粘附性的物质一化合物I,其合成路线如下:
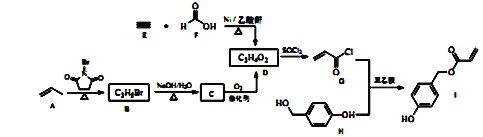
回答下列问题:
(1)A的化学名称为_____________________。
(2)由B生成C的化学方程式为_____________________________。
(3)由E和F反应生成D的反应类型为__________,由G和H反应生成I的反应类型为___________。
(4)D的结构筒式为____________,仅以D为单体合成高分子化合物的化学方程式为___________________。
(5)X是I的同分异构体,能发生银镜反应,能与饱和碳酸氢钠溶液反应放出CO2,其核磁共振氢谱显示有4种不同化学环境的氢,峰面积比为6:2:1:1。写出两种符合要求的X的结构简式_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D四种气体,A是密度最小的气体,B在通常情况下呈黄绿色,把四种气体分别通入酸性硝酸银溶液中,通入B、D气体时立即出现白色沉淀,纯净的A可以在B中安静地燃烧,发出苍白色的火焰并生成D。把无色无刺激气味气体C通入澄清石灰水时变浑浊。
(1)A、B、C、D的分子式分别为:A_______ B________ C_________D_______。
(2)写出下列各反应的化学方程式:
A与B_______________________________________________;
B与水_______________________________________________;
C与澄清石灰水_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学活动小组利用如图装置对电化学进行探究,开始两电极质量相等,下列说法正确的是( )
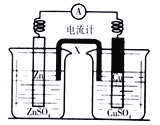
A. 若X为铜片,左池发生吸氧腐蚀作原电池,X在右池的电极反应式为Cu-2e-=Cu2+
B. 若X装载的是足量饱和KCl溶液浸泡的琼脂,当外电路通过0.02mol电子时,两电极的质量差为0.64g
C. 若X装载的是足量饱和KC1洛液浸泡的琼脂,则X中的K+移向左池
D. 若X为锌片,左池为电池的负极区
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表示对应化学反应的离子方程式正确的是 ( )
A. 向稀HNO3中滴加Na2SO3溶液: SO32-+2H+SO2↑+H2O
B. Na2CO3溶液中CO32-的水解:CO32-+H2O==HCO3-+OH-
C. 向Al2(SO4)3溶液中加入过量的NH3·H2O: Al3++4NH3·H2O[Al(OH)4]-+4N![]()
D. 向CuSO4溶液中加Na2O2:2Na2O2+2Cu2++2H2O4Na++2Cu(OH)2↓+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列反应:
①2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
②CaO+H2O=Ca(OH)2
③Ba(OH)2+H2SO4=BaSO4↓+2H2O
④Zn+2HCl=ZnCl2+H2↑
⑤2KClO3![]() 2KCl+3O2↑
2KCl+3O2↑
⑥CaCO3![]() CaO+CO2↑
CaO+CO2↑
⑦2CO+O2![]() 2CO2
2CO2
⑧SO42-+Ba2+=BaSO4↓
(1)既是分解反应又是氧化还原反应的是_____,既是化合反应又是氧化还原反应的是______(均填序号)。
(2)请用单向桥表示反应①的电子转移的方向和数目:________________。其中,该反应的氧化产物是___________,还原产物是__________。
(3)反应③的离子反应方程式为_________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com