
【题目】碱金属在电池、催化剂等领域有着广泛的用途,关于碱金属单质的性质叙述错误的是( )
A. 都是电和热的良导体 B. 从 Li 至 Cs,熔点逐渐降低
C. 都是柔软的银白色金属(铯略带金色) D. 都可以保存在煤油中
科目:高中化学 来源: 题型:
【题目】在一定条件下,将3 mol A和1 mol B两种气体混合于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g) ![]() xC(g)+2D(g)。2 min末该反应达到平衡,测得生成0.8 mol D和0.4 mol C。下列判断不正确的是( )
xC(g)+2D(g)。2 min末该反应达到平衡,测得生成0.8 mol D和0.4 mol C。下列判断不正确的是( )
A. x =1
B. 2 min时,A的浓度为0.9 mol·L-1
C. 2 min内A的反应速率为0.3 mol·L-1·min-1
D. B的转化率为60%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将a mol钠和a mol铝一同投入m g足量水中,所得溶液密度为d g·mL-1,该溶液中溶质质量分数为( )
A. ![]() % B.
% B. 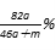 C.
C. ![]() % D.
% D. ![]() %
%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式与所述事实相符且正确的是
A.Ca(HCO3)2溶液中加入少量NaOH溶液:Ca2+ +2HCO3-+2OH-=CaCO3↓+CO32-+H2O
B.磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3-![]() 3Fe3++NO↑+3H2O
3Fe3++NO↑+3H2O
C.向含有0.4 mol FeBr2的溶液中通入0.3 mol Cl2充分反应:4 Fe2++2 Br-+3Cl2=4Fe3++6Cl-+Br2
D.以铜为电极电解饱和食盐水:2Cl-+2H2O![]() Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列化学方程式中,能用离子方程式H+ + OH— = H2O表示的是
A.H2CO3 + 2NaOH = Na2CO3+2H2O
B.HCl + NH3·H2O = NH4Cl + H2O
C.Fe(OH)3 + 3HCl = FeCl3 + 3H2O
D.H2SO4 + 2KOH = K2SO4 + 2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知溶液导电能力取决于自由移动离子的浓度和所带电荷数,离子浓度越大,所带电荷数越多,溶液导电能力越强。现有浓度均为1mol/L的以下电解质溶液:①![]() ②
②![]() ③
③![]() ④
④![]() ⑤
⑤![]() ⑥
⑥![]() ⑦
⑦![]() ⑧
⑧![]() ⑨
⑨![]() ⑩
⑩![]() 请回答相关问题。
请回答相关问题。
(1)这些溶液中导电能力最强的是_______(填溶质化学式),其电离方程式为_______。写出一种导电原理与电解质溶液不同的物质名称 _________。
(2)以上溶液两两混合后溶液的导电能力有多种变化趋势,请写出符合要求的组合(不考虑温度变化,填序号,如①和②)。导电能力变化符合图1的组合是_________(任写一组);导电能力变化符合图2的组合是__________,混合过程中发生反应的离子方程式是_________;①的溶液和_______(任写一种)的溶液混合导电能力变化符合图3且两溶液体积相等时导电能力最弱,溶液导电能力最弱时溶质的物质的量浓度为 ____________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在温度T1和T2时,分别将0.50 mol CH4和1.20 mol NO2充入体积为1 L的密闭容器中,发生如下反应:CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(g),测得n(CH4)随时间变化数据如下表:
N2(g)+CO2(g)+2H2O(g),测得n(CH4)随时间变化数据如下表:
时间/min | 0 | 10 | 20 | 40 | 50 | |
T1 | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
T2 | n(CH4)/mol | 0.50 | 0.30 | 0.18 | …… | 0.15 |
下列说法正确的是( )
A. T1时0~10 min NO2的平均反应速率为0.15 mol·L-1·min -1
B. T2时CH4的平衡转化率为70.0%
C. 保持其他条件不变,T1时向平衡体系中再充入0.30 mol CH4和0.80 mol H2O(g),平衡向正反应方向移动
D. 保持其他条件不变,T1时向平衡体系中再充入0.50 mol CH4和1.20 mol NO2,与原平衡相比,达新平衡时N2的浓度增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com