
【题目】下列关于容量瓶及其使用方法的叙述,正确的是
①是配制一定物质的量的浓度的溶液的专用仪器
②使用前要先检查容量瓶是否漏液 ③容量瓶可以用来加热
④不能用容量瓶贮存配制好的溶液 ⑤可以用400mL容量瓶配制250mL溶液
A. ①和② B. ①和④ C. 除了③ D. 除了③⑤
科目:高中化学 来源: 题型:
【题目】某学生用标准的0.2mol/L的盐酸滴定待测的NaOH溶液,其实验操作如下:A.用碱式滴定管取待测液NaOH溶液放入锥形瓶,滴加2﹣3滴酚酞指示剂.
B.用待测的NaOH溶液润洗碱式滴定管.
C.检查滴定管是否漏水.
D.取下酸式滴定管,用标准的盐酸溶液润洗后,再将标准的盐酸注入酸式滴定管至刻度“0”以上2cm﹣3cm处,把酸式滴定管固定好,调节液面.
E.把滴定管用蒸镏水洗净,并分别固定在滴定管架两边.
F.另取锥形瓶,再重复滴定操作一次.
G.把锥形瓶放在酸式滴定管的下面,瓶下垫一张白纸,然后边滴定边摇动锥形瓶,直至终点,记下滴定管的液面所在刻度.
据上述滴定操作,完成下列填空:
(1)滴定操作的正确操作顺序是(用上述各编号字母填写)→E→→B→→→;
(2)G步操作中判断滴定终点的依据是;
(3)D步骤的操作中液面应调节到 , 尖嘴部分应;
(4)酸式滴定管未用标准的盐酸润洗,待测溶液NaOH的测定值会;碱式滴定管未用待测的NaOH溶液润洗,待测NaOH溶液的测定值会 . (填“偏高”、“偏低”或“无影响”.)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学为了探究沉淀的溶解平衡原理并测定某温度下PbI2的溶度积常数,设计了如下实验:
Ⅰ、取100mL蒸馏水,加入过量的PbI2固体(黄色),搅拌、静置,过滤到洁净的烧杯中,得到滤液a
Ⅱ、取少量滤液a于试管中,向其中加入几滴0.1mol/L的KI溶液,观察现象
Ⅲ、另准确量取10.00mL滤液,与离子交换树脂(RH)发生反应:2RH+Pb2+=R2Pb+2H+ , 交换完成后,流出液用中和滴定法测得n(H+)=3.000×10﹣5mol分析过程,下列说法错误的是( )
A.步骤I中搅拌的目的是使碘化铅充分溶解
B.步骤II中观察到的现象是产生黄色沉淀
C.此实验温度下,PbI2的溶度积常数Ksp=1.350×10﹣8
D.若步骤I 盛装滤液的烧杯中有少量的水,Ksp的测定结果不受影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
Ⅰ.用化学用语回答下列问题:
(1)写出二氧化碳分子的电子式:___________;
(2)写出氮气分子的结构式___________。
(3)A+、Bˉ、C、D 四种粒子(分子或离子),它们都分别含10个电子,已知它们有如下转化关系:A++Bˉ![]() C+D↑,则A+的电子式:_____________;比较C和D的稳定性的强弱:_____________________(用化学式表示)。
C+D↑,则A+的电子式:_____________;比较C和D的稳定性的强弱:_____________________(用化学式表示)。
(4)用电子式表示MgCl2的形成过程__________________________________。
Ⅱ.下列物质:① N2 ② CO2 ③ NH3 ④ Na2O ⑤Na2O2 ⑥ NaOH ⑦ CaBr2 ⑧ H2O2 ⑨ NH4Cl ⑩ Ar。
(1)既含有极性键又含有非极性键的是_______;(填序号,下同)
(2)含有非极性键的离子化合物是_____。
(3)不含化学键的是_____。
Ⅲ.下列变化中:① 干冰气化; ② 硝酸钾熔化; ③ KHSO4熔融; ④ 硫酸溶于水;
⑤ 蔗糖溶于水;⑥ HI分解; ⑦ 碘升华; ⑧ 溴蒸气被木炭吸附。
(1)未破坏化学键的是___________;
(2)仅离子键被破坏的是_________;
(3)仅共价键被破坏的是_________。
Ⅳ.下列物质:① 1H、2H、3H ; ② H2O、D2O、T2O; ③ O2、O3; ④ 14N、14C
(1)互为同位素的是:______;
(2)互为同素异形体的是:______;
(3)氢的三种原子1H、2H、3H 与氯的两种原子35Cl、37Cl相互结合为氯化氢,可得分子中相对分子质量不同的有________种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2CO3(aq)与盐酸反应过程中的能量变化示意图如下,下列选项正确的是
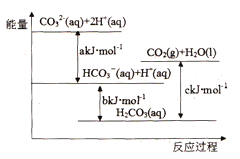
A. H2CO3(aq)=CO2(g)+H2O(l)为放热反应
B. CO32-(aq)+ H+(aq)=HCO3-(aq) △H=akJ/mol
C. HCO3-(aq)+H+(aq)= CO2(g)+H2O(l) △H=(c-b)kJ/mol
D. CO32-(aq)+ 2H+(aq)= CO2(g)+H2O(l) △H=(a+b-c)kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质按酸、碱、盐分类顺序排列正确的是( )
A. 硫酸、烧碱、纯碱B. 硫酸、纯碱、食盐
C. 碳酸、乙醇、高锰酸钾D. 磷酸、熟石灰、生石灰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是实验室进行氨溶于水的喷泉实验装置,下列叙述正确的是( )

A. 该实验说明氨气是一种酸性气体
B. 进入烧瓶中的液体颜色由无色变为红色,说明氨水有碱性
C. 形成喷泉的原因是氨气溶于水后,烧瓶内的气压大于大气压
D. 用氯气代替氨气,利用此装置也可进行喷泉实验
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有甲、乙、丙、丁四种元素,已知:甲元素是地壳中含量最多的元素;乙元素为金属元素,它的原子核外K、L层电子数之和等于M、N层电子数之和;丙元素的单质及其化合物的焰色反应都显黄色;氢气在丁元素的单质中燃烧,火焰呈苍白色。请回答下列问题。
(1)写出元素符号:乙_________ 丁__________。
(2)甲、丙两元素可形成原子个数比为1:1的化合物,其电子式为___________。
(3)下列有关与丙同主族的金属元素的叙述中,错误的是________(填选项字母)。
A.各元素的单质在氧气中燃烧均生成相应的过氧化物
B.随电子层数增加,各元素单质的熔沸点逐渐降低
C.各元素单质均能与水反应生成氢气
D.各元素单质均能保存于煤油中
(4)乙和丁形成的化合物的类型是_________化合物(填“离子”或“共价”),用电子式表示其形成过程:____________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com