
【题目】I.已知:![]()
烃基烯基醚A的相对分子质量(Mr)为176,分子中碳氢原子数目比为3:4,与A相关的反应如下:
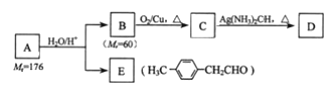
请回答下列问题:
(1)A的分子式为__,B的名称是__;
(2)写出C→D反应的化学方程式:__;
(3)链烃M的相对分子质量比B多24,分子中所有碳原子均在同一平面上,其结构简式是__;
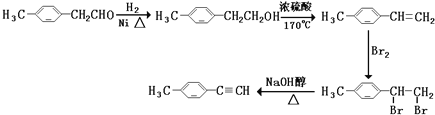
Ⅱ.由E转化为对甲基苯乙炔(![]() )的一条路线如下:
)的一条路线如下:

(4)①反应中所加试剂是__; ③的反应类型是__;
(5)写出G的结构简式:__;
(6)写出两种同时符合下列条件的E的同分异构体的结构简式:__。
①属于芳香醛;
②苯环上有两种不同环境的氢原子.
【答案】 C12H16O 1﹣丙醇(或正丙醇) ![]() (CH3)2C=C(CH3)2 氢气和催化剂 加成反应
(CH3)2C=C(CH3)2 氢气和催化剂 加成反应 ![]()
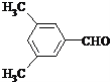
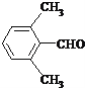
![]() (任意2种)
(任意2种)
【解析】
I.利用信息可知A的分子式可写为(C3H4)nO,则:40n+16=176,n=4,所以A的分子式为C12H16O,由信息可知,A反应生成B为醇,E为醛,B的相对分子质量为60,则B为CH3CH2CH2OH,B→C发生催化氧化反应,所以C为CH3CH2CHO,C→D为银镜反应,则D为CH3CH2COONH4,由B、E结构及信息可知,A为![]() ;
;
II.由E转化为对甲基苯乙炔(![]() ),先发生-CHO的加成,再发生醇的消去反应,然后与溴发生加成引入两个溴原子,最后发生卤代烃在NaOH醇溶液中的消去反应生成C≡C,合成路线流程图为
),先发生-CHO的加成,再发生醇的消去反应,然后与溴发生加成引入两个溴原子,最后发生卤代烃在NaOH醇溶液中的消去反应生成C≡C,合成路线流程图为
 ,据此解答
,据此解答
I.利用信息可知A的分子式可写为(C3H4)nO,则:40n+16=176,n=4,所以A的分子式为C12H16O,由信息可知,A反应生成B为醇,E为醛,B的相对分子质量为60,则B为CH3CH2CH2OH,B→C发生催化氧化反应,所以C为CH3CH2CHO,C→D为银镜反应,则D为CH3CH2COONH4,由B、E结构及信息可知,A为![]()
(1)由上述分析可知,A的分子式为C12H16O,B为CH3CH2CH2OH,名称为1-丙醇(或正丙醇);(2)C→D反应的化学方程式为:![]() ;(3)链烃M的相对分子质量比B多24,则M相对分子质量为84,分子中C原子最大数目=84/12=7,故M为C6H12,分子中所有碳原子均在同一平面上,则分子中含有C=C双键,且不饱和碳原子连接4个甲基,所以M结构简式为:(CH3)2C=C(CH3)2 ;
;(3)链烃M的相对分子质量比B多24,则M相对分子质量为84,分子中C原子最大数目=84/12=7,故M为C6H12,分子中所有碳原子均在同一平面上,则分子中含有C=C双键,且不饱和碳原子连接4个甲基,所以M结构简式为:(CH3)2C=C(CH3)2 ;
II.由E转化为对甲基苯乙炔(![]() ),先发生-CHO的加成,再发生醇的消去反应,然后与溴发生加成引入两个溴原子,最后发生卤代烃在NaOH醇溶液中的消去反应生成C≡C,合成路线流程图为
),先发生-CHO的加成,再发生醇的消去反应,然后与溴发生加成引入两个溴原子,最后发生卤代烃在NaOH醇溶液中的消去反应生成C≡C,合成路线流程图为 ; (4)①反应中所加试剂是:氢气和催化剂; ③的反应类型是:加成反应;(5)G的结构简式为:
; (4)①反应中所加试剂是:氢气和催化剂; ③的反应类型是:加成反应;(5)G的结构简式为:![]() ;(6)E的同分异构体符合条件:①属于芳香醛;②苯环上有两种不同环境的氢原子,符合条件的同分异构体的结构简式为
;(6)E的同分异构体符合条件:①属于芳香醛;②苯环上有两种不同环境的氢原子,符合条件的同分异构体的结构简式为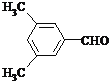 ,
, ,
,![]() (任意2种).
(任意2种).


 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
①二氧化硅可与NaOH溶液反应,因此可用NaOH溶液雕刻玻璃;
② 明矾溶于水可水解生成Al(OH)3胶体,因此可以用明矾对自来水进行杀菌消毒;
③ 可用蒸馏法、电渗析法、离子交换法等对海水进行淡化;
④ 从海带中提取碘只需用到蒸馏水、H2O2溶液和四氯化碳三种试剂;
⑤地沟油可用来制肥皂、提取甘油或者生产生物柴油;
⑥石英玻璃、Na2O·CaO·6SiO2、淀粉、氨水的物质类别依次为纯净物、氧化物、混合物、弱电解质。
A. ③⑤⑥ B. ①④⑤ C. 除②外都正确 D. ③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在体积为10 L的固定容器中发生反应:N2(g)+3H2(g)![]() 2NH3(g),反应过程如下图所示,下列说法正确的是
2NH3(g),反应过程如下图所示,下列说法正确的是

A. t1 min时正、逆反应速率相等
B. X曲线表示NH3的物质的量随时间变化的关系
C. 0~8 min,H2的平均反应速率v(H2)=3/4 mol·L-1·min-1
D. 10~12 min,N2的平均反应速率v(N2)=0.25 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以太阳能为热源,热化学硫碘循环分解水是一种高效、环保的制氢方法,其流程图如下:

相关反应的热化学方程式为:
反应I:SO2(g) + I2(g) + 2H2O(l) === 2HI(aq) + H2SO4(aq) ΔH1 =﹣213 kJ·mol-1
反应II:H2SO4(aq) === SO2(g) + H2O(l) + ![]() O2(g) ΔH2 = +327 kJ·mol-1
O2(g) ΔH2 = +327 kJ·mol-1
反应III:2HI(aq) === H2(g) + I2(g) ΔH3 = +172 kJ·mol-1
下列说法不正确的是:
A. 该过程实现了太阳能到化学能的转化
B. SO2和I2对总反应起到了催化剂的作用
C. 总反应的热化学方程式为:2H2O(l) === 2H2 (g)+O2(g) ΔH = +286 kJ·mol-1
D. 该过程降低了水分解制氢反应的活化能,但总反应的ΔH不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.只用新制氢氧化铜悬浊液即可检验淀粉是否水解完全
B.食用植物油和乙酸乙酯均可水解生成乙醇
C.鸡蛋清溶液中滴入浓硝酸微热有黄色沉淀生成
D.软脂酸(C15H31COOH)和油酸(C17H33COOH)均能使溴的CCl4溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用太阳光分解水制氢是未来解决能源危机的理想方法之一。某研究小组设计了如下图所示的循环系统实现光分解水制氢。反应过程中所需的电能由太阳能光电池提供,下列说法正确的是( )

A. 反应体系中I2和Fe2+可循环使用
B. 光电池是原电池
C. 光催化反应池中的反应方程式为:2I—+2Fe3+ ![]() I2+2Fe2+
I2+2Fe2+
D. 进入电解池B的溶液与从电解池B排出的溶液pH相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据反应Fe3++ Ag ![]() Fe2+ + Ag+ ,可用Fe3+的盐溶液做刻蚀液将试管中的银镜洗去。
Fe2+ + Ag+ ,可用Fe3+的盐溶液做刻蚀液将试管中的银镜洗去。
(1)FeCl3溶液显酸性,原因是_____________________________(用离子方程式表示)。
(2)关于FeCl3溶液洗银后的相关叙述正确的是_______(填序号)。
a.c(Fe3+)减小 b.c(Cl-)不变 c .铁元素质量减小
(3)乙同学欲从洗银废液(Fe3+、 Fe2+、 Ag+、 NO3-)中回收银和刻蚀液,设计了如下路线:

①过程Ⅰ中反应的离子方程式是_______________________、_____________________。
②过程Ⅱ中加入的试剂可以是_______________。
(4)镀银后的银氨溶液(Ag(NH3)2OH)放置时会析出有强爆炸性的物质,所以不能贮存。从银氨溶液中回收银的方法是:向银氨溶液中加入过量盐酸,过滤,向沉淀AgCl中加入羟氨(NH2OH),充分反应后可得银,羟氨被氧化为N2。
①生成AgCl沉淀的化学方程式是_____________________。
②若该反应中消耗3.3 g羟氨,理论上可得银的质量为_______g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取两份铝片,第一份与足量盐酸反应,第二份与足量烧碱溶液反应,同温同压下放出相同体积的气体,则消耗的HCl和NaOH的物质的量之比为( )
A.1:1B.2:1C.3:1D.1:3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com