
����Ŀ���ұ���������������ϩ�ķ�Ӧ��![]()
��1��һ���¶��£���amol�ұ��������ΪVL���ܱ������У�����������Ӧ����Ӧʱ����������������ѹǿ���������±���
ʱ��/min | 0 | 10 | 20 | 30 | 40 |
��ѹǿ/1000kPa | 1.0 | 1.2 | 1.3 | 1.4 | 1.4 |
��ƽ��ʱ���������������ʵ����ܺ�Ϊ mol���ұ���ת����Ϊ
����ʽ������¶��¸÷�Ӧ��ƽ�ⳣ��K
��2�����ݻ�ѧ��Ӧԭ����������Сѹǿ�Ը÷�Ӧ��Ӱ��
��3��ʵ�������ķ�Ӧ�ڳ�ѹ�½��У������ұ������в���ˮ��������������ѧ���ݼ���õ��¶Ⱥ�Ͷ�ϱȶ��ұ�ת���ʵ�Ӱ�����ͼ��ʾ��[M=n��H2O��/n���ұ�]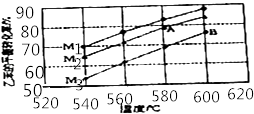
�Ƚ�ͼ��A��B�����Ӧƽ�ⳣ����С��KAKB
��ͼ��Ͷ�ϱȣ�M1��M2��M3���Ĵ�С˳��Ϊ
�����ŷ�Ӧ�Ľ��У������ϵ�������̿ʹ����Լ�����ˮ���������ڻָ������Ļ��ԣ�ԭ�������û�ѧ����ʽ��ʾ��
���𰸡�
��1��1.4a��40%��![]()
��2���÷�Ӧ���������ӣ���Сѹǿʹƽ�����ƣ��ұ�ת����������ϩ�������ӣ���Сѹǿʹ�ұ�Ũ�ȼ�С����Ӧ���ʼ�С
��3������M1��M2��M3��C+H2O ![]() CO+H2
CO+H2
���������⣺��1���������ݻ��̶�����������ѹǿ������������ʵ��������ȣ����ݱ������ݿ�֪���ﵽƽ��ʱѹǿΪ��Ӧǰ��1.4������ƽ��ʱ����������ʵ���Ϊ��amol��1.4=1.4amol��
ƽ��ʱ��������ʵ�������1.4amol��amol=0.4amol������x mol �ұ�����ת����
|
|
| H2 | ��n |
1 | 1 | 1 | 1 | |
xmol | 0.4amol |
��x= ![]() =0.4amol��
=0.4amol��
�����ұ���ת����Ϊ�� ![]() ��100%=40%��
��100%=40%��
���Դ��ǣ�1.4a��40%��
�ڷ�����ӦΪ
|
|
| H2 | |
��Ӧǰ��mol�� | a | 0 | 0 | |
ת����mol�� | 0.4a | 0.4a | 0.4a | |
ƽ��ʱ��mol�� | 0.6a | 0.4a | 0.4a |
��÷�Ӧ��ƽ�ⳣ��Ϊ��K= ![]() =
= ![]() ��
��
���Դ��ǣ� ![]() ����2�����ݷ�Ӧ����ʽ��֪���÷�Ӧ������ķ��������ӣ����Сѹǿ��ƽ�����ƣ��ұ�ת����������ϩ�������ӣ���Сѹǿ��ʹ�ұ�Ũ�ȼ�С����Ӧ���ʼ�С��
����2�����ݷ�Ӧ����ʽ��֪���÷�Ӧ������ķ��������ӣ����Сѹǿ��ƽ�����ƣ��ұ�ת����������ϩ�������ӣ���Сѹǿ��ʹ�ұ�Ũ�ȼ�С����Ӧ���ʼ�С��
���Դ��ǣ��÷�Ӧ���������ӣ���Сѹǿʹƽ�����ƣ��ұ�ת����������ϩ�������ӣ���Сѹǿʹ�ұ�Ũ�ȼ�С����Ӧ���ʼ�С����3����ͼ�������֪�����¶����ߣ��ұ�ת��������˵������ƽ��������У�����ӦΪ���ȷ�Ӧ��AB����B���¶ȸߣ�ƽ��������г̶ȴ�ƽ�ⳣ��B���KA��KB ��
���Դ��ǣ��������ұ���Խ�࣬Ͷ�ϱ�ԽС���ұ�ת����ԽС���ݴ˷����ж�M��ֵ��M1��M2��M3 ��
���Դ��ǣ�M1��M2��M3���۴����ϵ�������̿ʹ����Լ�����ˮ���������ڻָ������Ļ�������Ϊ̼��ˮ�����ڸ����·�Ӧ����һ����̼�������������ȥ����Ļ�̼����Ӧ�Ļ�ѧ����ʽΪ��C+H2O ![]() CO+H2 ��
CO+H2 ��
���Դ��ǣ�C+H2O ![]() CO+H2 ��
CO+H2 ��
�����㾫����������Ŀ����֪���������û�ѧƽ��״̬���ʼ������ͻ�ѧƽ��ļ�������֪ʶ���Եõ�����Ĵ𰸣���Ҫ���ջ�ѧƽ��״̬�����������ȡ��� V��=V��>0�����������Ƕ�̬ƽ�⣬ƽ��ʱ��Ӧ���ڽ��У�����������Ӧ������и���ְٷֺ������䣻���䡱�������ı䣬ƽ�ⱻ���ƣ������µ������½����µĻ�ѧƽ�⣻��;���أ�����������䣬���淴Ӧ�����Ǵ�����Ӧ��ʼ�����Ǵ��淴Ӧ��ʼ�����ɽ���ͬһƽ��״̬����Ч������Ӧ��ת����=ת��Ũ�ȡ���ʼŨ�ȡ�100%=ת�����ʵ�������ʼ���ʵ�����100%����Ʒ�IJ���=ʵ�����ɲ�������ʵ����������Ͽɵõ���������ʵ�����100%��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������ϢϢ��أ�����˵����ȷ���ǣ� ��
A.ҽ�þƾ���Ũ��ͨ����95%
B.���ۡ���֬�͵����ʶ��Ǹ߷��ӻ�����
C.���г��ּ�����ͨ���ǵ绯ѧ��ʴ����
D.úȼ�ղ���������ֱ���ŷŵ������У������ˮ��ĸ�Ӫ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���̲�����ȡ�����ķ������£�
��1����ⷨ���������۲���ͼ1���ش� 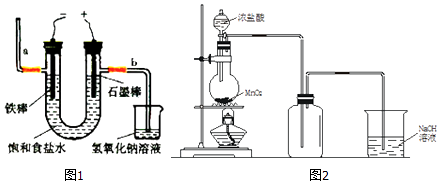
�ٴ˷�Ӧ��ѧ����ʽΪ ��
��������ʳ��ˮ�к��з�̪��ͨ��������������ʯī������������죮ͼ��b�˲�������������ʪ��ĵ��۩�KI��ֽ���飬������Ϊ ��
��2��ʵ����Ҳ�����ü���MnO2��Ũ������ȡCl2 �� ��ͼ2
��ʢװŨ�������������Ϊ��
����Ҫ�ռ������Ҹ����Cl2 �� ��װ�û�Ӧ���μ�����Լ�Ϊ��
��NaOH��Һ�������� �� ������Ӧ�Ļ�ѧ����ʽ����
��ʵ�������������ַ�����������I���ú�HCl 146g��Ũ������������MnO2��Ӧ��
II����87gMnO2������Ũ���ᷴӦ�����õ�����
A�� I�� II�� B�� II�� I�� C��һ���� D�����Ƚ�
�ݽ�Cl2����ˮ�õ����Ƶ���ˮ���ò�����պȡ���Ƶ���ˮ������pH��ֽ�ϣ�����Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����Ҫ��д�����з�Ӧ�Ļ�ѧ����ʽ��
���ɱ���FeCl3��Һ�Ʊ�Fe(OH)3����_______________________________��
������ḯʴ����____________________________________��
��2����Ҫ��д�����з�Ӧ�����ӷ���ʽ��
����Ư������Ч�ɷ�Ϊ���������____________________________________��
�������軯����Һ������Һ�к���Fe3+____________________________________��
����NaHSO4��Һ����μ���Ba(OH)2��Һ������____________________________________��������������Һ�м����μ�Ba(OH)2��Һ��д���˲������ӷ���ʽ_______________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ظ���أ�K2Cr2O7����Ҫ�����ƸӡȾ����Ƶȣ���ˮ��Һ�д���ƽ�⣺Cr2O72��+H2O2CrO42��+2H+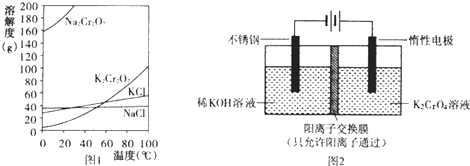
��1����֪�й������ܽ����ͼ1���ø��ֽⷨ�Ʊ�K2Cr2O7�IJ��������ǣ���Na2Cr2O7��Һ�м������ѧʽ���������ܽ⣬������ҺpHԼΪ5��������Һ��������������������ʱ�� �� ���˵õ��ֲ�Ʒ�������ؽᾧ���ᴿ�ֲ�Ʒ��
��2���Ը���أ�K2CrO4��Ϊԭ�ϣ��õ绯ѧ���Ʊ��ظ���ص�ʵ��װ����ͼ2��
�ٲ����������д���õ缫�ĵ缫��Ӧʽ ��
�ڷ����������ܵõ��ظ������Һ��ԭ�� ��
�۵�����ص�ת���ʴﵽxʱ������Һ��K��Cr�����ʵ���֮��Ϊ
��3�����Ի����������Ⱦ��ij���Է�ˮ�к���Cr2O72�� �� ����ʱ���ý��������ƣ�Na2S2O5����Cr2O72��ת��Ϊ���Խϵ͵�Cr3+ �� �ٵ���pHԼΪ8��ʹ��Ԫ�س������������������ˮ��Cr3+Ũ�ȣ�����0.5mgL��1��ﵽ�ŷű���
��Na2S2O5�μӷ�Ӧ�����ӷ���ʽΪ ��
�ھ��������մ�����ķ�ˮ��������Cr3+Ũ��ԼΪ mgL��1 ��
����֪������Ksp[Cr��OH��3]��6��10��31��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��N4�ķ��ӽṹ���ư����ӣ����Ľṹ��ͼ��ʾ����֪����1mol N��N����Ҫ����167kJ����������1mol N��N����ų�942kJ����������������Ϣ�����ݣ�����˵������ȷ���ǣ� �� 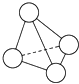
A.1 mol N4����ת��ΪN2���ų�775 kJ����
B.1 mol N4����ת��ΪN2���ų�882 kJ����
C.1 mol N4����ת��ΪN2������775 kJ����
D.1 mol N4����ת��ΪN2������882 kJ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����2C��s��+O2��g���T2CO��g����H=��221.0kJmol��1��
��2H2��g��+O2��g���T2H2O��g����H=��483.6kJmol��1 ��
���Ʊ�ˮú���ķ�ӦC��s��+H2O��g���TCO��g��+H2��g���ġ�HΪ�� ��
A.262.6 kJmol��1
B.��131.3 kJmol��1
C.��352.3 kJmol��1
D.131.3 kJmol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����ϴ���ij�����������Ĥ����Ӧ�����ӷ���ʽΪ________________����ϴʱ��������ð����ԭ����_________________�������ӷ���ʽ��ʾ�����÷�Ӧ�е���������___________��
��2����ȥ̼���ƹ����е�̼���������ʣ�������Ӧ�Ļ�ѧ����ʽΪ_________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Fe3+��SO42����Al3+��X�������������ʵ���֮��2: 4 :1 :1����������ͬһ��Һ�У�X�����ǣ�������
A.Na+B.Cl��C.CO32��D.OH��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com