
����Ŀ��������������þ��2.8 gͶ��100 mLϡ�����������ٲ�������Ϊֹ�����ռ�����״������2.24 L����������Һ�е���4.0 mol�qL-1������������Һ����ʼ����ʱ�������ɣ��μ�һ����������������Һ��ʼ���ְ�ɫ���������μ�����������Һ�����100 mLʱ��ǡ��ʹ������ȫ������(��Һ����仯���Բ���)��
(1)þ�����ѱ�������þ��δ��������þ�����ʵ���֮��____________��
(2)����������Һ�����ʵ����ʵ���Ũ��___________��
���𰸡�1:10 1.0 mol/L
��������
��1��þ��ϡ���ᷴӦ��������þ����������Ӧ�Ļ�ѧ����ʽΪMg+H2S04=MgSO4+H2������״�������£�2.24 L���������ʵ���Ϊ0.1mol���ɻ�ѧ����ʽ��֪þ�����ʵ���Ϊ0.1mol��������þ�����ʵ���Ϊ![]() =0.01mol����þԭ�Ӹ����غ��֪����������þ�����ʵ���Ϊ0.01mol��þ�����ѱ�������þ��δ��������þ�����ʵ���֮��Ϊ0.01mol��0.1mol=1:10���ʴ�Ϊ��1:10��
=0.01mol����þԭ�Ӹ����غ��֪����������þ�����ʵ���Ϊ0.01mol��þ�����ѱ�������þ��δ��������þ�����ʵ���֮��Ϊ0.01mol��0.1mol=1:10���ʴ�Ϊ��1:10��
��2���������֪�����������������Һ���к���Һ��δ��Ӧ��H2SO4��Ȼ����þ���ӷ�Ӧ����������þ������������þ������ȫʱNaOHȫ��ת��ΪNa2SO4������ԭ�Ӹ����غ��֪��n��Na2SO4��=![]() n��NaOH��=
n��NaOH��=![]() ��4.0 mol�qL-1��0.1L=0.2mol������������Һ�������Ƶ����ʵ���Ũ��
��4.0 mol�qL-1��0.1L=0.2mol������������Һ�������Ƶ����ʵ���Ũ��![]() =1.0mol/L���ʴ�Ϊ��1.0mol/L��
=1.0mol/L���ʴ�Ϊ��1.0mol/L��


 �ִʾ�ƪ��ͬ�����Ĵ��ϵ�д�
�ִʾ�ƪ��ͬ�����Ĵ��ϵ�д� �߽�������ϵ�д�
�߽�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��.��һ���¶��µĺ���������,���������������ٷ����仯ʱ�����ܱ�����Ӧ�� A��s��+3B��g��![]() 2C��g��+D��g���Ѵ�ƽ��״̬����
2C��g��+D��g���Ѵ�ƽ��״̬����
A. ��������ѹǿB. ���������ܶ�
C. 3v����C��=2v����B��D. �����ƽ����Է�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ�������ƹ�ʹ������ȼ�ϵ�صĹ���������ij������������Ϊ30%��KOH��ҺΪ����ʵ�����ȼ�ϵ����ʹ��ʱ�ĵ缫��Ӧ���£�2H2 +4OH- - 4e-![]() 4H2O�� O2 + 2H2O + 4e-
4H2O�� O2 + 2H2O + 4e-![]() 4OH- �������йظ�����ȼ�ϵ�ص�˵���У�����ȷ����( )
4OH- �������йظ�����ȼ�ϵ�ص�˵���У�����ȷ����( )
A.�õ�ع���һ��ʱ���KOH��Һ��Ũ������
B.����ʱ���ܷ�ӦΪ��2H2 + O2![]() 2H2O
2H2O
C.ȼ�ϵ�ص���Դ�����ʽϸߣ��������������Ժ�
D.��ȼ�ϵ�ؿ���������������ͬ�ĵ缫
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����.ʳ�����ճ�����ı���Ʒ��Ҳ����Ҫ�Ļ���ԭ�ϡ���ʳ�γ���������Ca2+��Mg2+��SO42-���������ӣ�ʵ�����ᴿNaCl���������£�

�ṩ���Լ�������Na2CO3��Һ������K2CO3��Һ��Ca(OH)2��Һ��BaCl2��Һ��Ba(NO3)2��Һ
��1������ȥ��Һ���е�Ca2+��Mg2+��SO42-���ӣ�ѡ��A���������Լ������μ�˳������Ϊ________��ֻ�ѧʽ����
��2���������������________�������õ���������Ҫ������̨���ƾ��ơ���Ȧ��������__________�����������ƣ���
��3���������Ŀ���ǣ������ӷ���ʽ��ʾ��_________________________
��.һ����ɫ��Һ�п��ܺ���Na+��Fe3+��H+��Mg2+��CO32-��OH-��HCO3-��Cl-��SO42-�������е������֡�Ϊ��ȷ����Һ����ɣ����������²�����
������Һ�еμӷ�̪��Һ����Һ�Ժ�ɫ��
��ȡ2mL��Һ���ȼ�����ϡ�����ữ��������������ټ��Ȼ�����Һ���м��飬û����������
��4��ԭ��Һ��һ�����ڵ�������______________��һ�����ܴ������ڵ�������_______________��
��5�������������������ܿ϶��Ƿ���ڵ�������________���Կ��ܺ��е����ӣ���ν���ʵ���Խ�һ������____________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о�С����ϳ�Ⱦ��X��ҽҩ�м���Y��
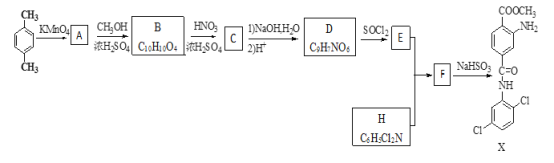
��֪����![]() ��
��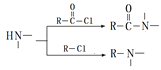 ��
��![]() ��
��![]() ��
��
��1������˵����ȷ����_________��
A.������A��������NaHCO3��Ӧ�������� B.X�ķ���ʽ��C15H14Cl2O3N2
C.������C�ܷ���ȡ������ԭ���ӳɷ�Ӧ D.A��B��B��C�ķ�Ӧ���;�Ϊȡ����Ӧ
��2��������D�Ľṹ��ʽ��_________��
��3��д��E+H��F �Ļ�ѧ��Ӧ����ʽ__________________��
��4��д��������B��C10H10O4��ͬʱ������������������ͬ���칹��Ľṹ��ʽ______________��
����NaHCO3��Һ��Ӧ��0.1mol��ͬ���칹���ܲ���4.48L����״���£�CO2���壻�ڱ����ϵ�һ�ȴ���ֻ�������ұ����ϵ�ȡ�����������������ۺ˴Ź������������ֲ�ͬ��ѧ�������⣬�ҷ������Ϊ1��2��2��2��3��
��5���������ϩΪԭ�Ϻϳ��Ʊ�Y��![]() ���ĺϳ�·��________________��������ͼ��ʾ�����Լ���ѡ����
���ĺϳ�·��________________��������ͼ��ʾ�����Լ���ѡ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ����������ȷ���ǣ� ��
A.̼��ĵ��뷽��ʽ��H2CO3![]() 2H++CO32��
2H++CO32��
B.������������ͨ������������Һ�еĻ�ѧ����ʽ��SO2+NaOH=NaHSO3
C.̼��������Һ�Լ��ԣ�HCO3��+H2O![]() H3O++CO32��
H3O++CO32��
D.��С�մ���Һ�м��������ʯ��ˮ��Ca2++OH��+HCO3��=CaCO3��+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£����и���������ָ����Һ���ܴ���������ǣ� ��
A.pH=l����Һ�У�Fe2+��NO3����SO42����Na+
B.��ˮ�����c(H+)=1��10��14mo1��L��1����Һ�У�Ca2+��K+��Cl����HCO3��
C.![]() =1013����Һ�У�NH4+��Al3+��NO3����Cl��
=1013����Һ�У�NH4+��Al3+��NO3����Cl��
D.c(Fe3+)=0.1mol��L��1����Һ�У�K+��ClO����SO42����SCN��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ܱ������зֱ����N2��H2��O2�������壬���¸��������������ȷ����(����)
A.�����ǵ�������¶ȡ�ѹǿ����ͬʱ������������ܶȣ���(H2)>��(N2)>��(O2)
B.�����ǵ��¶Ⱥ��ܶȶ���ͬʱ�����������ѹǿ��P(H2)>P(N2)>P(O2)
C.�����ǵ��������¶ȡ�ѹǿ����ͬʱ����������������V(O2)>V(N2)>V(H2)
D.�����ǵ�ѹǿ��������¶Ⱦ���ͬʱ�����������������m(H2)>m(N2)>m(O2)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ɶ��������Ƹߴ�����������£������ж��д������

A. �٢ڢ۾�����������ԭ��Ӧ B. H2��HCl����ѭ������
C. SiO2��һ�ּ�Ӳ���۵Ĺ��� D. SiHCl3Ħ������Ϊ135.5g
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com