
【题目】硅是无机非金属材料的主角之一。下列关于硅及其化合物性质的说法,不正确的是
A. 硅的非金属性比硫弱 B. 硅酸钠可溶于水
C. SiO2与氢氟酸能反应 D. 硅原子易失去或得到电子
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 从性质的角度分类,SO2属于酸性氧化物
B. 从对大气及环境影响的角度,SO2是一种大气污染物
C. 从在水中是否发生电离的角度,SO2属于电解质
D. 从元素化合价的角度分类,SO2即可作氧化剂又可作还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表揭示了许多元素的相似性和递变规律,根据元素周期表元素的性质和递变规律,回答下列问题.
(1)1~20号元素中金属性最强的元素与水反应生成的化合物为 .
(2)写出电子数为18的四种不同形式的微粒(原子、离子、双原子分子各一种)、和 .
(3)写出原子序数为16的元素阴离子的核外电子排布示意图 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知CaSO4受热分解,由于受热温度不同,气体成分也不同.气体成分可能为SO2、SO3和O2中的一种、二种或三种.某化学课外活动小组准备通过系列实验探究CaSO4分解生成的气体,进而确定CaSO4分解的化学方程式.
(1)[提出猜想]Ⅰ.所得气体的成分可能只含SO3一种;
Ⅱ.所得气体的成分可能含有二种;(填分子式)
(2)Ⅲ.所得气体的成分可能含有 SO2、SO3、O2三种.[设计实验]
该化学课外活动小组准备通过测定D装置的增重以及量筒中水的体积,来探究CaSO4分解生成的气体成分,进而确定CaSO4分解的化学方程式.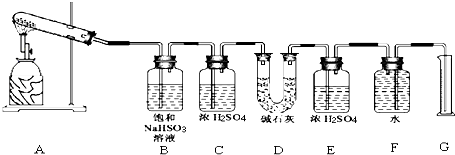
[实验过程]
根据上述实验方案进行试验.已知实验结束时,CaSO4完全分解.
请结合以下实验现象和记录的实验数据进行分析:
①若实验结束时,G中量筒没有收集到水,则证明猜想正确.(填Ⅰ或Ⅱ或Ⅲ)
②若实验结束时,装置D的总质量增加,能否断定气体产物中一定含有SO2而不含SO3?请说明理由: .
③该实验设计中,容易给测定带来较大误差的因素有 .
(写出一种即可)
④经改进后,有两组同学进行该实验,由于加热时的温度不同,实验测得数据也不同,
相关数据如下:
实验小组 | 称取CaSO4 | 装置D增加 | 量取气体体积的装置测量的气体体积 (折算成标准状况下气体的体积) (mL) |
一 | 4.08 | 2.56 | 224 |
二 | 5.44 | 2.56 | 448 |
请通过计算,推断第二组同学得出的CaSO4分解的化学反应方程式:
第二组: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将 Cl2 通入 NaBr 和 NaI 的混合液中,待反应充分后将所得的溶液加热蒸干,并灼烧,最后将得 到的固体冷却、称量.称量所得固体的质量与通入 Cl2 的体积关系如图所示.则原混合液中 NaI 的物 质的量为( )

A. 0.5 mol B. 0.4 mol C. 0.3 mol D. 0.25 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期元素A、B、C、D的性质或结构信息如下:信息①原子半径大小:A>B>C>D
信息②四种元素之间形成的某三种分子的比例模型及部分性质:
请根据上述信息回答下列问题.
(1)B元素在周期表中的位置;
(2)BC2分子的电子式;
(3)A元素的单质与物质甲发生反应的离子方程式;
(4)丙的钠盐溶液呈性,用化学用语表示其原因;
(5)物质丁的元素组成和甲相同,丁分子具有18电子结构.向盛有一定浓度丁溶液的试管中,逐滴加入用少量稀硫酸酸化的硫酸亚铁溶液.滴加过程中的现象是:①浅绿色溶液变成深棕黄色;
②有少量气泡出现(经验证是氧气),片刻后反应变得剧烈 , 并放出较多热量,继续滴加溶液,静置一段时间;
③试管底部出现红褐色沉淀 . 向浊液中再滴入稀硫酸,沉淀溶解,溶液呈黄色.
请用化学方程式或离子方程式及必要的文字解释①、②、③中划线的字.
①;
②;
③ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某汽车安全气囊的产气药剂主要含有NaN3、Fe2O3、KClO4、NaHCO3等物质.当汽车发生碰撞时,产气药剂产生大量气体使气囊迅速膨胀,从而起到保护作用.
(1)NaN3是气体发生剂,受热分解产生N2和Na,NaN3中N3﹣中心原子采用杂化.
(2)Fe2O3是主氧化剂,与Na反应生成的还原产物为(已知该反应为置换反应).
(3)KClO4是助氧化剂,反应过程中与Na作用生成KCl和Na2O,KClO4含有化学键的类型为 , K的原子结构示意图为 .
(4)NaHCO3是冷却剂,吸收产气过程中释放的热量而发生分解,其化学方程式为 .
(5)100g上述产气药剂产生的气体通过碱石灰后得到N2 33.6L(标准状况).
①用碱石灰除去的物质为;
②该产气药剂中NaN3的质量分数为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于胶体的叙述中,正确的是( )
A.胶体是一种分散质直径小于10-10m的分散系
B.用过滤的方法除去氢氧化铁胶体中的分散质
C.CuSO4溶液是一种胶体
D.用一束光线照射胶体,在垂直于光线的方向可看到一条光亮的通路
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com