
| A、0.02 mol |
| B、0.01 mol |
| C、0.04 mol |
| D、无法计算 |
| 0.224L |
| 22.4L/mol |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、按系统命名法,化合物 的名称是二溴乙烷 的名称是二溴乙烷 |
| B、丙烯的结构简式为CH2CHCH3 |
| C、2,2-二甲基丙烷的一氯代物有1种 |
| D、苯与甲苯互为同系物,均能使KMnO4酸性溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A.目的:浓度对化学反应速率的影响 | B.目的:配制银氨溶液 |
加入 1mol/L 1mL硫酸 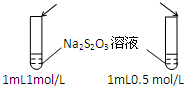 |
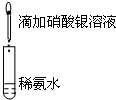 |
| C.目的:温度对化学平衡的影响 | D.目的:探究醋酸、碳酸、苯酚的酸性强弱 |
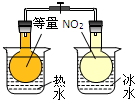 |
 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、3:3:2 | B、2:2:3 |
| C、1:1:1 | D、无法比较 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、放电时CO32-向负极移动 |
| B、放电时CO32-向正极移动 |
| C、正极反应:4OH--4e-═2H2O+O2↑ |
| D、当电池中生成1 mol水时,转移4 mol电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com