
| A. | 配制100mL该溶液需用5.85g NaCl | |
| B. | 该溶液的物质的量浓度为1mol•L -1 | |
| C. | 该溶液中含有58.5g NaCl | |
| D. | 量取100mL该溶液,其中Na+的物质的量为0.1mol |
分析 结合c=$\frac{n}{V}$、m=nM计算.
解答 解:A.0.5L某NaCl溶液中含有0.5molNa+,c(NaCl)=$\frac{0.5mol}{0.5L}$=1mol/L,则配制100mL该溶液需NaCl的质量为1mol/L×0.1L×58.5g/mol=5.85g,故A正确;
B.由选项A可知,该溶液的物质的量浓度为1mol•L -1,故B正确;
C.含0.5molNa+,则NaCl的质量为0.5mol×58.5g/mol=29.25g,故C错误;
D.溶液具有均一性,则量取100mL该溶液,其中Na+的物质的量为0.1L×1mol/L=0.1mol,故D正确;
故选C.
点评 本题考查物质的量浓度的计算,为高频考点,把握质量、体积、浓度与物质的量的关系为解答的关键,侧重分析与计算能力的考查,注意溶液具有均一性,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 属于置换反应 | B. | 碳发生了还原反应 | ||
| C. | 二氧化硅是氧化剂 | D. | 24g碳充分反应生成28g硅 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HClO 中氯元素化合价比 HClO4 中氯元素化合价低,所以 HClO4 的氧化性强 | |
| B. | 已知①Fe+Cu2+═Fe2++Cu; ②2Fe3++Cu═2Fe2++Cu2+,则氧化性强弱顺序为:Fe3+>Cu2+>Fe2+ | |
| C. | 已知还原性 B->C->D-,反应 2C-+D2═2D-+C2 和 2C-+B2=2B-+C2 都能发生 | |
| D. | 具有强氧化性和强还原性的物质放在一起就能发生氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
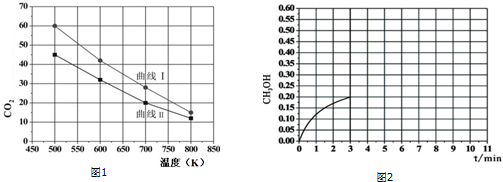
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
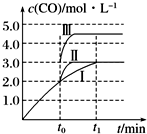 工业上可用CO或CO2来生产燃料甲醇.已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
工业上可用CO或CO2来生产燃料甲醇.已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:| 化学反应 | 平衡 常数 | 温度/℃ | |
| 500 | 800 | ||
| ①2H2(g)+CO(g)?CH3OH(g) | K1 | 2.5 | 0.15 |
| ②H2(g)+CO2(g)?H2O(g)+CO(g) | K2 | 1.0 | 2.50 |
| ③3H2(g)+CO2(g)?CH3OH(g)+H2O(g) | K3 | ||
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl和Na2CO3 | B. | 稀H2SO4和NaHCO3 | C. | CaCl2和Na2CO3 | D. | Ba(OH)2和NaHSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t/min | X/mol | Y/mol | Z/mol |
| 0 | 1.00 | 2.00 | 0.00 |
| 1 | 0.90 | 1.80 | 0.20 |
| 3 | 0.75 | 1.50 | 0.50 |
| 5 | 0.65 | 1.30 | 0.70 |
| 9 | 0.55 | 1.10 | 0.90 |
| 10 | 0.55 | 1.10 | 0.90 |
| 14 | 0.55 | 1.10 | 0.90 |
 2Z
2Z查看答案和解析>>
科目:高中化学 来源: 题型:选择题
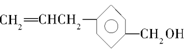 ,下列关于有机物A的说法错误的是( )
,下列关于有机物A的说法错误的是( )| A. | 有机物A可以与氯气反应 | |
| B. | 有机物A与 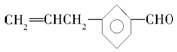 互为同分异构体 互为同分异构体 | |
| C. | 有机物A可与CH3COOH发生酯化反应 | |
| D. | 有机物A可以使酸性KMnO4溶液褪色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com