
【题目】香料甲和G在生活中有很多用途,工业上利用有机物A(![]() )来制备,其合成路线如下:
)来制备,其合成路线如下:

已知:R1—CHO+R2—CH2—CHO ![]()
![]() (R1、R2代表烃基或氢原子)
(R1、R2代表烃基或氢原子)
回答下列问题:
(1)C的名称是____,G中官能团的名称是__________。
(2)②的反应类型是________,F的结构简式为_______________。
(3)下列关于C的叙述正确的是___________.
A. 分子式为C9H10O B. 1mol E最多能与5molH2发生加成反应
C. 自身能发生加聚、缩聚反应 D. 最多有9个碳原子位于同一平面
(4)C有多种同分异构体,其中属于芳香族化合物的有____种。
(5)写出反应①的化学方程式__________________________________。
(6)F的同分异构体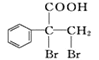 是一种重要的药物中间体,其合成路线与G相似,请以为原料设计它的合成路线(其他所需原料自选)。____________
是一种重要的药物中间体,其合成路线与G相似,请以为原料设计它的合成路线(其他所需原料自选)。____________
【答案】 苯甲醇 溴原子、羧基 加成反应 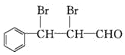 BD 4
BD 4 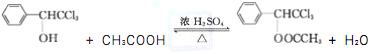
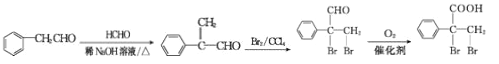
【解析】C在铜的催化氧化下转化为苯甲醛,则C为苯甲醇,B在氢氧化钠的水溶液中加热反应生成苯甲醇,且B为![]() 与氯气在光照条件下发生取代反应而得,故B为
与氯气在光照条件下发生取代反应而得,故B为![]() ;根据已知:R1—CHO+R2—CH2—CHO
;根据已知:R1—CHO+R2—CH2—CHO ![]()
![]() ,苯甲醛与乙醛在稀氢氧化钠水溶液中加热反应生成E为
,苯甲醛与乙醛在稀氢氧化钠水溶液中加热反应生成E为![]() ,
,![]() 与溴发生加成反应生成F为
与溴发生加成反应生成F为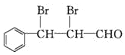 ;
;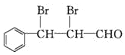 氧化得到G为
氧化得到G为![]() 。(1)C的名称是苯甲醇,G为
。(1)C的名称是苯甲醇,G为![]() ,官能团的名称是溴原子、羧基;(2)②是苯甲醛与三氯甲烷在氢氧化钾中发生加成反应生成
,官能团的名称是溴原子、羧基;(2)②是苯甲醛与三氯甲烷在氢氧化钾中发生加成反应生成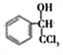 ,反应类型是加成反应,F的结构简式为
,反应类型是加成反应,F的结构简式为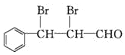 ;(3)A. E(
;(3)A. E(![]() )的分子式为C9H8O,选项A错误;B. 一分子E中含有一个苯环、一个碳碳双键和一个羰基,则1molE最多能与5molH2发生加成反应,选项B正确;C. 分子中含有碳碳双键和醛基,自身能发生加聚反应,,但不能发生缩聚反应,选项C错误;D. 根据苯分子中12个原子共面,乙烯6个原子共面,甲醛4个原子共面,若此三者同面则最多有9个碳原子位于同一平面,选项D正确。答案选BD;(4)C(苯甲醇)有多种同分异构体,其中属于芳香族化合物的有甲苯醚、邻甲基苯酚、间甲基苯酚、对甲基苯酚4种;(5)反应①的化学方程式为
)的分子式为C9H8O,选项A错误;B. 一分子E中含有一个苯环、一个碳碳双键和一个羰基,则1molE最多能与5molH2发生加成反应,选项B正确;C. 分子中含有碳碳双键和醛基,自身能发生加聚反应,,但不能发生缩聚反应,选项C错误;D. 根据苯分子中12个原子共面,乙烯6个原子共面,甲醛4个原子共面,若此三者同面则最多有9个碳原子位于同一平面,选项D正确。答案选BD;(4)C(苯甲醇)有多种同分异构体,其中属于芳香族化合物的有甲苯醚、邻甲基苯酚、间甲基苯酚、对甲基苯酚4种;(5)反应①的化学方程式为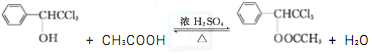 ;
;
(6)F的同分异构体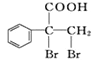 是一种重要的药物中间体,其合成路线与G相似,根据以上合成路线可知,合成路线为
是一种重要的药物中间体,其合成路线与G相似,根据以上合成路线可知,合成路线为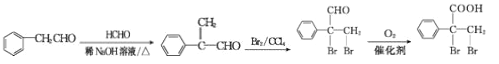 。
。


 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案科目:高中化学 来源: 题型:
【题目】下面是某化学研究小组探究外界条件对化学反应速率和化学平衡影响的图像,其中图像和实验结论表达均正确的是( )


A. ①是其他条件一定时,反应速率随温度变化的图像,正反应ΔH<0
B. ②是在平衡体系的溶液中溶入少量KCl晶体后化学反应速率随时间变化的图像
C. ③是在有无催化剂存在下建立的平衡过程图像,a是使用催化剂时的曲线
D. ④是一定条件下,向含有一定量A的容器中逐渐加入B时的图像,压强p1>p2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】控制变量是科学研究的重要方法。相同质量的锌粉与足量稀硫酸分别在下列条件下发生反应,开始阶段化学反应速率最大的是( )
选项 | A | B | C | D |
c(H2SO4)/(mol·L-1) | 0.5 | 2 | 0.5 | 2 |
t/℃ | 20 | 20 | 50 | 50 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于热化学反应的描述中正确的是( )
A. HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则1 mol硫酸与足量氢氧化钡溶液反应放热为 114.6 kJ
B. H2(g)的燃烧热是285.8 kJ·mol-1,则2H2O(l)===2H2(g)+O2(g)反应的ΔH=+571.6 kJ·mol-1、
C. 放热反应比吸热反应容易发生
D. 1 mol丙烷燃烧生成水和二氧化碳所放出的热量是丙烷的燃烧热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次磷酸(H3PO2)是一种精细磷化工产品,具有较强还原性。回答下列问题:
(1)H3PO2是一元中强酸,写出其电离方程式:____________。
(2)H3PO2及NaH2PO2均可将溶液中的Ag+还原为银,从而可用于化学镀银。
①H3PO2中,P元素的化合价为___________,NaH2PO2___________ (填“能”或“不能”)与NaOH反应。
②利用H3PO2进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4∶1,则氧化产物为________(填化学式)。
(3)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应。写出白磷与Ba(OH)2溶液反应的化学方程式:____________________。
(4)H3PO2也可用电渗析法制备,“四室电渗析法”工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过):
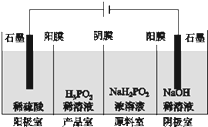
①写出阳极的电极反应式______________________________________________。
②分析产品室可得到H3PO2的原因______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中,溶质的物质的量浓度不是1 mol/L的是( )
A. 10 g NaOH固体溶解在水中配成250 mL溶液
B. 将80 g SO3溶于水并配成1 L的溶液
C. 将0.5 mol/L的NaNO3溶液100 mL加热蒸发掉50 g水的溶液
D. 标况下,将22.4 L氯化氢气体溶于水配成1 L溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置或操作设计正确、且能达到目的的是( )
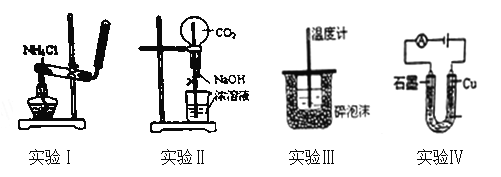
A. 实验Ⅰ:实验室制备氨气 B. 实验Ⅱ:用二氧化碳作喷泉实验
C. 实验Ⅲ:进行中和热的测定 D. 实验Ⅳ:电解氯化铜溶液得到铜和氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义。
(1)CO可用于炼铁,已知:
Fe2O3(s)+3C(s)═2Fe(s)+3CO(g)△H1=+489.0kJmol-1,
C(s)+CO2(g)═2CO(g)△H2=+172.5kJmol-1
则CO还原Fe2O3(s)的热化学方程式为__________。
(2)分离高炉煤气得到的CO与空气可设计成燃料电池(以KOH溶液为电解液)。写出该电池的负极反应式:__________。
(3)CO2和H2充入一定体积的密闭容器中,在两种温度下发生反应:CO2(g)+3H2(g)CH3OH(g)+H2O(g) 测得CH3OH的物质的量随时间的变化见图1。
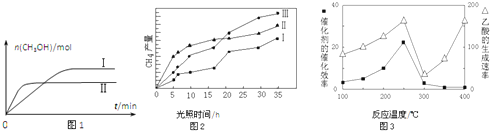
①曲线I、Ⅱ对应的平衡常数大小关系为KⅠ__________KⅡ(填“>”或“=”或“<”).
②一定温度下,在容积相同且固定的两个密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
容 器 | 甲 | 乙 |
反应物投入量 | 1molCO2、3molH2 | a molCO2、b molH2、 |
若甲中平衡后气体的压强为开始的0.8倍,要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则c的取值范围为__________。
(4)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2.紫外光照射时,在不同催化剂(I、II、III)作用下,CH4产量随光照时间的变化见图2.在0~15小时内,CH4的平均生成速率I、II和III从大到小的顺序为__________(填序号).
(5)以TiO2/Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率的关系见图3。
①乙酸的生成速率主要取决于温度影响的范围是__________。
②Cu2Al2O4可溶于稀硝酸,写出有关的离子方程式:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,A处通入潮湿的Cl2,关闭B阀时,C处干燥的红色布条看不到明显现象,打开B阀后,C处红色布条逐渐褪色,则D瓶中装的不可能是( )
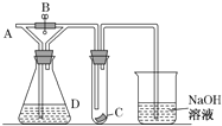
A. 浓H2SO4 B. NaOH溶液 C. 澄清石灰水 D. 饱和NaCl溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com