
【题目】如图所示,A处通入潮湿的Cl2,关闭B阀时,C处干燥的红色布条看不到明显现象,打开B阀后,C处红色布条逐渐褪色,则D瓶中装的不可能是( )
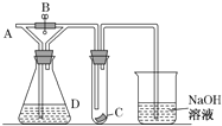
A. 浓H2SO4 B. NaOH溶液 C. 澄清石灰水 D. 饱和NaCl溶液
【答案】D
【解析】
次氯酸具有漂白作用而氯气不具有漂白性,所以干燥的氯气不能漂白有色布条,含水蒸气的氯气能使有色布条褪色,A处通入氯气,关闭B阀时,C处的红色布条看不到明显现象,打开B阀后,C处红色布条逐渐褪色,因此说明D中溶液可以吸收氯气或可干燥氯气,据此分析来解答。
A.浓硫酸具有吸水性,氯气通过浓硫酸得到干燥的氯气,故A与题意不符;
B.氯气通过NaOH溶液,与氢氧化钠反应,关闭B阀时,C处的红色布条看不到明显现象,故B与题意不符;
C.氯气通过澄清石灰水,与氢氧化钙反应,关闭B阀时,C处的红色布条看不到明显现象,故C与题意不符;
D.氯气与食盐水不反应,进入C的为潮湿的氯气,关闭B阀时,C处红色布条逐渐褪色,故D符合题意;
答案选D。


科目:高中化学 来源: 题型:
【题目】香料甲和G在生活中有很多用途,工业上利用有机物A(![]() )来制备,其合成路线如下:
)来制备,其合成路线如下:

已知:R1—CHO+R2—CH2—CHO ![]()
![]() (R1、R2代表烃基或氢原子)
(R1、R2代表烃基或氢原子)
回答下列问题:
(1)C的名称是____,G中官能团的名称是__________。
(2)②的反应类型是________,F的结构简式为_______________。
(3)下列关于C的叙述正确的是___________.
A. 分子式为C9H10O B. 1mol E最多能与5molH2发生加成反应
C. 自身能发生加聚、缩聚反应 D. 最多有9个碳原子位于同一平面
(4)C有多种同分异构体,其中属于芳香族化合物的有____种。
(5)写出反应①的化学方程式__________________________________。
(6)F的同分异构体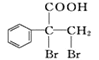 是一种重要的药物中间体,其合成路线与G相似,请以为原料设计它的合成路线(其他所需原料自选)。____________
是一种重要的药物中间体,其合成路线与G相似,请以为原料设计它的合成路线(其他所需原料自选)。____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一块金属钠投入到滴有紫色石蕊试液的盛冷水的烧杯中,甲同学认为可观察到下列现象,其中正确的有( )
①钠投入水中,先沉入水底,后浮出水面
②钠立即与水反应,并有气体产生
③反应后溶液变红
④钠熔成闪亮的小球
⑤小球在水面上四处游动
⑥有“嘶嘶”的响声发出
A. ①②③④ B. ②③④⑤
C. ②④⑤⑥ D. ③④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分析如图所示的四个原电池装置,其中结论正确的是( )

A. ①②中Mg作为负极,③④中Fe作为负极
B. ②中Mg作为正极,电极反应式为6H2O+6e-===6OH-+3H2↑
C. ③中Fe作为负极,电极反应式为Fe-2e-===Fe2+
D. ④中Cu作为正极,电极反应式为2H++2e-===H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,若电解5 min时,测得铜电极的质量增加2.16 g。试回答:

(1)电源中X极是________(填“正”或“负”)极。
(2)通电5 min时,B中共收集到224 mL(标准状况)气体,溶液体积为200 mL(电解前后溶液的体积变化忽略不计),则通电前c(CuSO4)=________。
(3)若A中KCl溶液的体积也是200 mL,电解后溶液中仍有Cl-,则电解后溶液的c(OH-)=________。
(4)二氧化碳是地球温室效应的罪魁祸首,目前人们处理二氧化碳的方法之一是使其与氢气合成为甲醇,甲醇是汽车燃料电池的重要燃料。已知氢气、甲醇燃烧的热化学方程式如下:
2H2(g)+O2(g)===2H2O(l) ΔH=-570 kJ·mol-1 ①
2CH3OH(l)+ 3O2(g)===2CO2(g)+4H2O(l) ΔH=-1452 kJ·mol-1 ②
写出二氧化碳与氢气合成甲醇液体的热化学方程式:_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某化工厂用氯气与石灰乳生产漂白粉,该厂出厂产品说明书如下:

①漂白粉长期露置在空气中会变质,写出漂白粉变质过程中涉及的化学方程式:_____________________________;______________。
②某实验室研究员将完全变质后的漂白粉溶于水,向其中加入足量稀硝酸,收集到标准状况下448 mL气体,则该漂白粉中所含有效成份的质量为___________(假设漂白粉中的其它成份不与硝酸反应)。
(2)将14 g Na2O和Na2O2的混合物加入足量的水中充分反应后,生成标准状况下的气体1.12 L,所得溶液的体积为400 mL。试计算:原混合物中Na2O的质量为___________g,所得溶液中Na+的物质的量为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~E五种物质都含有同一种元素,它们之间的转化关系如图所示,其中A为淡黄色固体化合物,B为单质。请回答下列问题。

(1)固体A的名称为_______________,其常见用途:_______________________________________。(仅举一例即可)
(2)写出下列反应的化学方程式:
①A→C_____________________________________________________________;
②A→D_____________________________________________________________;
③B→A_____________________________________________________________;
④B→C_____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是某品牌饮用矿物质水标签的部分内容。下列说法正确的是

A. 标签上给出的离子的物理量是物质的量浓度
B. 任何饮用水中氯离子(Cl-)的浓度均在10~27.3 mg/L之间
C. 该品牌饮用矿物质水中c(Mg2+)的最大值为2×10-4 mol/L
D. 一瓶该品牌饮用矿物质水中SO42-的物质的量不超过1×10-5 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验需要0.2 mol·L-1 NaCl溶液240 mL,配制流程如下:


回答下列问题:
(1)①中称得________gNaCl。
(2)玻璃棒在②③两步中的作用分别是____________、______________。
(3)某同学在第⑧步观察液面时俯视,所配溶液浓度______(填“偏高”“偏低”或“无影响”)。
(4)容量瓶在使用之前要__________,具体操作是________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com