
����Ŀ�����ӣ�Ni��Cd���ɳ�������ִ��������й㷺Ӧ�ã���֪ij���ӵ�صĵ������ҺΪKOH��Һ����䡢�ŵ簴��ʽ���У�Cd+2NiOOH+2H2O ![]() Cd��OH��2+2Ni��OH��2 �� �йظõ�ص�˵����ȷ���ǣ� ��
Cd��OH��2+2Ni��OH��2 �� �йظõ�ص�˵����ȷ���ǣ� ��
A.���ʱ������Ӧ��Ni��OH��2��e��+OH���TNiOOH+H2O
B.�������ǻ�ѧ��ת��Ϊ���ܵĹ���
C.�ŵ�ʱ����������Һ�ļ��Բ���
D.�ŵ�ʱ�������Һ�е�OH���������ƶ�
���𰸡�A
���������⣺A�����ʱ����װ���ǵ��أ������ϵ缫��ӦʽΪ��Ni��OH��2��e��+OH���TNiOOH+H2O����A��ȷ�� B��������ʵ�����ǰѵ���ת��Ϊ��ѧ�ܵĹ��̣���B����
C���ŵ�ʱ�������ϵ缫��ӦʽΪ��Cd��2e��+2OH��=Cd��OH��2 �� ���Լ��Լ�������C����
D���ŵ�ʱ���������Һ���������������ƶ�����D����
��ѡA��
�ŵ�ʱ�����Ϸ����ĵ缫��ӦʽΪ��Cd��2e��+2OH��=Cd��OH��2 �� �����Ϸ����ĵ缫��ӦʽΪ��NiOOH+e��+H2O�TNi��OH��2+OH�� �� ���ʱ�����Ϸ����ĵ缫��ӦʽΪ��Ni��OH��2+OH����e����NiOOH+H2O�������Ϸ����ĵ缫��ӦʽΪ��Cd��OH��2+2e���TCd+2OH�� �� �ŵ�ʱ����Һ���������������ƶ��������ǰѵ���ת��Ϊ��ѧ�ܵ�װ�ã�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� �� 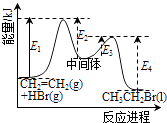
A.����ʽΪC2H4O���л�������������ͬ
B.ͬ��ͬѹ�£�ͬ������κ������������ͬ��ԭ����
C.�ܱ�������1molN2��3molH2��ַ�Ӧ������ķ�����Ϊ 2��6.02��1023
D.������ͼ�������߿�ȷ����Ӧ��CH2=CH2��g��+HBr��g����CH3CH2Br��l���ġ�H=��E1+E3��E2��E4��kJmol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������˳���д������
A.ԭ�Ӱ뾶��O��S��NaB.�ȶ��ԣ�pH3��H2S��NH3
C.���ԣ�H3PO4��H2SO4��HClO4D.���ԣ�Al(OH)3��Mg(OH)2��NaOH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£�������X������Y��0.16mol����10L�����ܱ������У�������ӦX��g��+Y��g��2Z��g������H��0��һ��ʱ���ﵽƽ�⣮��Ӧ�����вⶨ���������±���
t/min | 2 | 4 | 7 | 9 |
n��Y��/mol | 0.12 | 0.11 | 0.10 | 0.10 |
����˵����ȷ���ǣ� ��
A.0��2 min��ƽ������v��Z��=2.0��10��3 molL��1min��1
B.�����������䣬�����¶ȣ���Ӧ�ﵽ��ƽ��ǰ v��������v���棩
C.���¶��´˷�Ӧ��ƽ�ⳣ��K=144
D.�����������䣬�ٳ���0.2 mol Z��ƽ��ʱX�������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. ��״���£�22.4LCCl4�к��е�̼ԭ����Ϊ6.02��1023
B. ���³�ѹ�£�32gO3�к��еķ�����Ϊ2��6.02��1023
C. 1mol��L��1Al2(SO4)3�к��е���������Ϊ2��6.02��10 23
D. 2molCl2������NaOH��ȫ��Ӧ��ת�Ƶ�����Ϊ2��6.02��1023
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һ�ֹ��ɽ���Ԫ�أ�ͨ�������Ͻ���ֵ����Ӽ�������Ԫ�ؿ���ǿ�Ͻ��ǿ�ȡ�Ӳ�ȡ��ɺ��Լ����ԣ�������ǿ�����¼���ʴ���ܣ���ͼ�ǻ����������Ʊ����������Ҫ����ͼ�� 
��1����Ӧ�ٵ�β��������NH3H2O��Һ���պϳɷ��ϣ�д����Ӧ�����ӷ���ʽ ��
��2���������Һ�е���Ҫ�����ӵļ��鷽���� ��
��3�������ʵ����ģ�����1�Ͳ���2������Ҫʹ�õ���Ҫ���������� ��
��4��д����Ӧ�ٵĻ�ѧ����ʽ�� ��
��5����ҵ���Ʊ���ԭ������CO��H2�ķ�Ӧԭ��ΪCO2+CH4 ![]() 2CO+2H2 �� CH4+H2O
2CO+2H2 �� CH4+H2O ![]() CO+3H2 �� �������������Ϊ80%��a L����״������Ȼ��������������̼��ˮ�����Ļ�����ڸ����·�Ӧ������ת����Ϊ90%���ò����Ļ�ԭ�����壨CO��H2����ԭMoO3���⣬�������������������Ϊ ��
CO+3H2 �� �������������Ϊ80%��a L����״������Ȼ��������������̼��ˮ�����Ļ�����ڸ����·�Ӧ������ת����Ϊ90%���ò����Ļ�ԭ�����壨CO��H2����ԭMoO3���⣬�������������������Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2CH4��g��+2NH3��g��+3O2��g��=2HCN��g��+6H2O��g����Ӧ�У���֪v ��HCN��=n mol/��Lmin������v��O2��=m mol/��Lmin������m��n�Ĺ�ϵ��ȷ���ǣ� ��
A.m= ![]() n
n
B.m= ![]() n
n
C.m= ![]() n
n
D.m=2n
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ��������Ҫ����2mol/L��NaCl��Һ950mL������ʱӦѡ�õ�����ƿ�Ĺ��ͳ�ȡ��NaCl�����ֱ��� ( )
A.950mL��11.2gB.500mL��117g
C.1000mL��117.0gD.������111.2g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£���2mol A��3mol B����һ�ܱ������У�������Ӧ��aA��g��+B��g��C��g��+D��g����5min��ﵽƽ�⣮��֪���¶�����ƽ�ⳣ��K=1�����¶Ȳ���ʱ���������������Ϊԭ����10����A��ת���ʲ������仯���� ��
A.a=3
B.a=2
C.B��ת����Ϊ40%
D.B��ת����Ϊ60%
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com