
����Ŀ��һ���¶��£���3molA�����1molB����ͨ��һ�ܱ������У��������·�Ӧ��3A(g)+B(g)![]() xC(g)����д���пհף�
xC(g)����д���пհף�
(1)����������̶�Ϊ2L����Ӧ2minʱ���ʣ��0.6molB��C��Ũ��Ϊ0.4mol/L��
��2min�ڣ�A��ƽ����Ӧ����Ϊ________��x=_______��
������Ӧ��4min�ﵽƽ�⣬ƽ��ʱC��Ũ��__________0.8mol/L������������������������С����![]() ��
��
(2)��ά������ѹǿ���䣺�ﵽƽ��ʱC���������________22%������������������������С����![]() ��
��
���𰸡�0.3mol/(Lmin) 2 С�� ����
��������
(1)�ټ���μӷ�ӦB�����ʵ������ٸ��ݷ���ʽ����μӷ�ӦA�����ʵ���������v=![]() ����v(A)������n=c��V��������C�����ʵ������������ʵ���֮�ȵ��ڻ�ѧ������֮�ȼ���x��
����v(A)������n=c��V��������C�����ʵ������������ʵ���֮�ȵ��ڻ�ѧ������֮�ȼ���x��
�����ŷ�Ӧ�Ľ��У���Ӧ������С������Ӧ��4min�ﵽƽ�⣬��2min��ƽ������С��ǰ2min��ƽ�����ʣ���2min��C��Ũ�ȱ仯С��0.4mol/L��
(2)��ά������ѹǿ���䣬�ж���������仯����ЧΪѹǿ�仯������ƽ���ƶ�����
(1)��Ӧ2minʱ���ʣ��0.6molB����μӷ�Ӧ��B�����ʵ���n(B)=1mol-0.6mol=0.4mol���ɷ���ʽ��֪�μӷ�Ӧ��A�����ʵ���n(A)=0.4mol��3=1.2mol����v(A)=![]() =
=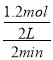 =0.3mol/(Lmin)��C��Ũ��Ϊ0.4mol/L��������C�����ʵ���n(C)=2L��0.4mol/L=0.8mol����0.4mol��0.8mol=1��x����ã�x=2��
=0.3mol/(Lmin)��C��Ũ��Ϊ0.4mol/L��������C�����ʵ���n(C)=2L��0.4mol/L=0.8mol����0.4mol��0.8mol=1��x����ã�x=2��
�����ŷ�Ӧ�Ľ��У���Ӧ������С������Ӧ��4min�ﵽƽ�⣬��2min��ƽ������С��ǰ2min��ƽ�����ʣ�ǰ2min��C��Ũ�ȱ仯Ϊ0.4mol/L�����2min��C��Ũ�ȱ仯С��0.4mol/L����ƽ��ʱC��Ũ��С��0.8mol/L��
(2)��������̶�ʱC���������Ϊ22%�����ڸ÷�Ӧ������Ӧ�����������С�ķ�Ӧ����ά������ѹǿ���䣬��Ӧ��С�������ݻ�����ЧΪ����ѹǿ��������ϵ��ѹǿ����ѧƽ�������������С������Ӧ�����ƶ�����˴ﵽƽ��ʱC�������������22%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС��ģ�ҵ�ϴ���������Ҫ�ɷ���Al2O3����SiO2��Fe2O3�����ʣ�����ȡ�������Ĺ�����ʵ�飬�������£�
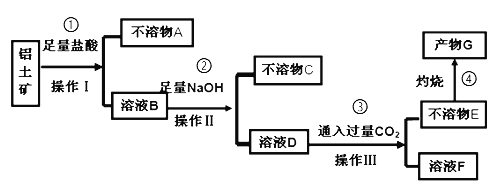
��ش��������⣺
(1)������������Ϊ_________��
(2)��֤��ҺB���Ƿ���Fe3+�ķ�����_______________________________��
(3)������A��_____(�ѧʽ)��д������D��E��Ӧ�����ӷ���ʽ_____________________________��
(4)�������м������NaOH��Һ������Ӧ�����ӷ���ʽ������H++OH��=H2O��Fe3++3OH��=Fe(OH)3������______________________________��
(5)���������10g������������պ�ò�����G����Ϊ5.1g�����ʯ����Ԫ�صĺ���Ϊ_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����淴Ӧ2A(g)��B(g)![]() 2C(g)��2D(g) ��4�ֲ�ͬ����·�Ӧ���ʷֱ����£����з�Ӧ����v������
2C(g)��2D(g) ��4�ֲ�ͬ����·�Ӧ���ʷֱ����£����з�Ӧ����v������
A. v(A)��0.15mol��(L��min) -1B. v (B)��0.2 mol��(L��min) -1
C. v (C)��0.3 mol��(L��min) -1D. v (D)��0.1 mol��(L��min) -1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ����������β���ŷų���SO2��NOx�ȣ����γ���������Ҫ���ء������ɿ����еĻҳ������ᡢ���ᡢ�л�̼�⻯����������γɵ�������
(1)SO2���̳��Ĵ����γ�����ķ�Ӧ����ʽ��_____��
(2)NOx��SO2�ڿ����д�������ƽ�⣺
2NO(g)+O2(g)![]() 2NO2(g) ��H=-113.0kJmol-1
2NO2(g) ��H=-113.0kJmol-1
2SO2(g)+O2(g)![]() 2SO3(g) ��H=-196.6kJmol-1
2SO3(g) ��H=-196.6kJmol-1
SO2ͨ���ڶ��������Ĵ����£���һ��������������SO3��
��д��NO2��SO2��Ӧ���Ȼ�ѧ����ʽΪ_____��
�����¶����ߣ��÷�Ӧ��ѧƽ�ⳣ���仯������____��
(3)���2SO2+O2![]() 2SO3��Ӧ��SO2��ת���ʣ��Ǽ���SO2�ŷŵ���Ч��ʩ��
2SO3��Ӧ��SO2��ת���ʣ��Ǽ���SO2�ŷŵ���Ч��ʩ��
��T�¶�ʱ����1L���ܱ������м���2.0molSO2��1.0molO2��5min��Ӧ�ﵽƽ�⣬���������ת����Ϊ50%���÷�Ӧ��ƽ�ⳣ����___��
���ڢ��������£���Ӧ�ﵽƽ��ı�������������ʹSO2��ת������ߵ���____������ĸ����
a.�¶Ⱥ�����������䣬����1.0molHe
b.�¶Ⱥ�����������䣬����1.0molO2
c.��������������ʱ���������������
d.��������������ʱ�����ø�Ч����
e.��������������ʱ��������ϵ�¶�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йػ�ѧ��Ӧ��������ȷ����(����)
A.SO2��Ba(NO3)2��Ӧ����BaSO3
B.NH3�ڴ�O2��ȼ������NO2
C.����CO2�백ˮ��Ӧ����NH4HCO3
D.����������Fe��ˮ������Ӧ����Fe(OH)3��H2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ������в������������ʵ���(Y)������Լ������ʵ���(X)֮��Ĺ�ϵ��ȷ����(����)
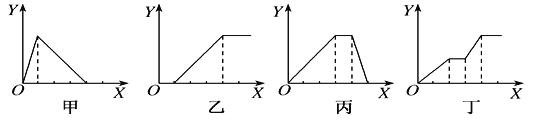
A. ����AlCl3��Һ����μ���NaOH��Һ�������ұߵα���
B. ����NaAlO2��Һ�еμ�ϡ�����������ұߵα���
C. ����NH4Al(SO4)2��Һ����μ���NaOH��Һֱ������
D. ����NaOH��Ba(OH)2��NaAlO2�Ļ����Һ����ͨ��CO2������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ԭ�������������ӵ�ǰ�����ڵ�����Ԫ��A~H���й��������£�
Ԫ�ش��� | A | B | C | D | E | F | G | H |
ԭ�Ӱ뾶/nm | 0.037 | 0.074 | 0.073 | 0.071 | 0.143 | 0.102 | 0.099 | 0.114 |
��Ҫ���ϼ� | +1 | +5����3 | ��2 | ��1 | +4����4 | +6����2 | +7����1 | +7����1 |
��֪E�ĵ�����һ�ֳ����İ뵼����ϣ������������ݣ�����Ӧ�Ļ�ѧʽ�ش��й����⣺
��1��Ԫ��A��C��ԭ�Ӹ�����Ϊ1:1�Ļ�����ĵ���ʽΪ_______��
��2��Ԫ��B��C��D�ĵ�һ�������ɴ�С��˳��Ϊ_______
��3��Ԫ��C��F�γɵ�������FC32-�ռ乹��Ϊ_______
��4��Ԫ��G��H����̬�⻯����ȶ�����ǿ����˳��Ϊ________
��5��Ԫ��C��F����̬�⻯��е��ɸߵ��͵�˳��Ϊ______��ԭ����______
��6��Ԫ��E���⻯�EH4������_______����(���������������Ǽ�����)
��7�����Ļ�̬ԭ�Ӽ۵����Ų�ʽΪ______��
��8������[H2NCONH2]�����У�Cԭ�ӵ��ӻ���ʽΪ____��1mol���ط����У���������ĿΪ______��
��9�����������ᾧˮ���Ȼ��������ٻ�ɫ�ľ��壬�仯ѧʽΪ[Fe(H2O)6]Cl3���û������У���Fe3+�γ���λ����ԭ����______��д��H2O��һ�������ӵĵȵ�����______
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����ʱ��0.1mol��L��1ijһԪ��HA�ĵ���ƽ�ⳣ��ԼΪ1��10��7����������������ǣ� ��
A. ����Һ��pH��4
B. ����Һ�У�HAԼ��0.1%��������
C. ��ˮϡ�ͣ�HA�ĵ���ƽ�������ƶ���HA�ĵ���ƽ�ⳣ������
D. ��HA�������c(H��)ԼΪˮ�������c(H��)��106��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������װ���ܴﵽʵ��Ŀ�ĵ���
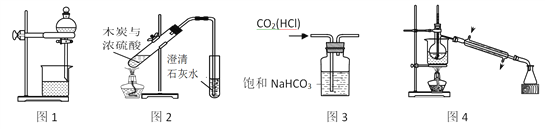
A. ͼ1���ڷ���ƾ���ˮ
B. ͼ2������֤ľ̿��Ũ����ķ�Ӧ�����к���CO2
C. ͼ3���ڳ�ȥCO2�е�����HCl
D. ͼ4�����Ʊ�����ˮ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com