
【题目】(1)常温时,将浓度为m molL﹣1的CH3COOH溶液和n molL﹣1 NaOH溶液等体积混合,混合后溶液的pH=7,m与n的大小关系是m____ n(填“>”、“<”或“=”,下同);若将pH=2的CH3COOH溶液和pH=12的NaOH溶液等体积混合,混合溶液的pH______ 7。
(2)消防用的泡沫灭火器内装的药品是硫酸铝溶液和碳酸氢钠溶液,用离子方程式表示二者混合时发生的反应_________________.
(3)常温下某强酸溶液pH=a,强碱溶液pH=b,已知a+b=12,酸碱溶液混合pH=7,则酸溶液体积V1和碱溶液体积V2的关系为_________.
(4)常温时Ksp[Cu(OH)2]=2.2×10﹣20,将Cu(OH)2溶于2.2mol/L CuCl2溶液中形成平衡溶液的pH为____.
(5)物质的量浓度相同的下列溶液①(NH4)2CO3②(NH4)2SO4③NH4HCO3④NH4HSO4⑤NH4Cl⑥NH3H2O,c(NH4+)由小到大的排列顺序是___________(填序号)。
【答案】 > < Al3++3HCO3﹣=Al(OH)3↓+3CO2↑ V2=102V1 4 ⑥③⑤④①②
【解析】(1)由于醋酸钠水解溶液显碱性,如果要显中性,则醋酸一定过量,因此m>n;若将pH=2的CH3COOH溶液和pH=12的NaOH溶液等体积混合,醋酸一定过量,则混合溶液的pH<7。(2)硫酸铝溶液和碳酸氢钠溶液混合水解相互促进产生二氧化碳,离子方程式为Al3++3HCO3﹣=Al(OH)3↓+3CO2↑;(3)混合后显中性,则V1×10-a=V2×10b-14,解得V2=100V1;(4)溶液中铜离子浓度是2.2mol/L,则根据氢氧化铜的溶度积常数可知溶液中氢氧根浓度![]() ,因此pH=4。(5)NH3H2O是弱电解质,电离程度很小,故溶液中c(NH4+)小于所有铵盐的c(NH4+),即一水合氨溶液中铵根离子浓度最小;③④⑤中铵根离子系数都是1,碳酸氢根离子促进铵根离子水解,氢离子抑制铵根离子水解;①②中铵根离子系数都是2,其溶液中铵根离子浓度大于其余溶液中铵根离子浓度,碳酸根离子促进铵根离子水解,则溶液c(NH4+)由小到大的排列顺序是 ⑥<③<⑤<④<①<②。
,因此pH=4。(5)NH3H2O是弱电解质,电离程度很小,故溶液中c(NH4+)小于所有铵盐的c(NH4+),即一水合氨溶液中铵根离子浓度最小;③④⑤中铵根离子系数都是1,碳酸氢根离子促进铵根离子水解,氢离子抑制铵根离子水解;①②中铵根离子系数都是2,其溶液中铵根离子浓度大于其余溶液中铵根离子浓度,碳酸根离子促进铵根离子水解,则溶液c(NH4+)由小到大的排列顺序是 ⑥<③<⑤<④<①<②。


科目:高中化学 来源: 题型:
【题目】某同学设计如下实验方案,以分离KNO3和Ba(NO3)2两种固体混合物,试回答下列问题:

供选试剂:Na2SO4溶液、K2CO3溶液、K2SO4溶液、盐酸、硫酸、硝酸。
(1)试剂a是____________,加入试剂 b所发生反应的离子方程式为______________________。
(2)该方案能否达到实验目的:______________________。(填“能”或“不能”)。若不能, 应如何改进?______________________________________________(若能,此问不用回答)。
(3)若要测定原混合物中 Ba(NO3)2的质量分数,除了要准确称量混合物的质量外至少还要获得的数据是___________的质量。
(4)用所制备的KNO3固体配制0.1mol/KNO3溶液450mL,回答下列问题:
①配制过程中需要用到的玻璃仪器有烧杯、玻璃棒,量筒、胶头滴管、___________;
②需要用托盘天平称量___________gKNO3固体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列反应框图填空。已知反应①是工业上生产化合物D的反应,反应⑤是实验室检验化合物E的反应。

(1)单质L是________;化合物A是________。
(2)图中除反应①以外,还有两个用于工业生产的反应,是________和________(填代号)。它们反应的化学方程式分别是:______________________和_____________________。
(3)E和K、J混合溶液反应的化学方程式为____________________。此反应的发生说明了_____________________________________________________________________。
(4)把K、J混合固体放入少量浓盐酸中,则其反应的现象是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将下图所示实验装置的 K 闭合,下列判断正确的是

A. Cu电极上发生还原反应 B. 电子沿 Zn→a→b→Cu路径流动
C. 片刻后甲池中c(SO![]() )增大 D. 片刻后可观察到滤纸b点变红色
)增大 D. 片刻后可观察到滤纸b点变红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高分子材料PET聚酯树脂和PMMA的合成路线如下:

已知:
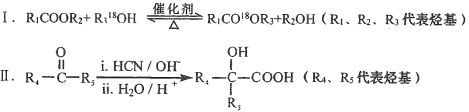
(1)①的反应类型是_______________。
(2)②的化学方程式为_______________。
(3)PMMA单体的官能团名称是________________________________________________。
(4)F的核磁共振氢谱显示只有一组峰,⑤的化学方程式为_________________。
(5)G的结构简式为_________________________。
(6)下列说法正确的是_____________(填字母序号)。
a.⑦为酯化反应
b.B和D互为同系物
c.1 mol  与足量NaOH溶液反应时,最多消耗4 mol NaOH
与足量NaOH溶液反应时,最多消耗4 mol NaOH
(7)J的某种同分异构体与J具有相同官能团,且为顺式结构,其结构简式是_______。
(8)写出由PET单体制备PET聚酯并生成B的化学方程式_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2和I2在一定条件下能发生反应:H2(g)+I2(g)![]() 2HI(g)△H=-a kJmol-1。
2HI(g)△H=-a kJmol-1。
已知:

下列说法正确的是( )
A. 该反应为吸热反应
B. 断开2 mol HI分子中的化学键所需能量约为(c+b+a)kJ
C. 反应物的总能量低于生成物的总能量
D. 向密闭容器中加入2 mol H2(g)和2 mol I2(g),充分反应后放出的热量为2a kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于Na2CO3和NaHCO3的说法中,不正确的是
A. 均属于盐
B. 焰色反应均为黄色
C. 可以用加热的方法除去Na2CO3固体中的NaHCO3杂质
D. 物质的量相同的两种固体分别与足量盐酸反应,Na2CO3产生的二氧化碳多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某NaCl溶液样品中含有Na2SO4、CaCl2杂质(该溶液用X表示)。除去杂质的实验方案如下:

(1)B溶液中存在的阳离子有_________,阴离子有_________。
(2)C中所含物质的化学式是_________。
(3)D中加入适量盐酸后,大量减少的微粒有__________。
(4)①和②不能调换顺序的理由是__________。
(5)某同学认为可将上方案进行改进:①加入过量BaCO3 ②加入适量盐酸,即可达到除杂的目的,而且步骤更为简便。请评价这种方法是否正确______,说明理由_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲同学通过查询资料知道,一定浓度的硝酸与镁反应时,可得到二氧化氮、一氧化氮、氮气三种气体。该同学用下列仪器组装装置来直接验证有二氧化氮、一氧化氮生成并制取氮化镁 (假设实验中每步转化均是完全的) 。查阅文献得知:
①二氧化氮沸点为21.1 ℃、熔点为-11 ℃,一氧化氮沸点为-151 ℃、熔点为-164 ℃;
②镁也能与二氧化碳反应;
③氮化镁遇水反应生成氢氧化镁和氨气。

(1)实验中先打开开关K,通过导管向装置内通入二氧化碳气体以排出装置内的空气,停止通入二氧化碳的标志是________________________________。
(2)为实现上述实验目的,所选用的仪器的正确连接方式是A→____________→E,确定还原产物中有二氧化氮的现象是______________________________________,实验中要多次使用装置F,第二次使用F的目的是______________________________________________。
(3)实验过程中,发现在D中产生预期现象的同时,C中溶液颜色慢慢褪去,试写出C中反应的离子方程式:________________________________。
(4)甲同学在A中开始反应时,马上点燃B处的酒精灯,实验结束后通过测试发现B处的产品纯度不高,原因是______________________________________。
(5)设计一种实验方案,验证镁与硝酸反应时确实有氮气生成:__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com