
【题目】根据如图所示的实验回答问题。
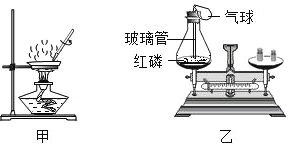
(1)甲为蒸发溶液的实验。加热时若不搅拌,造成的后果是________;当观察到________时,停止加热。
(2)乙为通过红磷燃烧前后质量的测定验证质量守恒定律的实验。用红热玻璃管引燃红磷,实验现象是红磷燃烧,产生________,放出大量热。实验中气球的作用除了使装置密闭之外,还可以防止________;实验时若取用红磷的量不足,对实验的结果________ (选填“有”或“没有”)影响。
(3)用图1装置进行实验,先后将溶液快速全部推入,测得一段时间内压强变化如图2所示。
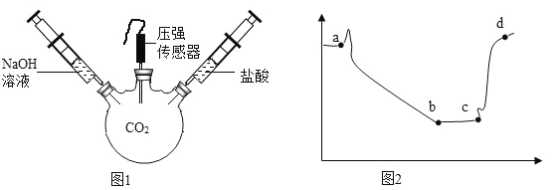
①先推入的溶液是________
②be段压强不变,原因是________
③cd段压强变大,用化学方程式解释:________
【答案】液体飞溅 蒸发皿中出现较多固体 白烟 瓶塞飞出 没有 氢氧化钠溶液 氢氧化钠溶液与二氧化碳充分反应,反应停止 Na2CO3+2HCl═2NaCl+H2O+CO2↑
【解析】
化学反应遵循质量守恒定律,即参加反应的物质的质量之和,等于反应后生成的物质的质量之和,是因为化学反应前后,元素的种类不变,原子的种类、总个数不变,据此分析第(1)和(2)问。
(3)根据二氧化碳与氢氧化钠溶液反应生成碳酸钠和水,使压强减小,碳酸钠溶液与稀盐酸反应生成氯化钠、水和二氧化碳,使压强增大,进行分析解答。
(1)甲为蒸发溶液的实验,加热时若不搅拌,造成的后果是液体飞溅;当观察到蒸发皿中出现较多固体时,停止加热,故答案为:液体飞溅;蒸发皿中出现较多固体;
(2)红磷燃烧,产生白烟,放出大量热;实验中气球的作用除了使装置密闭之外,还可以防止瓶塞飞出;实验时若取用红磷的量不足,对实验的结果没有影响,这是因为无论红磷是否完全反应,天平都保持平衡,故答案为:白烟;瓶塞飞出;没有;
(3)①由一段时间内压强变化图,压强先减小,先推入的溶液是氢氧化钠溶液;
②bc段压强不变,原因是氢氧化钠溶液与二氧化碳充分反应,反应停止;
③cd段压强变大,是因为碳酸钠溶液与稀盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑。


 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,根据表中序号对应元素回答有关问题:
族 周期 | IA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
4 | ⑨ | ⑩ |
(1)表中元素,化学性质最不活泼的是___,只有负价而无正价的是___,原子半径最大的是___;(填写元素符号);
(2)表中能形成两性氢氧化物的元素是___(填元素符号),分别写出该元素的氢氧化物与⑥、⑨的最高价氧化物对应水化物反应的离子方程式分别是___、___。
(3)元素①组成的单质的电子式为___;用电子式表示⑥的氢化物的形成过程___。
(4)②和③的单质加热时反应生成物质X,其化学式为___,该物质中含有的化学键的类型为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计的微型实验装置验证SO2的性质,通过分析实验,下列结论表达正确的是
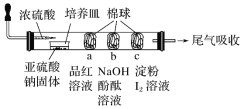
A. a棉球褪色,验证SO2具有氧化性
B. b棉球褪色,验证SO2具有酸性氧化物的通性
C. c棉球蓝色褪去,验证SO2漂白性
D. 可以使用浓硫酸吸收尾气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲和乙在一定条件下反应生成丙和丁。下列结论正确的是
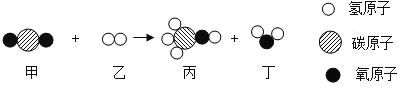
A.丙的相对分子质量为32gB.丙中C、H、O元素质量比为3:1:4
C.生成的丙和丁的分子个数比为2:1D.该反应为置换反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用铝土矿(主要成分为Al2O3,含Fe2O3杂质)为原料冶炼铝的工艺流程如下:
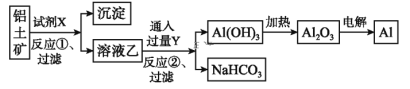
下列叙述正确的是( )
A. 试剂X可以是氢氧化钠溶液,也可以是盐酸
B. 反应①过滤后所得沉淀为氢氧化铁
C. 图中所示转化反应都不是氧化还原反应
D. 反应②的化学方程式为NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() (b)、
(b)、![]() (d)、
(d)、![]() (p)的分子式均为C6H6,下列说法正确的是( )
(p)的分子式均为C6H6,下列说法正确的是( )
A. b的同分异构体只有d和p两种
B. b、d、p中只有b的所有原子处于同一平面
C. b、d、p均可与酸性高锰酸钾溶液反应
D. b、d、p的二氯代物均只有三种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将a克Fe2O3、Al2O3样品溶解在过量的200mL pH=1的硫酸溶液中,然后向其中加入NaOH 溶液使Fe3+、Al3+刚好完全沉淀,用去NaOH 溶液100 mL,则NaOH 溶液的浓度为
A. 0.1 mol/LB. 0.2 mol/LC. 0.4 mol/LD. 0.8 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构见下图,电池总反应可表示为2H2+O2==2H2O,下列有关说法正确的是()

A. 电子通过外电路从b极流向a极
B. b极上的电极反应式为:O2+2H2O+4e-=4OH-
C. 每转移0.1 mol电子,便消耗1.12 升的H2
D. H+由a极通过固体酸电解质传递到b极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒容密闭容器中,用铜铬的氧化物作催化剂,用一定量的HCl(g)和O2制取Cl2的原理为:4HCl(g)+O2(g) ![]() 2Cl2(g)+2H2O(g) ΔH<0。下列有关说法不正确的是
2Cl2(g)+2H2O(g) ΔH<0。下列有关说法不正确的是
A. 平衡前,随着反应的进行,容器内压强变小
B. 平衡时,其他条件不变,分离出H2O(g),逆反应速率减小
C. 平衡时,其他条件不变,升高温度平衡常数增大
D. 其他条件不变,使用不同催化剂,HCl(g)的转化率不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com