
【题目】1,6-己二酸是合成高分子化合物尼龙的重要原料之一,可用六个碳原子的化合物氧化制备。如图是合成尼龙的反应流程:
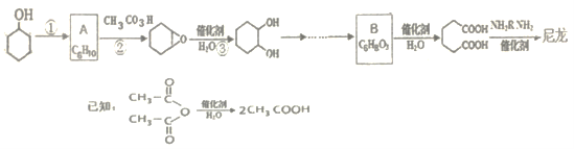
完成下列填空:
(1)写出反应类型:反应①_____反应②_______。
(2)A和B的结构简式为_______、_______。
(3)由![]() 合成尼龙的化学方程式为___。
合成尼龙的化学方程式为___。
(4)由A通过两步制备1,3-环己二烯的合成线路为:_______。
【答案】消去反应 加成(氧化)反应 ![]()
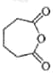 n
n![]() +NH2RNH2
+NH2RNH2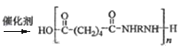 +(2n-1)H2O
+(2n-1)H2O 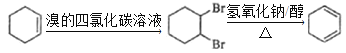
【解析】
根据A的分子式可知,A中含1个不饱和度,因此可推出A为环己烯,其结构简式为:![]() ,它是通过环己醇通过消去反应而得到,A经过氧化得到
,它是通过环己醇通过消去反应而得到,A经过氧化得到![]() ,
,![]() 与水在催化剂作用下生成
与水在催化剂作用下生成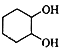 ;根据已知信息,结合B在水的催化作用下生成
;根据已知信息,结合B在水的催化作用下生成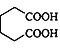 ,采用逆合成分析法可知B应为
,采用逆合成分析法可知B应为 其分子式正好为C6H8O3;最后
其分子式正好为C6H8O3;最后 经过缩聚反应合成尼龙,据此分析作答。
经过缩聚反应合成尼龙,据此分析作答。
根据上述分析可知,
(1)反应①的反应类型为:消去反应;反应②为加氧氧化过程,其反应类型为加成(氧化)反应,故答案为:消去反应;加成(氧化)反应;
(2)根据上述分析可知,A的结构简式为:![]() ;B的结构简式为:
;B的结构简式为: ,故答案为:
,故答案为:![]() ;
; ;
;
(3) 与NH2RNH2发生缩聚反应生成尼龙,其化学方程式为:n
与NH2RNH2发生缩聚反应生成尼龙,其化学方程式为:n![]() +NH2RNH2
+NH2RNH2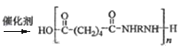 +(2n-1)H2O;
+(2n-1)H2O;
(4)A为![]() ,若想制备1,3-环己二烯,可先与溴的四氯化碳溶液发生加成反应生成1,2—二溴环己烷,1,2—二溴环己烷再在氢氧化钠乙醇溶液、加热的条件下发生消去反应生成1,3﹣环己二烯,其具体合成路线如下:
,若想制备1,3-环己二烯,可先与溴的四氯化碳溶液发生加成反应生成1,2—二溴环己烷,1,2—二溴环己烷再在氢氧化钠乙醇溶液、加热的条件下发生消去反应生成1,3﹣环己二烯,其具体合成路线如下: 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】(1)下列说法正确的是___________
A.化学反应的实质就是旧化学键的断裂,新化学键的形成,在化学反应中,反应物转化为生成物的同时,必然伴随着能量的变化
B.钢铁生锈腐蚀时,铁被氧化
C.放热反应发生时,不一定要加热。但吸热反应必须要加热才能发生
(2)在 101 kPa 时,2g H2完全燃烧生成液态水,放出285.8kJ 热量,氢气燃烧的热化学方程式表示为___________________________;
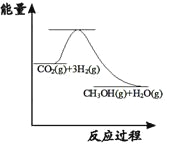
(3)目前工业上有一种方法是用CO2来生产甲醇:CO2(g)+3H2(g)![]() CH3OH(g) +H2O(g);
CH3OH(g) +H2O(g);
下图表示该反应进行过程中能量的变化。(单位为:kJ·mol-1)该反应是___________(填“吸热”或“放热”)反应。ΔH__________0(填“>”或“<”)。
(4)比较下面各组热化学方程式,ΔH1<ΔH2的是________。
A.2H2(g)+O2(g)=2H2O(g)ΔH1;2H2(g)+O2(g)=2H2O(1)ΔH2
B.S(g)+O2(g)=SO2(g)ΔH1;S(s)+O2(g)=SO2(g)ΔH2
C.C(s)+1/2O2(g)=CO(g)ΔH1;C(s)+O2(g)=CO2(g)ΔH2
D.H2(g)+Cl2(g)=2HCl(g)ΔH1;1/2H2(g)+1/2Cl2(g)=HCl(g)ΔH2
(5)101 kPa条件下,14g N2和3g H2反应生成NH3的能量变化如下图示意:
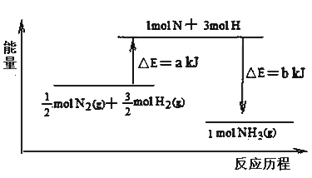
又已知:①已知b=1173;②25 ℃、101 kPa下N2(g)+3H2(g)![]() 2 NH3(g) ΔH =-92 kJ·mol-1则a =_________________。
2 NH3(g) ΔH =-92 kJ·mol-1则a =_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制 100 mL 1.00 mol/L NaCl 溶液,下列说法正确的是( )
A.将所需量的 NaCl 溶于 100 mL 水中
B.将所需量的 NaCl 溶于少量水中,再加水定容到 100 mL
C.将所需量的 NaCl 直接放入容量瓶中,加水定容到 100 mL
D.定容时俯视读刻度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请完成实验室制取蒸馏水的相关内容(装置图见图 1)
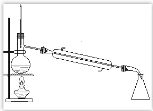
图 1
(1)蒸馏的原理:利用_____不同除去液体混合物中难挥发或不挥发的杂质。
(2)为了避免加热时液体发生暴沸现象,可以在蒸馏烧瓶里加入少量_____。
(3)冷凝管套管下端的开口用橡皮管与自来水龙头相连接,上端开口接上橡皮管后通到水 槽下水道里。即:冷却水从_____进,从_____出。
(4)温度计下端水银球应置于_____处。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对甲烷和CO2的高效利用不仅能缓解大气变暖,而且对日益枯竭的石油资源也有一定的补充作用,甲烷临氧耦合CO2重整反应有:
反应(i):2CH4(g)+O2(g)![]() 2CO(g)+4H2(g) △H=-71.4kJmol-1
2CO(g)+4H2(g) △H=-71.4kJmol-1
反应(ii):CH4(g)+CO2(g)![]() 2CO(g)+2H2(g) △H=+247.0 kJmol-1
2CO(g)+2H2(g) △H=+247.0 kJmol-1
(1)写出表示CO燃烧热的热化学方程式:_______________________________。
(2)在两个体积均为2L的恒容密闭容器中,起始时按表中相应的量加入物质,在相同温度下进行反应(ii):CH4(g)+CO2(g)![]() 2CO(g)+2H2(g) (不发生其它反应),CO2的平衡转化率如下表所示:
2CO(g)+2H2(g) (不发生其它反应),CO2的平衡转化率如下表所示:
容器 | 起始物质的量(n) / mol | CO2的 平衡转化率 | |||
CH4 | CO2 | CO | H2 | ||
Ⅰ | 0.1 | 0.1 | 0 | 0 | 50% |
Ⅱ | 0.1 | 0.1 | 0.2 | 0.2 | / |
①下列能说明反应达到平衡状态是_________。
A.v正(CH4) =2v逆(CO)
B.容器内各物质的浓度满足c(CH4)·c(CO2)=c2(CO)·c2(H2)
C.容器内混合气体的总压强不再变化
D.容器内混合气体密度保持不变
②若容器Ⅰ内反应从开始到平衡所用的时间为t min,则t min内该反应的平均反应速率为:v(H2) = ________(用含t的表达式表示)。
③达到平衡时,容器Ⅰ、Ⅱ内CO的物质的量的关系满足:2n(CO)Ⅰ_______n(CO)Ⅱ(填“>”、“=”或“<”)
(3)将CH4(g)和O2(g)以物质的量比为4:3充入盛有催化剂的恒容密闭容器内,发生上述反应(i):2CH4(g)+O2(g)![]() 2CO(g)+4H2(g),相同时间段内测得CO的体积分数[ψ(CO)]与温度(T)的关系如图如示。
2CO(g)+4H2(g),相同时间段内测得CO的体积分数[ψ(CO)]与温度(T)的关系如图如示。
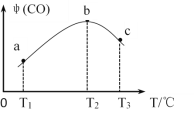
① T2℃时,CO体积分数最大的原因是_____________。
②若T2℃时,容器内起始压强为P0,平衡时CO的体积分数为20%,则反应的平衡常数KP =_______(用平衡分压强代替平衡浓度计算,分压=总压×物质的量分数)。
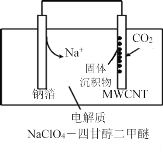
(4)2016年我国科研人员根据反应Na+CO2→ Na2CO3+C(未配平) 研制出一种室温“可呼吸”Na-CO2电池。放电时该电池“吸入”CO2,充电时“呼出”CO2。其放电时的工作原理如图所示,已知吸收的全部CO2中,有![]() 转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面,写出放电时正极的电极反应式:_________________。
转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面,写出放电时正极的电极反应式:_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图1是课本“还原铁粉与水蒸气反应”的实验装置图。
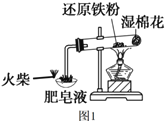
(1)铁粉与水蒸气反应的化学方程式是___。
(2)证明还原铁粉与水蒸气发生了反应的现象是___。
某同学设计图2装置进行“铁与水蒸气反应”的实验。(图中部分夹持及尾气处理装置略)
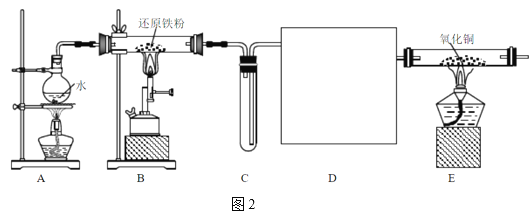
(3)图1装置中湿棉花的作用与图2中___(填“A、B、C、D、E”)装置的作用一样。
(4)装置D的作用是干燥氢气,请在方框内补充完整的装置和试剂___。
(5)实验结束,该同学取反应后装置B中固体混合物溶于足量稀硫酸,再向其中滴加几滴KSCN溶液,振荡,未见溶液变红,得出结论“反应后装置B中固体混合物”不含Fe3O4。你认为正确吗?为什么?你认为___,理由是___。
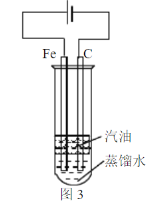
(6)某同学为实现“常温下铁与液态水的反应”设计了图3装置。实验中发现碳棒上冒气泡,蒸馏水中出现白色沉淀。书写该实验发生的化学方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硒(Se)是人体健康必需的一种微量元素,已知Se的原子结构示意图如图:下列说法不正确的是

A. 该原子的质量数为34
B. 该元素处于第四周期第ⅥA族
C. SeO2既有氧化性又有还原性
D. 酸性:H2SO4>H2SeO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由两种或两种以上金属离子(或铵根离子)和一种酸根离子构成的盐称为复盐。为确定某复盐结晶水合物Q(含有两种金属阳离子)的组成,甲、乙两位同学分别进行了如下实验:
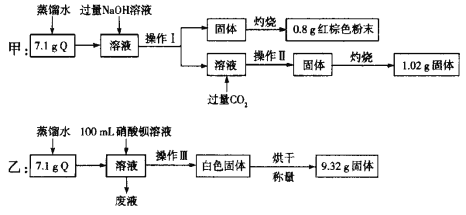
请回答下列问题:
(1)操作Ⅰ、Ⅱ、Ⅲ相同,为__________、洗涤,仅由甲的实验能不能确定操作Ⅰ中所得固体的成分?__________(填“能”或“不能”),说明理由:_________。
(2)甲实验中通入过量二氧化碳发生反应生成沉淀的离子方程式为_______。
(3)0.8 g红棕色粉末的物质的量为__________。
(4)乙实验中,若100 mL硝酸钡溶液恰好完全反应,则硝酸钡溶液的物质的量浓度为__________。
(5)Q的化学式为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com