
【题目】请完成实验室制取蒸馏水的相关内容(装置图见图 1)
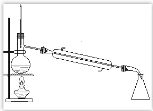
图 1
(1)蒸馏的原理:利用_____不同除去液体混合物中难挥发或不挥发的杂质。
(2)为了避免加热时液体发生暴沸现象,可以在蒸馏烧瓶里加入少量_____。
(3)冷凝管套管下端的开口用橡皮管与自来水龙头相连接,上端开口接上橡皮管后通到水 槽下水道里。即:冷却水从_____进,从_____出。
(4)温度计下端水银球应置于_____处。
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:
【题目】一定温度范围内用氯化钠熔浸钾长石(主要成份为KAlSi3O8)可制得氯化钾,主要反应是:NaCl(l)+KAlSi3O8(s) ![]() KCl(l)+NaAlSi3O8(s),完成下列填空:
KCl(l)+NaAlSi3O8(s),完成下列填空:
(1)上述反应涉及的第三周期元素中,离子半径最小的是___;Cl原子与Si原子可构成有5个原子核的分子,其分子的空间构型为____。
(2)用最详尽描述核外电子运动状态的方式,表示氧离子核外电子的运动状态_____。
(3)Na和O2反应形成Na2O和Na2O2的混合物,阴阳离子的个数比为__;NaAlSi3O8改写成氧化物形式是___。
(4)某兴趣小组为研究上述反应中钾元素的熔出率(液体中钾元素的质量占样品质量分数)与温度的关系,进行实验(保持其它条件不变),获得如下数据:
1.5 | 2.5 | 3.0 | 3.5 | 4.0 | |
800℃ | 0.054 | 0.091 | 0.127 | 0.149 | 0.165 |
830℃ | 0.481 | 0.575 | 0.626 | 0.669 | 0.685 |
860℃ | 0.515 | 0.624 | 0.671 | 0.690 | 0.689 |
950℃ | 0.669 | 0.711 | 0.713 | 0.714 | 0.714 |
分析数据可以得出,氯化钠熔浸钾长石是__________反应(填“放热”或“吸热”);在950℃时,欲提高熔出钾的速率可以采取的一种措施是_______。
(5)Na(l)+KCl(l) ![]() NaCl(l)+K(g)是工业上冶炼金属钾常用的方法,该方法可行的原因是___。
NaCl(l)+K(g)是工业上冶炼金属钾常用的方法,该方法可行的原因是___。
(6)铝可用于冶炼难熔金属,利用铝的亲氧性,还可用于制取耐高温的金属陶瓷。例如将铝粉、石墨和二氧化钛按一定比例混合均匀,涂在金属表面上,然后在高温下煅烧,可在金属表面形成耐高温的涂层TiC,该反应的化学方程式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出表示含有8个质子、10个中子的原子的符号__________。
(2)画出Si原子的原子结构示意图 ________________________。
(3)写出H2O的电子式 ________
(4)第34号元素在元素周期表中的位置____________、____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用可溶性钡盐检验 SO![]() 离子的存在时,先在待测溶液中加入盐酸,其作用是( )
离子的存在时,先在待测溶液中加入盐酸,其作用是( )
A.形成较多的白色沉淀
B.形成的沉淀纯度更高
C.排除 SO![]() 以外的其它阴离子及 Ag+的干扰
以外的其它阴离子及 Ag+的干扰
D.排除 Ba2+以外的其它阳离子的干扰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,相同体积、相同pH的氨水和氢氧化钠溶液加水稀释时的pH变化曲线如下图所示,下列判断正确的是
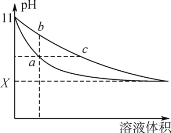
A. b点溶液导电能力比a点溶液强
B. 对于b、c两点,电离平衡常数Kb>Kc
C. 与盐酸完全反应时,消耗盐酸体积:Va>Vc
D. X的值接近7,但大于7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1,6-己二酸是合成高分子化合物尼龙的重要原料之一,可用六个碳原子的化合物氧化制备。如图是合成尼龙的反应流程:
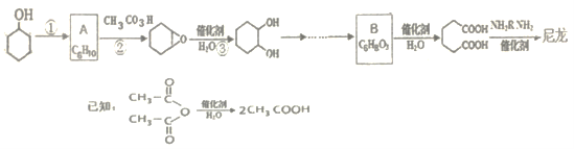
完成下列填空:
(1)写出反应类型:反应①_____反应②_______。
(2)A和B的结构简式为_______、_______。
(3)由![]() 合成尼龙的化学方程式为___。
合成尼龙的化学方程式为___。
(4)由A通过两步制备1,3-环己二烯的合成线路为:_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)用O2将HCl转化为Cl2,可提高效益、减少污染。新型RuO2催化剂对上述HCl转化为Cl2的总反应具有更好的催化活性。
①实验测得在一定压强下,总反应的HCl平衡转化率随温度变化的αHCl~T曲线如图,则总反应的ΔH__0(填“>”、“=”或“<”);A、B两点的反应速率中较大的是__。
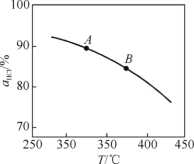
②下列措施有利于提高αHCl的有____(填字母)。
A.增大n(HCl) B. 增大n(O2)
C. 使用更好的催化剂 D. 移去H2O
(2)乙苯催化脱氢制苯乙烯反应:![]() +H2(g),工业上,通常在乙苯蒸气中掺混水蒸气(原料气中乙苯和水蒸气的物质的量之比为1∶9),控制反应温度600 ℃,并保持体系总压为常压的条件下进行反应。在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了H2以外的产物中苯乙烯的物质的量分数)示意图如图。
+H2(g),工业上,通常在乙苯蒸气中掺混水蒸气(原料气中乙苯和水蒸气的物质的量之比为1∶9),控制反应温度600 ℃,并保持体系总压为常压的条件下进行反应。在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了H2以外的产物中苯乙烯的物质的量分数)示意图如图。
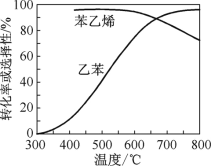
①掺入水蒸气能提高乙苯的平衡转化率,解释说明该事实:_________。
②控制反应温度为600 ℃的理由是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组在实验室用下图所示装置快速制取氨并验证氨的某些性质,同时收集少量纯净的氮气,请回答。
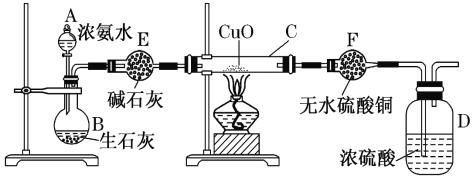
(1)写出用生石灰和浓氨水反应制氨的化学方程式____________________________,解释放出NH3的原因_______________________________________________________。
(2)实验进行一段时间,观察到硬质玻璃管内黑色氧化铜粉末变为红色,盛无水硫酸铜的干燥管内出现蓝色,并且在最后的出气导管口处收集到纯净、干燥的氮气。根据这些现象,写出在硬质玻璃管内发生反应的化学方程式:___________________________________,
(3)在最后的出气导管口处收集干燥、纯净的氮气,收集方法是________。
A.排空气法 B.排水法 C.用气囊收集
(4) E中的碱石灰________(填“能”或“不能”)换成CaCl2。
(5) 在浓硝酸中放入铜片,若铜有剩余,开始反应的化学方程式为 __________________,
(6) 若将12.8 g铜跟一定量的浓硝酸反应,铜消耗完时,共产生NO和NO2 气体V L(标准状况),将产生的气体与一定量的氧气混合恰好被一定量的NaOH溶液吸收生成硝酸盐,则通入氧气的物质的量是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾是一种新型、高效、多功能水处理剂,工业上采用向KOH溶液中通入氯气,然后再加入![]() 溶液的方法制备
溶液的方法制备![]() ,发生反应:
,发生反应:
①![]() (未配平);
(未配平);
②![]() 。
。
下列说法正确的是
A.若反应①中![]() ,则氧化剂与还原剂的物质的量之比为2:1
,则氧化剂与还原剂的物质的量之比为2:1
B.反应①中每消耗4 mol KOH,吸收标准状况下![]()
C.氧化性:![]()
D.若反应①的氧化产物只有KClO,则得到![]() 时消耗
时消耗![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com