
【题目】柠檬酸(用H3R表示)是一种高效除垢剂。常温时,用一定浓度的柠檬酸溶液去除水垢,溶液中H3R、H2R-、HR2-、R3-的物质的量百分数随pH的变化如图所示。下列说法正确的是
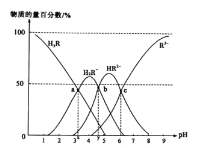
A.由a点判断H3R的第一步电离常数Ka1(H3R)的数量级为10-3
B.若b点溶液中金属阳离子只有Na+,则有c(Na+)=c(R3-)+c(HR2-)+c(H2R-)+c(H3R)
C.pH=6时,c(R3-)=c(HR2-)>c(H+)>c(OH-)
D.反应2H2R-![]() H3R+HR2-在该温度下的平衡常数K=10x-y
H3R+HR2-在该温度下的平衡常数K=10x-y
【答案】CD
【解析】
A. 柠檬酸溶液电离方程式:H3R![]() H2R-+H+,H2R-
H2R-+H+,H2R-![]() HR2-+H+,HR2-
HR2-+H+,HR2-![]() R3-+H+,在a点时,c(H2R-)=c(H3R),第一步电离常数Ka1(H3R)=
R3-+H+,在a点时,c(H2R-)=c(H3R),第一步电离常数Ka1(H3R)=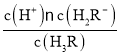 =c(H+)=10-3.3,故其数量级为10-4,A错误;
=c(H+)=10-3.3,故其数量级为10-4,A错误;
B. b点时,c(NaH2R)=c(Na2HR),根据物料守恒可得2c(Na+)=3[c(R3-)+c(HR2-)+c(H2R-)+c(H3R)],B错误;
C. 根据图示,随着pH值的增大,氢离子浓度会减小,平衡向右移动,所以H3R含量会减少。pH=6时,c(R3-)=c(HR2-),溶液显示酸性,c(H+)>c(OH-),盐电离产生的离子浓度大于弱电解质电离产生的离子浓度,即c(HR2-)>c(H+),故c(R3-)=c(HR2-)>c(H+)>c(OH-),C正确;
D. H3R![]() H2R-+H+的电离平衡常数Ka1(H3R)=
H2R-+H+的电离平衡常数Ka1(H3R)=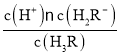 =c(H+)=10-x;H2R-
=c(H+)=10-x;H2R-![]() HR2-+H+的电离平衡常数Ka2(H3R)=
HR2-+H+的电离平衡常数Ka2(H3R)= =c(H+)=10-y,反应2H2R-
=c(H+)=10-y,反应2H2R-![]() H3R+HR2-在该温度下的平衡常数K=
H3R+HR2-在该温度下的平衡常数K=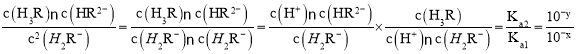 =10x-y,D正确;
=10x-y,D正确;
故合理选项是CD。


科目:高中化学 来源: 题型:
【题目】某同学为测定Na2CO3固体(含少量NaCl)的纯度,设计如下装置(含试剂)进行实验。
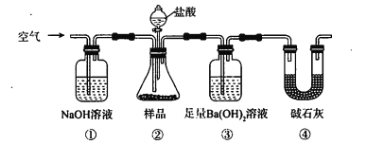
下列说法不正确的是
A. 必须在②③间添加吸收HCl的装置
B. ④的作用是防止空气中的气体影响实验的精确度
C. 通入空气的作用是保证②中产生的气体完全转移到③中
D. 称取样品和③中产生的沉淀的质量即可求算Na2CO3固体的纯度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 表示阿伏加德罗常数的值,工业制备硝酸的过程中发生反应
表示阿伏加德罗常数的值,工业制备硝酸的过程中发生反应![]() 。下列说法正确的是
。下列说法正确的是
A.室温下,22.4LNO2中所含原子总数为![]()
B.36g![]() 中含有
中含有![]() 键的总数为
键的总数为![]()
C.标准状况下,11.2LNO中所含电子总数为![]()
D.上述反应中,生成1mol![]() 转移电子的数目为
转移电子的数目为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列各说法中,正确的是
A.ΔH>0表示放热反应,ΔH<0表示吸热反应
B.热化学方程式中的化学计量数只表示物质的量,可以是分数
C.已知C(s)+![]() O2(g)=CO(g) ΔH=-110.5kJ·mol-1,说明碳的燃烧热为110.5kJ·mol-1
O2(g)=CO(g) ΔH=-110.5kJ·mol-1,说明碳的燃烧热为110.5kJ·mol-1
D.1molH2与0.5molO2反应放出的热就是H2的燃烧热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于苯的叙述正确的是( )
A.苯与溴水混合振荡,二者发生加成反应,静置后溴水层为无色
B.由苯的结构式![]() 可知,苯分子中含C=C键,能使溴的四氯化碳溶液褪色
可知,苯分子中含C=C键,能使溴的四氯化碳溶液褪色
C.由苯的分子式C6H6可知,苯是不饱和烃,能与溴水发生加成反应
D.苯不能使酸性高锰酸钾溶液褪色,说明苯分子中不含碳碳双键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组用如图装置(支撑仪器略去)探究乙醇的催化氧化反应。
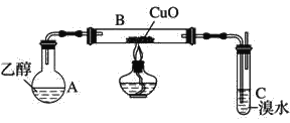
(1)实验开始时,对A进行水浴加热,其目的是__。
(2)B中反应方程式为__。
(3)若装置C中开始发生倒吸,则采取的应急措施是__(填编号)。
a.移去图中的酒精灯 b.将C中橡皮塞拔出
c.将B尾端的乳胶管取下 d.将A与B之间的乳胶管取下
(4)探究:充分反应后,观察到溴水完全褪色。学习小组通过测定反应前溴水中n(Br2)与反应后溶液中n(Br﹣)来确定乙醛使溴水褪色的原因。
①假设:请写出假设1的反应类型。
假设1:CH3CHO+Br2→CH2BrCHO+HBr__;
假设2:CH3CHO+Br2→CH3CHBrOBr 加成反应;
假设3:CH3CHO+Br2+H2O→CH3COOH+2HBr 氧化反应。
①结论:若实验测得n(Br2)=0.005mol,n(Br﹣)=0.01mol,则证明假设__正确。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中发生下列反应aA(g)![]() cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡1.8倍,下列叙述正确的是
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡1.8倍,下列叙述正确的是
A.平衡向正反应方向移动B.A的转化率变大
C.D的物质的量变多D.a<c+d
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值。下列叙述正确的是( )
A.1.0L0.1mol·L-1乙酸钠溶液中,CH3COO-数目为0.1NA
B.11.2L(标准状况)正戊烷完全燃烧生成CO2分子的数目为2.5NA
C.标准状况下,14g乙烯与2-丁烯的混合物中含有的氢原子数为2NA
D.含0.1molHNO3的稀硝酸与足量Cu反应,转移电子数为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用真空碳热还原冶炼镁、铝及锰的单质或合金是治金工业的热点之一。回答下列问题:
(1)已知体系自由能变化![]() 时反应能自发进行。
时反应能自发进行。![]() 真空碳热还原冶炼镁的主要反应为
真空碳热还原冶炼镁的主要反应为![]() ,其自由能变化与温度、压强的关系如图所示:
,其自由能变化与温度、压强的关系如图所示:

温度由低到高的顺序是_______________,![]() 时该反应不能自发进行的温度是_________(填“
时该反应不能自发进行的温度是_________(填“![]() ”“
”“![]() ”或“
”或“![]() ”)。
”)。
(2)![]() 提出的碳热还原
提出的碳热还原![]() 冶炼
冶炼![]() 的机理如下:
的机理如下:
(Ⅰ)![]()
(Ⅱ)![]()
(Ⅲ)![]()
则反应![]() 的
的![]() ______________
______________![]() (用含a、b、c的代数式表示);中间体之一
(用含a、b、c的代数式表示);中间体之一![]() 与
与![]() 反应可用于实验室制备甲烷,写出
反应可用于实验室制备甲烷,写出![]() 与
与![]() 反应的化学方程式:_________________________________________________________。
反应的化学方程式:_________________________________________________________。
(3)制备锰合金的相关反应及平衡时![]() 与温度的关系如图所示(
与温度的关系如图所示(![]() 为用分压表示的平衡常数,分压=总压×体积分数):
为用分压表示的平衡常数,分压=总压×体积分数):
(Ⅰ)![]()
(Ⅱ)![]()
(Ⅲ)![]()
①![]() 的反应是___________(填标号)。
的反应是___________(填标号)。
②![]() ____________[用
____________[用![]() 、
、![]() 表示];A点
表示];A点![]() ___________用[
___________用[![]() 表示]。
表示]。
③向某恒容密闭容器中充入![]() 并加入足量
并加入足量![]() ,若只发生反应:
,若只发生反应:![]() ,达到B点的平衡状态。达到平衡前,v(正)__________v(逆)(填“大于”“小于”或“等于”),达到平衡时,
,达到B点的平衡状态。达到平衡前,v(正)__________v(逆)(填“大于”“小于”或“等于”),达到平衡时,![]() _______________(保留小数点后两位)。
_______________(保留小数点后两位)。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com