
【题目】下列物质中能明显增强漂白粉溶液的漂白能力的是( )
A.食盐
B.白醋
C.小苏打
D.烧碱
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:
【题目】短周期元素A、B、C、D、E原子序数依次增大。A是周期表中原子半径最小的元素,B原子的价电子数等于该元素最低化合价的绝对值,C与D能形成D2C和D2C2两种化合物,而D是同周期中金属性最强的元素,E的负一价离子与C和A形成的某种化合物分子含有相同的电子数。
(1)A、C、D形成的化合物中含有的化学键类型为_______________。
(2)已知:①E-E→2E·;△H=+a kJ·mol-1
② 2A·→A-A;△H=-b kJ·mol-1
③E·+A·→A-E;△H=-c kJ·mol-1(“·”表示形成共价键所提供的电子)
写出298K时,A2与E2反应的热化学方程式____________________________________。
(3)在某温度下、容积均为2L的三个密闭容器中,按不同方式投入反应物,保持恒温恒容,使之发生反应:2A2(g)+BC(g)![]() X(g);△H=-dJ·mol-1(d>0,X为A、B、C三种元素组成的一种化合物)。初始投料与各容器达到平衡时的有关数据如下:
X(g);△H=-dJ·mol-1(d>0,X为A、B、C三种元素组成的一种化合物)。初始投料与各容器达到平衡时的有关数据如下:
实验 | 甲 | 乙 | 丙 |
初始投料 | 2 molA2、1 molBC | 1 molX | 4 molA2、2 molBC |
平衡时n(X) | 0.5mol | n2 | n3 |
反应的能量变化 | 放出Q1kJ | 吸收Q2kJ | 放出Q3kJ |
体系的压强 | P1 | P2 | P3 |
反应物的转化率 | α1 | α2 | α3 |
①在该温度下,假设甲容器从反应开始到平衡所需时间为4 min,则该时间段内A2的平均反应速率v(A2)________。
②该温度下此反应的平衡常数K的值为___________。
③三个容器中的反应分别达平衡时各组数据关系正确的是_______(填序号)。
A.α1+α2=1 B.Q1+Q2=d C.α3<α1
D.P3<2P1=2P2 E.n2<n3<1.0mol F.Q3=2Q1
④在其他条件不变的情况下,将甲容器的体系体积压缩到1L,若在第8min达到新的平衡时A2的总转化率为65.5%,请在下图中画出第5min 到新平衡时X的物质的量浓度的变化曲线。_______
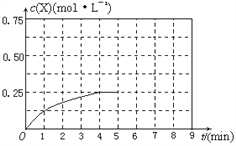
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2(g)+NO2(g)![]() SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图所示。下列说法正确的是
SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图所示。下列说法正确的是

A. 反应物浓度:a点小于b点
B. 反应物的总能量大于生成物的总能量
C. △t1=△t2时,SO2的转化率:a~b段大于b~c段
D. 反应进行到c点达平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若某原子的外围电子排布式为4d15s2,则下列说法正确的是
A. 该元素位于周期表中第五周期IIIB族 B. 该元素原子价电子数为2个
C. 该元素为非金属元素 D. 该元素原子N能层共有8个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.126C和146C互为同位素
B.金刚石和石墨互为同素异形体
C.CH3COOCH2CH3和CH3CH2CH2COOH互为同分异构体
D.CH4和CH3Cl互为同系物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com