
| A. | 正极反应为4OH--4e-=2H2O+O2↑ | |
| B. | 放电时CO32-向负极移动 | |
| C. | 电池放电时,电池中CO32-的物质的量将逐渐减少 | |
| D. | 电路中电子由负极、经熔融的K2CO3流到正极,形成闭合回路 |
分析 该原电池中,通入燃料氢气的电极是负极,通入氧化剂氧气的电极是正极,负极反应式为H2+CO32--2e-=H2O+CO2,正极反应式为O2+2CO2+4e-=2CO32-,
A.正极上氧气得电子和二氧化碳反应生成碳酸根离子;
B.放电时,电解质中阴离子向负极移动,阳离子向正极移动;
C.放电时,根据电池反应式知,碳酸根离子不参加反应;
D.放电时,电子从负极沿导线流向正极,不进入电解质中.
解答 解:A.正极上氧气得电子和二氧化碳反应生成碳酸根离子,正极反应式为O2+2CO2+4e-=2CO32-,故A错误;
B.放电时,电解质中阴离子向负极移动,阳离子向正极移动,所以CO32-向负极移动,故B正确;
C.放电时,根据电池反应式知,碳酸根离子不参加反应,所以电解质中碳酸根离子物质的量不变,故C错误;
D.放电时,电子从负极沿导线流向正极,不进入电解质中,电解质中通过阴阳离子定向移动形成电流,故D错误;
故选B.
点评 本题考查化学电源新型电池,为高频考点,明确电子流向、离子移动方向、各个电极发生的反应是解本题关键,难点是电极反应式的书写,要结合电解质特点书写,易错选项是D.


科目:高中化学 来源: 题型:解答题
 A、B、C、D、E、F六种物质的相互转化关系如图所示(反应条件未标出),其中反应①是置换反应.
A、B、C、D、E、F六种物质的相互转化关系如图所示(反应条件未标出),其中反应①是置换反应.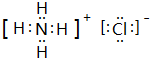 ,反应③的化学方程式是4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.
,反应③的化学方程式是4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,下列说法错误的是( )
,下列说法错误的是( )| A. | 反应物的分子式为C10H10O4 | |
| B. | X的结构简式为CH3OH | |
| C. | 生成物中带“※”号的C原子来自“ ”中的甲基 ”中的甲基 | |
| D. | 反应物和生成物具有相同的不饱和度 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该有机物分子中C、H、O原子个数比为1:2:3 | |
| B. | 该有机物中必定含有氧元素 | |
| C. | 该有机物分子中C、H原子个数比为1:2 | |
| D. | 该有机物化学式为C2H4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com