
ЎѕМвДїЎїТСЦЄНєНЕЁБтЛбїЙТФФЪјУИИМхјюПВ·ўЙъИзПВ·ґУ¦Јє
Cu+2H2SO4(ЕЁ)![]() CuSO4+ SO2 Ўь +2H2O
CuSO4+ SO2 Ўь +2H2O
(1)ИЎТ»¶ЁБїµДНЖ¬Ул100mL18mol/LµДЕЁH2SO4ід·Ц·ґУ¦Ј¬Из№ыёГ·ґУ¦№эіМЦРЧЄТЖБЛ0.2molµзЧУЈ¬јЖЛгЙъіЙµДCuSO4µДЦКБї_______єНЙъіЙµДSO2ЖшМеФЪ±кЧјЧґїцПВМе»э_______ЈЁјЩЙиЖшМеИ«ІїТЭіцЈ©ЎЈ
(2)Ѕ«·ґУ¦єуЛщµГµЅµДИЬТєУлЧгБїBa(OH)2ИЬТєід·Ц·ґУ¦Ј¬јЖЛгЈє·ґУ¦єуЛщµГіБµнµДЦКБї_______ЈЁ±ЈБфµЅ0.1gЈ©ЎЈ
Ўѕґр°ёЎї16g 2.24L 405.9g
ЎѕЅвОцЎї
(1)ЅбєП·ґУ¦µД·ЅіМКЅТФј°Сх»Ї»№Ф·ґУ¦ЦРµГК§µзЧУКэДїПаµИјЖЛгЎЈ
(2)ёщѕЭФЄЛШКШєгЈ¬ПИјЖЛгіцЕЁБтЛбЦРSµДОпЦКµДБїЈ¬јхИҐSO2µДОпЦКµДБїЈ¬ѕНµГµЅ·ґУ¦єуИЬТєЦРSO42-µДОпЦКµДБїЈ¬јУИлBa(OH)2ИЬТєЈ¬·ґУ¦ІъЙъBaSO4іБµнЈ¬ИЬТєЦРµДCu2+УлOH-ЅбєПРОіЙCu(OH)2іБµнЈ¬·ґУ¦єуЛщµГіБµнОЄCu(OH)2єНBaSO4Ј¬ёщѕЭФЄЛШКШєгЈ¬їЙјЖЛгіцCu(OH)2єНBaSO4іБµнµДЦКБїєНЎЈ
(1)CuУлЕЁH2SO4·ґУ¦·ЅіМКЅОЄЈєCu+2H2SO4(ЕЁ)![]() CuSO4+ SO2 Ўь +2H2OЈ¬їЙЦЄЈєµзЧУЧЄТЖ2molЈ¬ѕН»бЙъіЙ1molSO2ЖшМеєН1molCuSO4Ј¬ФтёГ·ґУ¦№эіМЦРЧЄТЖБЛ0.2molµзЧУЈ¬ЙъіЙµД0.1molSO2 ЖшМеЈ¬ЖдФЪ±кЧјЧґїцПВМе»эОЄV(SO2)=0.1molЎБ22.4L/mol=2.24LЈ¬ЙъіЙµДCuSO4µДОпЦКµДБїОЄ0.1molЈ¬ЖдЦКБїОЄm(CuSO4)=0.1molЎБ160g/mol=16gЈ»
CuSO4+ SO2 Ўь +2H2OЈ¬їЙЦЄЈєµзЧУЧЄТЖ2molЈ¬ѕН»бЙъіЙ1molSO2ЖшМеєН1molCuSO4Ј¬ФтёГ·ґУ¦№эіМЦРЧЄТЖБЛ0.2molµзЧУЈ¬ЙъіЙµД0.1molSO2 ЖшМеЈ¬ЖдФЪ±кЧјЧґїцПВМе»эОЄV(SO2)=0.1molЎБ22.4L/mol=2.24LЈ¬ЙъіЙµДCuSO4µДОпЦКµДБїОЄ0.1molЈ¬ЖдЦКБїОЄm(CuSO4)=0.1molЎБ160g/mol=16gЈ»
(2)n(H2SO4)=cV=18mol/LЎБ0.1L=1.8molЈ¬·ґУ¦ІъЙъSO2ЖшМеЈ¬ПыєДµДSO42-µДОпЦКµДБїКЗ0.1molЈ¬ТтґЛ·ґУ¦єуИЬТєЦРє¬УРµДSO42-µДОпЦКµДБїОЄn(SO42-)=1.8mol-0.1mol=1.7molЈ¬ПтёГИЬТєЦРјУИлЧгБїBa(OH)2ИЬТєЈ¬·ґУ¦ІъЙъBaSO4іБµнЈ¬ёщѕЭSФЄЛШКШєгЈ¬їЙЦЄBaSO4іБµнµДОпЦКµДБїКЗ1.7molЈ¬Фтm(BaSO4)=1.7molЎБ233g/mol=396.1gЎЈёщѕЭ(1)јЖЛгїЙЦЄn(CuSO4)=0.1molЈ¬јУИлBa(OH)2єуЈ¬Cu2+ЧЄ»ЇОЄCu(OH)2іБµнЈ¬ФтёщѕЭCuФЄЛШКШєгїЙµГn[Cu(OH)2]=n(CuSO4)=0.1molЈ¬m[Cu(OH)2]=0.1molЎБ98g/mol=9.8gЈ¬ЛщТФЧоєуїЙµГіБµнµДЦКБїОЄЈє396.1g+9.8g=405.9gЎЈ


 РВїО±кЅЧМЭФД¶БСµБ·ПµБРґр°ё
РВїО±кЅЧМЭФД¶БСµБ·ПµБРґр°ё їЪЛгРДЛгЛЩЛгУ¦УГМвПµБРґр°ё
їЪЛгРДЛгЛЩЛгУ¦УГМвПµБРґр°ё
| Дкј¶ | ёЯЦРїОіМ | Дкј¶ | іхЦРїОіМ |
| ёЯТ» | ёЯТ»Гв·СїОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СїОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СїОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СїОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СїОіМНЖјцЈЎ | іхИэ | іхИэГв·СїОіМНЖјцЈЎ |
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїАыУГјЧНйУлВИЖш·ўЙъИЎґъ·ґУ¦Ј¬Н¬К±»сµГё±ІъЖ·СОЛбµДЙиПлФЪ№¤ТµЙПТСіЙОЄПЦКµЎЈДі»ЇС§РЛИ¤РЎЧйДвФЪКµСйКТЦРДЈДвЙПКц№эіМЈ¬ЖдЙијЖµДДЈДвЧ°ЦГИзПВЈє

ёщѕЭТЄЗуМоїХЈє
ЈЁ1Ј©µј№ЬaµДЧчУГКЗ______________________ЎЈBЧ°ЦГУРИэЦЦ№¦ДЬЈ»ўЩёЙФп»мєПЖшМеЈ»ўЪЅ«ЖшМе»мєПѕщФИЈ»ўЫ___________________________ЎЈ
ЈЁ2Ј©CЧ°ЦГЦРCH4УлCl2·ґУ¦ЙъіЙТ»ВИґъОпµД»ЇС§·ґУ¦·ЅКЅКЗ_______________________ЎЈ
DЧ°ЦГЦРµДКЇГЮЙПѕщФИёЅЧЕі±КЄµДKIЈ¬Рґіц·ґУ¦µДАлЧУ·ЅіМКЅКЗ____________________ЎЈ
ЈЁ3Ј©EЧ°ЦГЦРіэБЛУРСОЛбЙъіЙНвЈ¬»№є¬УРУР»ъОпЎЈґУEЦР·ЦАліцСОЛбµДЧојС·Ѕ·ЁОЄ___________
ЈЁ4Ј©EЧ°ЦГµДЧчУГКЗ____________ЎЈЈЁМоРтєЕЈ©ЎЈ
AЈ®КХјЇЖшМе BЈ®ОьКХВИЖш CЈ®·АЦ№µ№Оь DЈ®ОьКХВИ»ЇЗв
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїПВБРУР№ШН¬·ЦТм№№МеКэДїµДРрКцІ»ХэИ·µДКЗ
A. јЧ±Ѕ±Ѕ»·ЙПµДТ»ёцЗвФЧУ±»є¬3ёцМјФЧУµДНй»щИЎґъЈ¬ЛщµГІъОпУР6ЦЦ
B. Ул![]() »ҐОЄН¬·ЦТм№№МеµД·јПгЧе»ЇєПОпУР6ЦЦ
»ҐОЄН¬·ЦТм№№МеµД·јПгЧе»ЇєПОпУР6ЦЦ
C. є¬УР5ёцМјФЧУµДДі±ҐєНБґМюЈ¬ЖдТ»ВИИЎґъОпїЙДЬУР3ЦЦ
D. ·ЖµДЅб№№јтКЅОЄ Ј¬ЛьУлПхЛб·ґУ¦Ј¬їЙЙъіЙ5ЦЦТ»Пх»щИЎґъОп
Ј¬ЛьУлПхЛб·ґУ¦Ј¬їЙЙъіЙ5ЦЦТ»Пх»щИЎґъОп
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїПЦУРЛДЖїК§ИҐ±кЗ©µДОЮЙ«ИЬТєЈ¬їЙДЬКЗCaCl2ЎўAgNO3ЎўHClЎўNa2CO3ЦРµДЖдЦРТ»ЦЦЈ¬ОЄБЛИ·¶ЁѕЯМеіЙ·ЦЈ¬ЛжТвЅ«ЛДЖїИЬТє±кјЗОЄAЎўBЎўCЎўDєуЈ¬ЅшРРБЛПВБРЛДЧйКµСйЎЈ
КµСйЛіРт | КµСйДЪИЭ | КµСйПЦПу |
ўЩ | A+B | ОЮГчПФПЦПу |
ўЪ | B+D | УРЖшМе·Еіц |
ўЫ | B+C | УРіБµнЙъіЙ |
ўЬ | A+D | УРіБµнЙъіЙ |
ёщѕЭ±нЦРКµСйПЦПу»ШґрПВБРОКМвЈє
ЈЁ1Ј©AЎўBЎўCЎўD·Ц±р¶ФУ¦µДИЬЦК»ЇС§КЅОЄ____________Ўў___________Ўў___________Ўў___________Ј»
ЈЁ2Ј©Зл·Ц±рРґіцЙПКцКµСйўЪєНўЫµДАлЧУ·ЅіМКЅЈє
ўЪ________________________________________________________Ј»
ўЫ________________________________________________________ЎЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїПВБРРрКцХэИ·µДКЗ
A. 24 g ГѕУл27 gВБЦРЈ¬є¬УРПаН¬µДЦКЧУКэ
B. Н¬µИЦКБїµДСхЖшєНіфСхЦРЈ¬µзЧУКэПаН¬
C. 1 molЦШЛ®Ул1 molЛ®ЦРЈ¬ЦРЧУКэ±ИОЄ2ЎГ1
D. 1 molТТНйєН1 molТТП©ЦРЈ¬»ЇС§јьКэПаН¬
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїКµСйКТЕдЦЖ500 mL 0.2 molЎ¤LЈ1µДNa2CO3ИЬТєЈ¬КµСйІЩЧчІЅЦиУР
ўЩУГМмЖЅіЖИЎТ»¶ЁБїµДNa2CO3Ў¤10H2OЈ¬·ЕФЪЙХ±ЦРУГККБїµДХфБуЛ®Ѕ«ЖдНкИ«ИЬЅвЈ»
ўЪ°СЦЖµГµДИЬТєРЎРДµШЧўИл______ЦРЈ»
ўЫјМРшПтИЭБїЖїЦРјУХфБуЛ®ЦБТєГжѕаїМ¶ИПЯ1 cmЎ«2 cmґ¦Ј¬ёДУГ______РЎРДµОјУХфБуЛ®ЦБИЬТє°јТєГжЧоµНґ¦УлїМ¶ИПЯПаЗРЈ»
ўЬУГЙЩБїХфБуЛ®ПґµУЙХ±єНІЈБ§°ф2Ў«3ґОЈ¬ГїґОПґµУµДТєМе¶јРЎРДЧЄТЖИлИЭБїЖїЈ¬ІўЗбЗбТЎФИЈ»
ўЭЅ«ИЭБїЖїИыИыЅфЈ¬ід·ЦТЎФИЎЈ
ЗлМоРґПВБРїХ°ЧЈє
(1)ІЩЧчІЅЦиµДХэИ·ЛіРтОЄ(МоРтєЕ)_________Ј»
(2)РґіцўЪўЫІЅЦиЦРЈ¬ЛщИ±µДТЗЖч______________Ўў______________Ј»
(3)ИфКµСйУцПВБРЗйїцЈ¬ИЬТєµДОпЦКµДБїЕЁ¶ИКЗЈє ўЩЖ«ёЯ ўЪЖ«µН ўЫГ»У°Пм
A.јУЛ®¶ЁИЭК±ё©КУїМ¶ИПЯ________(МоРтєЕ)
B.НьјЗЅ«ПґµУТєЧЄИлИЭБїЖї__________(МоРтєЕ)
C.К№УГЗ°ИЭБїЖїУГХфБуЛ®ПґµУЈ¬ЗТГ»УРёЙФп__________ (МоРтєЕ)
D.¶ЁИЭК±Ј¬І»РЎРДјУЛ®№эБїЈ¬ВнЙПУГЅєН·µО№ЬОьіц __________ (МоРтєЕ)
(4)јЖЛгЛщРиNa2CO3Ў¤10H2OµДЦКБї__________ЎЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїДіС§ЙъПлЦЖЧчТ»ЦЦјТУГ»·±ЈРНПы¶ѕТє·ўЙъЖчЈ¬УГКЇД«Ччµзј«µзЅв±ҐєНВИ»ЇДЖИЬТєЈ¬НЁµзК±Ј¬ОЄК№Cl2±»НкИ«ОьКХЈ¬ЦЖµГУРЅПЗїЙ±ѕъДЬБ¦µДПы¶ѕТєЈ¬ЙијЖБЛИзНјµДЧ°ЦГЎЈ¶ФµзФґµзј«ГыіЖєНПы¶ѕТєµДЦчТЄіЙ·ЦЕР¶ПХэИ·µДКЗ
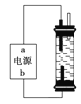
A. aОЄХэј«Ј¬bОЄёєј«Ј»NaClOєНNaCl
B. aОЄёєј«Ј¬bОЄХэј«Ј»NaClOєНNaCl
C. aОЄСфј«Ј¬bОЄТхј«Ј»HClOєНNaCl
D. aОЄТхј«Ј¬bОЄСфј«Ј»HClOєНNaCl
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїЈЁ1Ј©ЕдЖЅёГ·ґУ¦µД»ЇС§·ЅіМКЅЈє___
ўЩ FeSO4+ KMnO4+ H2SO4= K2SO4+ MnSO4+ Fe2(SO4)3+ H2O
ўЪёГ·ґУ¦ЦРµДСх»ЇјБКЗ___Ј¬Сх»ЇІъОпКЗ____ЎЈ
ўЫИфПыєД3.16gKMnO4Ј¬ФтёГ·ґУ¦ЧЄТЖµДµзЧУКэДїОЄ____ЎЈ
ЈЁ2Ј©ТСЦЄ·ґУ¦ЈєўЩCl2+2KBr=2KCl+Br2Ј¬ўЪ2KMnO4+16HCl(ЕЁ)=2KCl+2MnCl2+5Cl2Ўь+8H2OЈ¬ўЫBr2+K2S=2KBr+SЎЈ
ўЩПВБРЛµ·ЁХэИ·µДКЗ__ЎЈ
AЈ®ЙПКцИэёц·ґУ¦¶јУРµҐЦКЙъіЙЈ¬ЛщТФ¶јКЗЦГ»»·ґУ¦
BЈ®Сх»ЇРФУЙЗїµЅИхЛіРтОЄKMnO4ЈѕCl2ЈѕBr2ЈѕS
CЈ®·ґУ¦ўЪЦР»№ФјБУлСх»ЇјБµДОпЦКµДБїЦ®±ИОЄ8Јє1
DЈ®·ґУ¦ўЫЦР1mol»№ФјБ±»Сх»ЇФтЧЄТЖµзЧУµДОпЦКµДБїОЄ2mol
ўЪУГµҐПЯЗЕ·Ё±кіц·ґУ¦ўЪЦРµзЧУЧЄТЖµД·ЅПтєНКэДї___ЎЈ
2KMnO4+16HCl(ЕЁ)=2KCl+2MnCl2+5Cl2Ўь+8H2O
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїОЄМЅѕїДіОпЦКX(Ѕцє¬БЅЦЦФЄЛШ)µДЧйіЙєНРФЦКЈ¬ЙијЖІўНкіЙИзПВКµСйЎЈ(ЖшМеМе»эТСЧЄ»ЇОЄ±кїцМе»э)
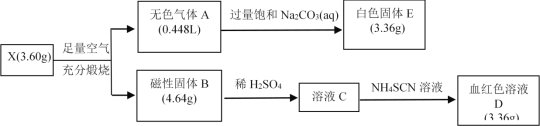
Зл»ШґрПВБРОКМвЈє
(1)XµД»ЇС§КЅОЄ___________ЎЈ
(2)AµДЅб№№КЅОЄ________Ј¬EКфУЪ_______»ЇєПОп(МоАлЧУ»т№ІјЫ)ЎЈ
Ійїґґр°ёєНЅвОц>>
№ъјКѧУУЕСЎ - Б·П°ІбБР±н - КФМвБР±н
єю±±КЎ»ҐБЄНшОҐ·ЁєНІ»БјРЕПўѕЩ±ЁЖЅМЁ | НшЙПУРє¦РЕПўѕЩ±ЁЧЁЗш | µзРЕХ©ЖѕЩ±ЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРє¦РЕПўѕЩ±ЁЧЁЗш | ЙжЖуЗЦИЁѕЩ±ЁЧЁЗш
ОҐ·ЁєНІ»БјРЕПўѕЩ±Ёµз»°Јє027-86699610 ѕЩ±ЁУКПдЈє58377363@163.com