
| A、铜和稀硝酸反应:3Cu+8H++2NO3-═3Cu2++2NO2↑+4H2O |
| B、二氧化碳通入足量澄清石灰水中:Ca2++2OH-+CO2═CaCO3↓+H2O |
| C、铁和盐酸反应:2Fe+6H+═2Fe3++3H2↑ |
| D、氧化铜溶于足量盐酸中:O2-+2H+═H2O |


科目:高中化学 来源: 题型:
 醋酸是中学常用的一种弱酸.
醋酸是中学常用的一种弱酸.查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D | |
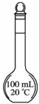
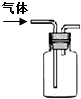
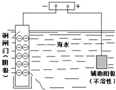
图示 |
 |
 |
 |
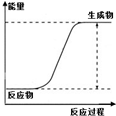 |
| 说明 | 该仪器用于配制一定质量分数的溶液 | 该装置可以收集二氧化氮 | 该装置可保护钢闸门不被腐蚀 | 该化学反应为吸热反应 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、一段时间后两烧杯中c(Zn2+)、c(Cu2+)均减小 |
| B、原电池工作时,Cu电极流出电子,发生氧化反应 |
| C、原电池工作时的总反应为Zn+Cu2+═Zn2++Cu |
| D、盐桥中装有含氯化钾的琼脂,其作用是传递电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 称量氢氧化钠固体 |
B、 配制150mL 0.10mol/L盐酸 |
C、 检验铁粉与水蒸气反应产生的氢气 |
D、 分离两种互溶但沸点相差较大的液体混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验目的 | 操作 | |
| A | 除去溴乙烷中溶有的溴 | 加入亚硫酸钠溶液,振荡,静置,分液 |
| B | 确定组成为 C2H4O2的有机物的结构简式 |
加入银氨溶液,水浴加热 |
| C | 证明蛋白质在某些无机盐溶液作用下发生变性 | 向鸡蛋清溶液中加入饱和硫酸钠溶液,过滤,将沉淀加入蒸馏水中 |
| D | 证明SO2具有漂白粉 | 将SO2通入酸性KMnO4溶液中 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、采取“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”等方法,可提高空气质量 |
| B、采用天然石材装修家居,可减轻室内甲醛污染但会导致一定量的放射性物质的污染 |
| C、汽油中添加含铅化合物Pb(C2H5)4,可提高汽油的抗爆震性能,有利于改善大气环境 |
| D、PM2.5表示每立方米空气中直径小于或等于2.5微米的颗粒物的含量,PM2.5值越高,大气污染越严重 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| △ |
| 实验序号 | 时间浓度温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | C2 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 3 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com