
【题目】许多国家重视海水资源的综合利用,不需要化学变化就能够从海水中获得的物质是
A. 氯、溴、碘 B. 烧碱、氢气 C. 粗盐、淡水 D. 钠、镁、铝
科目:高中化学 来源: 题型:
【题目】某有机物的氧化产物是甲,还原产物是乙,甲和乙都能与钠反应放出H2,甲和乙反应生成丙,甲和丙都能发生银镜反应。该有机物是
A. 甲醛 B. 乙醛 C. 甲酸 D. 甲醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无机盐在生命活动中不可缺少,合成叶绿素和血红蛋白分子必需的离子分别是( )
A. Mg2+、Fe2+ B. Ca2+、Mg2+
C. PO43-、K+ D. K+、I-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】84消毒液的pH为10.1,最适宜的测定方法是
A. 使用pH试纸 B. 使用红色石蕊试纸
C. 使用数字pH计 D. 以酚酞为指示剂进行酸碱中和滴定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列物质中,属于弱电解质的是(填序号,下同) ,属于非电解质是 。
①硫酸氢钠固体 ②次氯酸钠 ③氯化氢气体 ④蔗糖 ⑤硫酸钡 ⑥氨气 ⑦冰醋酸
(2)写出下列物质在水中的电离方程式:碳酸: 。次氯酸钠: 。
(3)甲、乙两瓶氨水的浓度分别为1 molL-1、0.1 molL-1,则c(OH﹣)甲:c(OH﹣)乙 10(填“大于”、“等于”或“小于”)。
(4)现有常温条件下甲、乙、丙三种溶液,甲为0.1 molL-1的NaOH溶液,乙为0.1 molL-1的HCl溶液,丙为0.1 molL-1的CH3COOH溶液,甲、乙、丙三种溶液中由水电离出的c(OH﹣)的大小关系为 。
(5)NO2与NO之间存在如下可逆反应:2NO2![]() 2NO+O2。T oC时,在一恒容密闭容器中充入适量NO2,反应达到平衡状态的标志是 。(填序号)
2NO+O2。T oC时,在一恒容密闭容器中充入适量NO2,反应达到平衡状态的标志是 。(填序号)
①混合气体的颜色不再改变的状态
②混合气体的密度不再改变的状态
③混合气体的压强不再改变的状态
④混合气体的平均相对分子质量不再改变的状态
⑤![]() 的比值不再改变的状态
的比值不再改变的状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁及其化合物有重要用途,如聚合硫酸铁![]() 是一种新型高效的水处理混凝剂,而高铁酸钾(其中铁的化合价为+6)是一种重要的杀菌消毒剂,某课题小组设计如下方案制备上述两种产品:
是一种新型高效的水处理混凝剂,而高铁酸钾(其中铁的化合价为+6)是一种重要的杀菌消毒剂,某课题小组设计如下方案制备上述两种产品:

请回答下列问题:
(1)若A为H2O(g),写出反应方程式:_________________________。
(2)若B为NaClO3与稀硫酸,写出其氧化Fe2+的离子方程式(还原产物为Cl-) 。
(3)若C为KNO3和KOH的混合物,写出其与Fe2O3加热共融制得高铁酸钾(K2FeO4)的化学方程式,并配平:
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关下列图像的分析正确的是
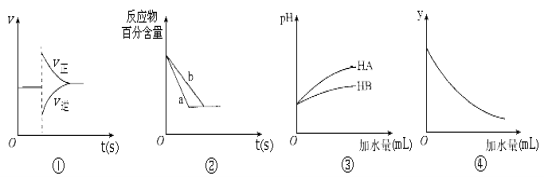
A.图①表示在N2(g)+3H2(g)![]() 2NH3(g)达到平衡后,减少NH3浓度时速率的变化
2NH3(g)达到平衡后,减少NH3浓度时速率的变化
B.图②中a、b曲线分别表示反应H2(g)十I2(g)![]() 2HI(g)在有催化剂和无催化剂存在下建立平衡的过程。
2HI(g)在有催化剂和无催化剂存在下建立平衡的过程。
C.图③说明HB是比HA更弱的酸
D.图④中的y可表示将冰醋酸加水稀释时溶液导电能力的变化情况
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列说法正确的是
A.lmolNaCl 固体中含有NA个Na+
B.18gD2O和18gH2 O中含有的质子数均为10NA
C.标准状况下2.24LH2O 含有的共价键数为0.2NA
D.密闭容器中2molNO 与lmolO2充分反应,产物的分子数为2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com