
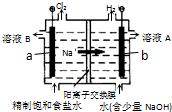
| A、b电极上发生还原反应 |
| B、a电极的材料为金属铁 |
| C、溶液A为电解后的稀氯化钠残液 |
| D、溶液B为NaCl、NaClO的混合液 |
| ||


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、温度不变,增大容器的体积,液体的颜色变浅 |
| B、温度不变,减少容器的体积,S2Cl2的转化率降低 |
| C、压强不变,升高温度,液体的颜色变浅 |
| D、体积不变,降低温度,氯气的转化率升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分子式为C4H8有机物最多存在4个C-C单键 |
B、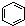 和 和 均是芳香烃, 均是芳香烃, 既是芳香烃又是芳香化合物 既是芳香烃又是芳香化合物 |
C、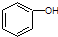 和 和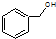 分子组成相差一个-CH2-,因此是同系物关系 分子组成相差一个-CH2-,因此是同系物关系 |
| D、乙酸分子中含有碳氧双键,所以它能使溴水褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、431 | B、649 |
| C、896 | D、945.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
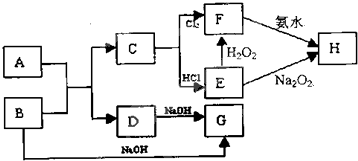
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳和水反应吸收热量131.3 kJ |
| B、1 mol C(s)和1 mol H2O(g)反应生成一氧化碳和氢气,并吸收131.3 kJ的热量 |
| C、1 mol C跟1 mol H2O反应吸收131.3 kJ的热量 |
| D、固体碳和气态水各1 mol反应,放出131.3 kJ的热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 稀H2SO4 |
| △ |
| 一定条件 |
| 浓H2SO4 |
| 170℃ |
| 试剂X |
| XNaOH溶液 |
| △ |
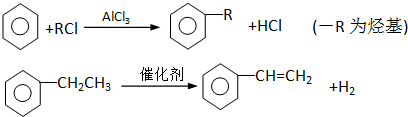
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com