
����Ŀ�����ʵķ�����ж��ַ��������ж��������������ͼ��
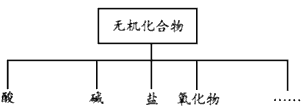
��1����ͼ��ʾ�����ʷ����������____________________��
��2����K��Na��H��O��S��N�������ֻ�����Ԫ����ɺ��ʵ����ʣ��ֱ������±��Тڡ��ܡ����档
������� | �� | �� | �� | ������ | �⻯�� |
��ѧʽ | ��HNO3 ��_______ | ��NaOH ��_______ | ��Na2SO4 ��_______ | ��CO2 ��SO3 | ��NH3 |
��3��д�����������Ģ���Һ��Ӧ�����ӷ���ʽ_______________________��
��4��д���������Һ��Ӧ�Ļ�ѧ����ʽ______________________��
��5����ͼ��ijѧУʵ���Ҵӻ�ѧ�Լ��̵���ص�Ũ�����Լ���ǩ�ϵIJ������ݡ����ø�Ũ��������480 mL 1 mol�� L��1��ϡ���ᡣ
�ɹ�ѡ�õ������У��ٽ�ͷ�ιܢ���ƿ���ձ�����������ҩ�ע���Ͳ��������ƽ��

��ش��������⣺
a������������ʵ���Ũ��Ϊ __________ mol�� L��1��
b������ϡ����ʱ����ȱ�ٵ������� ______________ (д��������)��
c�������㣬����480mL 1mol�� L��1��ϡ������Ҫ����Ͳ��ȡ����Ũ��������Ϊ_________mL��
d���������Ƶ�ϡ������вⶨ��������Ũ�ȴ���1 mol�� L��1�����ƹ��������и�������������������ԭ���� ___________��
A������ʱ����������ƿ�̶��߽��ж��� ��
B����ϡ�ͺ��ϡ��������ת������ƿ�����žͽ����Ժ��ʵ�������
C��ת����Һʱ��������������Һ��������ƿ���档
D������ƿ������ˮϴ�Ӻ�δ���������������ˮ ��
E�����ݺ�����ƿ����ҡ�Ⱥ���Һ����ڿ̶��ߣ��㲹�伸��ˮ���̶ȴ���
���𰸡���״���෨H2SO4KOHKNO3CO2+OH�� �� HCO3��2NaOH+2Al+2H2O===2NaAlO2+3H2��18.4mol/L500mL����ƿ27.2mL��2�֣�A��B
����������1����ѧ�еķ��෨�����֣�һ�ǽ�����෨��������״���෨����״���෨��һ�ֺ�����ķ��෨�����ղ�Σ�һ��һ�����֣�����һ�ô�������Ҷ��֦���ˡ�����ͼʾ����������״ͼ���ʴ�Ϊ����״���෨
��2����������εĶ��壬���ǵ������������ȫ���������ӵĻ������H2SO4�����ǵ������������ȫ��Ϊ���������ӣ���NaOH���ε������������Ϊ�������ӣ���笠����ӣ���������Ϊ������ӣ���KNO3���ʴ�Ϊ����H2SO4����NaOH����KNO3
��3��������̼�������������Ʒ�Ӧ����ˮ��̼�����ƣ��䷴Ӧ�����ӷ���ʽΪ��CO2+OH�� �THCO3��+H2O���ʴ�Ϊ��CO2+OH���THCO3��+H2O
��4��Al�������ᷴӦ��������Ӧ����Ϊ�� 2NaOH+2Al+2H2O===2NaAlO2+3H2��
��5����a��֪��һ����Һ���ܶȡ����ʵ���������������ֱ�����ù�ʽ������ʵ���Ũ�ȣ�
![]() �����������c =18.4mol/L
�����������c =18.4mol/L
(b)��Ũ��Һ����ϡ��Һ��Ҫ�������У���ͷ�ιܡ��ձ���������������Ͳ��500mL����ƿ ���������ṩ��������֪����ȱ��500ml����ƿ��
(c)ץסϡ���������ʵ����ʵ�����������Ũ����������ע��������500mlϡ��Һ��������Ũ�������ΪV��V*18.4=500*1��V=27.2mL��
(d)A������ʱ����������ƿ�̶��߽��ж��ݣ���ˮƫС�����ƫ��Ũ��ƫ�ߣ�A��ȷ��B����ϡ�ͺ��ϡ��������ת������ƿ��δ��ȴ��������Һ������ͣ����ݼ�ˮƫС��Ũ��ƫ�ߣ�B��ȷ��C��ת����Һʱ��������������Һ��������ƿ���棬Ũ��ƫС��C����D������ƿ������ˮϴ�Ӻ�δ���������������ˮ ���Խ����Ӱ�죬D����E�����ݺ�����ƿ����ҡ�Ⱥ���Һ����ڿ̶��ߣ��㲹�伸��ˮ���̶ȴ������Ǵ���IJ��������ڿ̶�������ȷ��������Ϊ������Һճ��ƿ���ϣ�E������ȷ��ΪAB



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����
A���������յķ���������ë�ͺϳ���ά
B���������ƿ���ΪDZˮͧ���������Դ
C��̼�ᱵ����Һ������θ��X �����ӵġ����͡�
D����ĵ����Խ��ڵ���;�Ե��֮�䣬�����������뵼�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����е��ӹ��͵�ԭ���У��ڶ����������һ���������������(����)
A. 1s22s22p5 B. 1s22s22p6 C. 1s22s22p63s1 D. 1s22s22p63s2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʷ����ڿ���������������ԭ��Ӧ�����ʵ��ǣ�������
A.NaOH
B.Na2O
C.Na
D.CaO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��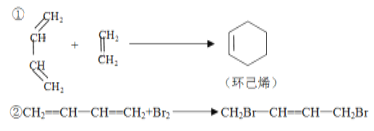
(1)д�����з�Ӧ����Ľṹ��ʽ��
H2C=CHCH=CHCH3+H2C=CHCHO�� _______________��
(2)��ij����AΪ��ʼԭ�Ϻϳɻ�����G ��·������(ͼ�� Mr ��ʾ��Է�������)
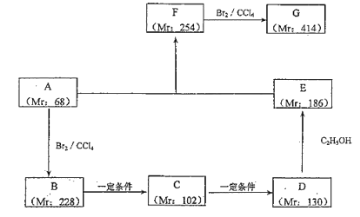
��д����Ӧ���� B��C��_______��F��G��_______��
��д���������ʵĽṹ��ʽ��A��________��F��_______��
��д�����з�Ӧ�Ļ�ѧ����ʽ��
B��C��________________��D��E��_______________��
��д�� G ������������Һ��Ӧ�ķ���ʽ____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���μ�������ˮ�����и������ӿ��ܴ������ڵ���
A. Fe3+��Al3+��Cl-��NO3- B. K+��Na+��I-��SO42-
C. Ag+��Ca2+��NH4+��NO3- D. Na+��Ba2+��CO32-��SO42-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2-�ȱ���Ϊ��Ҫԭ����ȡ1,2-�������������ķ�ӦΪ
A. �ӳ�һ��ȥ-ȡ�� B. ��ȥһ�ӳ�һȡ��
C. ȡ��һ��ȥһ�ӳ� D. ȡ��-�ӳ�-��ȥ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����4L�ܱ������г���6molA�����5molB���壬һ�������·�����Ӧ��3A��g��+B��g��![]() 2C��g��+xD��g�����ﵽƽ��ʱ��������2molC�����ⶨ��D��Ũ��Ϊ0.5mol/L�������ж���ȷ����
2C��g��+xD��g�����ﵽƽ��ʱ��������2molC�����ⶨ��D��Ũ��Ϊ0.5mol/L�������ж���ȷ����
A. B��ת����Ϊ20%
B. ƽ��ʱA��Ũ��Ϊ1.50mol/L
C. x��1
D. �ﵽƽ��ʱ������ͬ�¶��������ڻ�������ѹǿ�Ƿ�Ӧǰ��85%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������һ���������ܹ��棬��������Ӧ�Լ���ᷢ����ѧ�仯�����������ӷ���ʽ��ȷ���ǣ� ��
ѡ�� | ������ | �����Լ� | �����Լ�������Ӧ�����ӷ���ʽ |
A | Fe2����NO | ϡ���� | 3Fe 2����NO |
B | Fe3����I����ClO�� | ����������Һ | Fe3����3OH��= Fe(OH)3�� |
C | Ba2����HCO | ����������Һ | HCO |
D | Al3����Cl����NO | ��������������Һ | Al3����3OH��= Al(OH)3�� |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com