
【题目】M、N、R、X、Y为原子序数依次增大的短周期主族元素,Z、W都是第四周期过渡元素。R是同主族元素中最活泼的非金属元素,且能生成MR2型共价化合物, Z和Z2+具有相同的单电子数,Z2+的价电子数是W+的二分之一, W 有W +和W2+两种常见离子,R和X同主族。请回答下列问题(以下均用化学符号表示):
(1)写出R基态原子的电子排布图_________________,M、N和R第一电离能由小到大的顺序是____________。
(2)N的气态氢化物极易溶于R的氢化物,且该体系呈碱性,请用结构式表示出两者主要的结合方式_________________。
(3)在上述元素形成的分子中,有四种分子互为等电子体,分别是MR2、MX2和MRX以及_______,该分子的结构式为___________,N与Y形成的NY3分子的空间构型是________。
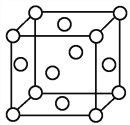
(4)M和R所形成MR2晶体以及W晶体的结构都可以如图表示(O表示一个MR2分子或一个W原子),晶体中正八面体和正四面体空隙数的比值是_________,Z的硫化物有3种晶体,其中一种是Z2+为面心立方堆积,而晶体中全部正四面体空隙的二分之一被S2-占据,如果两种离子核间距为acm,则该晶体密度为__________________。
(5)Z的一种氧化物常用来氧化Y的氢化物的水化物的浓溶液制备Y2,该反应的化学方程式是____________。
【答案】 ![]() C<O<N
C<O<N 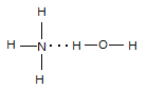 N2O N=N=O 三角锥型 1:2 261
N2O N=N=O 三角锥型 1:2 261![]() /16NAa3 MnO2+4HCl(浓)
/16NAa3 MnO2+4HCl(浓)![]() MnCl2+Cl2+2H2O
MnCl2+Cl2+2H2O
【解析】M、N、R、X、Y为原子序数依次增大的短周期主族元素, R是同主族元素中最活泼的非金属元素,且能生成MR2型共价化合物,则M为+4价,R为-2价,R和X同主族,因此R为O,M为C;X为S,则Y为Cl,N为N元素;Z、W都是第四周期过渡元素,W 有W +和W2+两种常见离子,则W为Cu元素;Z和Z2+具有相同的单电子数,Z2+的价电子数是W+的二分之一,则Z2+的价电子排布式为3d5,Z为Mn元素。
(1)R为O元素,基态O原子的电子排布图为![]() ;同周期的主族元素随核电荷数的增大,第一电离能呈增大的趋势,但氮的2p轨道为半充满结构,相对稳定,则C、N、O的第一电离能由小到大的顺序是C<O<N,故答案为:
;同周期的主族元素随核电荷数的增大,第一电离能呈增大的趋势,但氮的2p轨道为半充满结构,相对稳定,则C、N、O的第一电离能由小到大的顺序是C<O<N,故答案为:![]() ;C<O<N;
;C<O<N;
(2)NH3与H2O均为极性分子,且NH3与H2O分子之间存在氢键,根据相似相溶原理,故NH3易溶于水,氨水中存在NH3H2O,能部分电离出OH-,导致氨水显碱性,NH3H2O的结构式为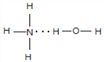 ,故答案为:
,故答案为: 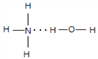 ;
;
(3)在上述元素形成的分子中,有四种分子互为等电子体,分别是CO2、CS2和COS以及N2O,等电子体检验相似的结构,则N2O的结构式为N=N=O,NCl3中N原子含有3个σ键和1个孤电子对,中心原子N是sp3杂化,则NCl3为三角锥型,故答案为:N2O;N=N=O;三角锥型;
(4)由晶胞结构可知,一个晶胞围成正八面体空隙共有4个(如图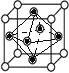 1个和12个
1个和12个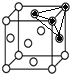 ,是正八面体的
,是正八面体的![]() ,计3个);晶体中共有类似A点的顶点共有8个,晶体中围成正四面体空隙共有8个(如图
,计3个);晶体中共有类似A点的顶点共有8个,晶体中围成正四面体空隙共有8个(如图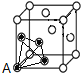 ),个数比为4:8=1:2;MnS有3种晶体,其中一种是Mn2+为面心立方堆积,而晶体中全部正四面体空隙的二分之一被S2-占据,则晶胞结构为
),个数比为4:8=1:2;MnS有3种晶体,其中一种是Mn2+为面心立方堆积,而晶体中全部正四面体空隙的二分之一被S2-占据,则晶胞结构为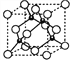 ,在晶胞中Mn2+共有8×
,在晶胞中Mn2+共有8×![]() +6×
+6×![]() =4,S2-共有4个,设晶胞的边长为x,则
=4,S2-共有4个,设晶胞的边长为x,则![]() x=4acm,x=
x=4acm,x=![]() cm,因此晶体密度=
cm,因此晶体密度=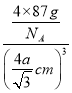 =
=![]() g/cm3,故答案为:1:2;
g/cm3,故答案为:1:2; ![]() ;
;
(5)二氧化锰常用来氧化氯化氢的水化物的浓溶液制备氯气,反应的化学方程式为MnO2+4HCl(浓)![]() MnCl2+Cl2+2H2O,故答案为:MnO2+4HCl(浓)
MnCl2+Cl2+2H2O,故答案为:MnO2+4HCl(浓)![]() MnCl2+Cl2+2H2O。
MnCl2+Cl2+2H2O。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】已知某密闭容器中存在下列平衡:CO(g)+H2O(g) ![]() CO2(g)+H2(g),CO2的平衡物质的量浓度c(CO2)与温度t的关系如图所示。下列说法错误的是 ( )
CO2(g)+H2(g),CO2的平衡物质的量浓度c(CO2)与温度t的关系如图所示。下列说法错误的是 ( )

A. 平衡状态A与C相比,平衡状态A的c(CO)较小
B. 在t2时,D点的反应速率:v(逆)>v(正)
C. 反应CO(g)+H2O(g) ![]() CO2(g)+H2(g)的ΔH>0
CO2(g)+H2(g)的ΔH>0
D. 若t1、t2时的平衡常数分别为K1、K2,则K1<K2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图分别为生物体内分子的部分结构模式图,请据图回答问题:

(1)甲图中的三种物质分别属于动物、植物细胞中的储能物质的是_____,组成这三种物质的单体都是_____。
(2)乙图所示化合物的基本组成单位是___________,即图中字母_______________ 所示的结构表示,各基本单位之间是通过_____________(填“①”“②”或“③”)连接起来 的。
(3)丙图是由________个氨基酸经__________ 过程形成的,氨基酸的结构通式为__________ 。检验丙和戊可以用______________ 试剂。
(4)丁和戊中的 Mg2+、Fe2+体现了无机盐具有什么功能?_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 1 mol CO2 的质量为44g/mol
B. CO2的摩尔质量为44g
C. 64gO2中含有4mol氧原子
D. NA个CO2分子的质量等于CO2的相对分子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“化学是你,化学是我”.化学与生产、生活密切相关,下列说法错误的是( )
A. 中国古代利用明矾溶液的酸性清除铜镜表面的铜锈
B. 水泥冶金厂常用高压电除去工厂烟尘,利用了胶体的性质
C. 开发利用太阳能、风能、生物能、海洋能等清洁能源,符合“低碳经济”
D. 二氧化硫有漂白性,常用于棉、麻、纸张和食品的漂白
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用质量分数为98%、密度为1.84g/cm3的浓硫酸,配制0.2mol/L的硫酸溶液480mL.请回答下列问题:
(1)所需浓硫酸的体积为________mL(计算结果保留到小数点后1位)
(2)从下列用品中选出实验所需要的仪器__________(填序号).
A.1000mL烧杯B.100mL烧杯C.10mL量筒 D.100mL量筒E.500mL容量瓶.F.1000mL容量瓶 G.广口瓶H.托盘天平I.玻璃棒
除选用上述仪器外,尚缺少必要的仪器或用品是_____________.
(3)容量瓶在使用前必须进行的一步操作是______________________。
(4)该学生根据计算结果,进行如下实验操作:①用量筒量取计算所需体积的浓硫酸;
②向量筒中加入少量蒸馏水,并用玻璃棒搅拌;③立即将稀释后的溶液转入容量瓶中;④将蒸馏水直接注入容量瓶至刻度线;⑤把容量瓶盖盖紧,再振荡摇匀.
指出上述实验中错误的操作是______________(用编号表示).
(5)若实验中出现下列现象,造成所配溶液浓度偏高的有________。
a、浓硫酸稀释后未冷至室温即转移至容量瓶进行定容。
b、定容摇匀时,液面下降,再加水。
c、定容后,经振荡、摇匀、静置,液面下降。
d、定容时俯视刻度线。
e、定容时水加多了,用滴管吸出。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列属于物理变化的是
A. 麦芽糖和稀硫酸共热
B. 蛋白质溶液中加入饱和NaCl溶液,有沉淀析出
C. 蛋白质溶液中加入浓NaOH溶液
D. 氨基酸中加入盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活、社会密切相关,下列有关说法正确的是
A. 古有“青蒿一握,以水二升渍,绞取汁”,今用乙醚从黄花蒿中可提取青蒿素是利用氧化还原反应原理
B. 食用“地沟油”对人体危害很大,但可以通过蒸馏的方式获得汽油、柴油等,实现资源的再利用。
C. 牛奶中加入果汁会产生沉淀,是因为发生了酸碱中和反应
D. CO2是大量使用的灭火剂,但着火的镁条在CO2中继续燃烧说明它也可以助燃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源可划分为一次能源和二次能源,直接来自于自然界的能源称为一次能源;需依靠其他能源的能量间接制取的能源称为二次能源。下列叙述正确的是( )
A.水煤气是二次能源B.水力是二次能源
C.天然气是二次能源D.电能是一次能源
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com