
ԭ���������������X��Y��Z��M��N����Ԫ�أ�XZ2����������ЧӦ����Ҫ���壬M
�����������ǵ��Ӳ�����2������N2+����3d��9�����ӣ���ش��������⣺
��1��Nλ��Ԫ�����ڱ��� ����X��Y��Z�ĵ縺������Ϊ ��
 ��2��XZ
��2��XZ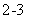 ������ԭ���ӻ���ʽΪ ��
������ԭ���ӻ���ʽΪ ��
��3�� Z���⻯��(H2Z)���Ҵ��е��ܽ�ȴ���H2M����ԭ���� ��
��4��Na2M2Z3��ԭ�Խ�ǿ������Һ���ױ�Cl2������MZ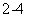 �����������ȼ����÷�Ӧ�����ӷ���ʽΪ ��
�����������ȼ����÷�Ӧ�����ӷ���ʽΪ ��
��5��N��Y���γɵ�һ�־������õĵ�ѧ��ѧ���ܵĻ����
�侧���ṹ��ͼ��ʾ����û�����Ļ�ѧʽΪ ��
 ����������ϵ�д�
����������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
NA��ʾ�����ӵ�����������������ȷ����
A��lmol FeI2������������Ӧʱת�Ƶĵ�����Ϊ2NA
B��2 L0.5 mol��L-1�������Һ�����������������ΪNA
C��1 mol Na2O2�����к���������Ϊ4NA
D����ϩ�ͻ�������ɵ�42 g�����������ԭ�ӵĸ���Ϊ6 NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������γɶ��ֻ������NH3��N2H4��HCN��NH4NO3�ȡ�
��1����֪��N2(g)+2H2(g)=N2H4(l) ��H= + 50.6kJ��mol-1
2H2(g)+O2(g)=2H2O(l) ��H=-571.6 kJ��mol-1
���N2H4(l)+O2(g)=N2(g)+2H2O(l) ��H= kJ��mol-1
��N2(g)+2H2(g)=N2H4(l) �����Է����е�ԭ���� ��
���ô������������������Եõ�N2H4��ϡ��Һ���÷�Ӧ�Ļ�ѧ����ʽ�� ��
��2���ɿ��Һ�е�CN- ����H2O2��������֪��H2SO4=H++ HSO4- HSO4-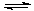 H++ SO42-�ò��缫������������Һ��������������S2O82-��S2O82-ˮ����Եõ�H2O2��д�������ϵĵ缫��Ӧʽ ��
H++ SO42-�ò��缫������������Һ��������������S2O82-��S2O82-ˮ����Եõ�H2O2��д�������ϵĵ缫��Ӧʽ ��
��3������þ������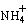 �ķ�ˮ�ᷢ�����·�Ӧ��
�ķ�ˮ�ᷢ�����·�Ӧ��
MgO+H2O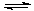 Mg(OH)2 Mg(OH)2+2NH4+
Mg(OH)2 Mg(OH)2+2NH4+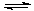 Mg2+ +2NH3��H2O��
Mg2+ +2NH3��H2O��
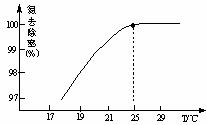 ���¶ȶԵ������ʵ�Ӱ����ͼ��ʾ����25��ǰ�������¶ȵ�ȥ���������ԭ���� ��
���¶ȶԵ������ʵ�Ӱ����ͼ��ʾ����25��ǰ�������¶ȵ�ȥ���������ԭ���� ��
��ʣ�������þ������Է�ˮ�γɶ�����Ⱦ�������� ��
��4���ζ������ˮ�еİ������������������백�������ʽ������ˮ�У��������£���ȡ10 mL��ˮˮ����������ƿ�У��ټ�����ˮ�������Ϊ175 mL���Ƚ�ˮ���������ԣ��ټ�������þʹˮ�������ԣ����Ȣ���25 mL��������������İ�[2NH3+4H3BO3��(NH4)2B4O7+5H2O]�ܽ�����Һ������ƿ�У�����2��ָʾ������c mol��L-1������ζ����յ�[(NH4)2B4O7+H2SO4+5H2O��(NH4)2SO4+4H3BO3]����¼���ĵ����V mL����ˮ���е��ĺ����� mg��L-1���ú�c��V�ı���ʽ��ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪A��g��+B��g�� C��s��+2D��g����Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���£�
C��s��+2D��g����Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���£�
| �¶�/�� | 700 | 800 | 830 | 1000 | 1200 |
| ƽ�ⳣ�� | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
�ش��������⣺
��1���÷�Ӧ��ƽ�ⳣ������ʽK= ����H=�� 0���������������=������
��2��830��ʱ����һ��5L���ܱ������г���0.20mol��A��0.80mol��B���練Ӧ��ʼ6s��A��ƽ����Ӧ����v(A)=0.003mol•L��1•s��1����6sʱc(A)=�� �� mol•L��1����Ӧ�ﵽƽ��ʱA��ת����Ϊ80%�������ʱ����ܱ��������ٳ���1mol���������ƽ��ʱA��ת����Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ȷ��ʾ���з�Ӧ�����ӷ���ʽ��
A��Na2O2����ˮ�Ʊ�O2��2O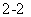 ��2H2O=4OH����O2��
��2H2O=4OH����O2��
B����ϡ����ϴ���Թ��ڱڵ�������Ag+2H��+NO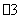 =Ag��+NO��+H2O
=Ag��+NO��+H2O
C����Ba(OH)2��Һ�еμ�NaHSO4��Һ�����ԣ�Ba2����2OH����2H����SO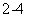 ��BaSO4����2H2O
��BaSO4����2H2O
D�� ������Һ��ͨ������CO2��2C6H5O- + CO2 + H2O  2C6H5OH + CO
2C6H5OH + CO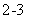
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ͬ�������ͬ���ʵ���Ũ�ȵ�KCl��CaCl2��FeCl3��Һ�ֱ���VmL 1 mol /L��AgNO3��Һ��֮��Ӧ������ʹCl������ǡ����ȫ������������������Һ��������ǣ� ����
A��1��2��3 B��3��2��1 C��6��3��2 D��2��3��6
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ti���ѣ���һ�־��������������ܵĽ�Ϊ����Ľ������Ѻ��ѺϽ���Ϊ��21���͵���Ҫ�������ϡ�ij��ѧ��ȤС����ʵ������̽��Ti��Mg��Cu�Ļ��˳����������ͬ�¶��£�ȡ��С��ͬ�����ֽ�����Ƭ���ֱ�Ͷ����������Ũ�ȵ�����ϡ�����У��۲��������£�
| ���� | Ti | Mg | Cu |
| ������������ | �ų����� ���ʻ��� | �ų����� ���ʿ� | �ޱ仯 |
�����й����ֽ�����˵����ȷ���ǣ� ����
A�����ֽ����Ļ����ǿ������˳����Ti��Mg��Cu
B�����ѷ��л���Mg���ᴿTiʱ����ϡ�����ȥMg
C����Ti��CuSO4��Һ���û���Cu�ǹ�ҵ��ȡCu�ĺܺ�;��
D��Cu��MgCl2��Һ��������ѧ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ȷ��ʾ���з�Ӧ�����ӷ���ʽ�ǣ�������
A��Ũ��������м��Ӧ��2Fe+6H+=2Fe3++3H2��
B������CuSO4��Һ��Ӧ��2Na+Cu2+=Cu��+2Na+
C��NaHCO3��Һ��ϡH2SO4��Ӧ��CO2-3+2H+=H2O+CO2��
D����FeCl3��Һ�м���Mg(OH)23Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
δ������Դ���ص�����Դ�ḻ����ʹ��ʱ�Ի�������Ⱦ����Ⱦ��С���ҿ�����������������δ������Դ������
����Ȼ�� ��ú �ۺ��� ��ʯ�� ��̫���� ���������� �߷��� ������
A���٢ڢۢ� B���ݢޢߢ� C���ۢݢޢߢ� D���ۢܢݢޢߢ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com