
能正确表示下列反应的离子方程式是
A.Na2O2加入水制备O2:2O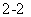 +2H2O=4OH-+O2↑
+2H2O=4OH-+O2↑
B.用稀硝酸洗涤试管内壁的银镜:Ag+2H++NO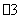 =Ag++NO↑+H2O
=Ag++NO↑+H2O
C.向Ba(OH)2溶液中滴加NaHSO4溶液至中性:Ba2++2OH-+2H++SO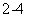 =BaSO4↓+2H2O
=BaSO4↓+2H2O
D. 向苯酚钠溶液中通入少量CO2:2C6H5O- + CO2 + H2O  2C6H5OH + CO
2C6H5OH + CO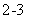
科目:高中化学 来源: 题型:
已知:2H2(g) +O2(g) = 2H2O(g) ΔH =-483.6 kJ/mol


下列说法不正确的是
A.该反应原理可用于设计氢氧燃料电池
B.破坏1 mol H—O 键需要的能量是463.4 kJ
C.H2O(g)=H2(g) + 1/2O2(g) ΔH = +241.8 kJ/mol
D.H2(g) 中的H—H 键比 H2O(g) 中的H—O 键牢固
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验过程中曲线变化正确的是( )
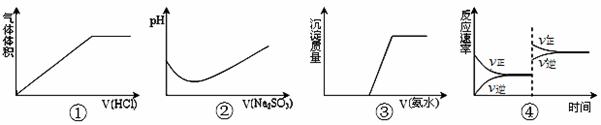
A.①表示Na2CO3溶液中滴入稀盐酸
B.②表示溴水中滴入Na2SO3溶液
C.③表示AgNO3溶液中滴入氨水
D.④表示一定条件下2SO2+O2 2SO3 △H<0达平衡后,升高温度
2SO3 △H<0达平衡后,升高温度
查看答案和解析>>
科目:高中化学 来源: 题型:
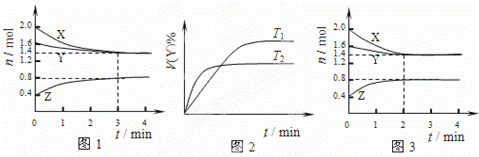
T℃时在2L容积不变的密闭容器中使X(g)与Y(g)发生反应生成Z(g).反应过程中X、Y、Z的浓度变化如图1所示;若保持其他条件不变,温度分别为T1和T2时,Y的体积百分含量与时间的关系如图2所示.则下列结论错误的是( )
|
| A. | 容器中发生的反应可表示为:3X(g)+Y(g) |
|
| B. | 反应进行前3min内,用X表示的反应速率v(X)=0.1mol/(L•min) |
|
| C. | 若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强 |
|
| D. | 保持其他条件不变,升高温度,化学平衡向逆反应方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
标况下将1g纯净的C2H2在空气中完全燃烧,生成CO2气体和液态水,放出akJ热量,则表示C2H2燃烧热的热化学方程式为:_______________________
⑵.(4分)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当它们混合反应时,立即产生大量氮气和水蒸气,并放出大量的热。已知0.4mol液态肼与足量的液态双氧水反应,生成氮气和水蒸气,放出256KJ的热量。反应的热化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
原子序数依次增大的X、Y、Z、M、N五种元素,XZ2是引起温室效应的主要气体,M
最外层电子数是电子层数的2倍,,N2+核外3d有9个电子,请回答下列问题:
(1)N位于元素周期表的 区,X、Y、Z的电负性最大的为 。
 (2)XZ
(2)XZ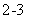 中中心原子杂化方式为 。
中中心原子杂化方式为 。
(3) Z的氢化物(H2Z)在乙醇中的溶解度大于H2M,其原因是 。
(4)Na2M2Z3还原性较强,在溶液中易被Cl2氧化成MZ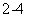 ,常用作脱氯剂,该反应的离子方程式为 。
,常用作脱氯剂,该反应的离子方程式为 。
(5)N与Y可形成的一种具有良好的电学和光学性能的化合物,
其晶胞结构如图所示,则该化合物的化学式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,在溶液中可发生以下反应:① H++Z-+XO=== X2++Z2+H2O(未配平),
② 2M2++R2===2M3++2R-,③ 2R-+Z2=== R2+2Z-。由此判断下列说法正确的是
A.常温下反应2M2++Z2===2M3 ++2Z-不可以自发进行
B.R元素在反应②中被氧化,在③中被还原
C.反应①配平后,H2O的化学计量数为8
D.还原性强弱顺序为:X2+>Z->R->M2+
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E为易溶化合物,其离子组成为
| 阳离子 | Fe3+、Ba2+、Al3+、Na+、Ag+ |
| 阴离子 | NO3—、OH—、SO42—、Cl—、CO32— |
在各化合物中离子不重复,分别取其溶液进行实验,结果如下:
①在A溶液中逐滴加入氨水,有白色沉淀生成,继续加氨水至过量,沉淀消失;
②用pH试纸测得B和C溶液显碱性,0.1mol/L的C溶液pH小于13;
③在D溶液中加入铁粉,溶液质量增加;④在E溶液中加入过量B,没有沉淀产生。
完成下列填空:
(1)A的化学式为 ;
(2)③反应的离子方程式为 ;
(3)检验D溶液中阴离子的的方法是 ;
(4)E的的化学式为 ,将E蒸干、灼热至质量不再改变,最后所得物质是(填化学式) 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com