
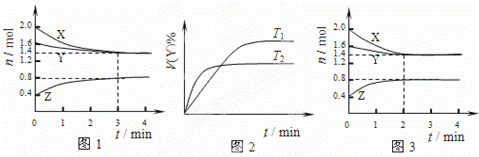
T℃时在2L容积不变的密闭容器中使X(g)与Y(g)发生反应生成Z(g).反应过程中X、Y、Z的浓度变化如图1所示;若保持其他条件不变,温度分别为T1和T2时,Y的体积百分含量与时间的关系如图2所示.则下列结论错误的是( )
|
| A. | 容器中发生的反应可表示为:3X(g)+Y(g) |
|
| B. | 反应进行前3min内,用X表示的反应速率v(X)=0.1mol/(L•min) |
|
| C. | 若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强 |
|
| D. | 保持其他条件不变,升高温度,化学平衡向逆反应方向移动 |
科目:高中化学 来源: 题型:
某温度下,密闭容器中X、Y、Z、W四种气体的初始浓度和平衡浓度如下表,下列说法错误的是( )
| 物质 | X | Y | Z | W |
| 初始浓度/mol·L-1 | 0.5 | 0.6 | 0 | 0 |
| 平衡浓度/mol·L-1 | 0.1 | 0.1 | 0.4 | 0.6 |
A.反应达到平衡时,X的转化率为80%
B.该反应的平衡常数表达式为K=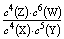
C.增大压强其平衡常数不变,但使平衡向生成Z的方向移动
D.改变温度可以改变此反应的平衡常数
查看答案和解析>>
科目:高中化学 来源: 题型:
氮可以形成多种化合物,如NH3、N2H4、HCN、NH4NO3等。
(1)已知:N2(g)+2H2(g)=N2H4(l) △H= + 50.6kJ·mol-1
2H2(g)+O2(g)=2H2O(l) △H=-571.6 kJ·mol-1
则①N2H4(l)+O2(g)=N2(g)+2H2O(l) △H= kJ·mol-1
②N2(g)+2H2(g)=N2H4(l) 不能自发进行的原因是 。
③用次氯酸钠氧化氨,可以得到N2H4的稀溶液,该反应的化学方程式是 。
(2)采矿废液中的CN- 可用H2O2处理。已知:H2SO4=H++ HSO4- HSO4-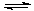 H++ SO42-用铂电极电解硫酸氢钾溶液,在阳极上生成S2O82-,S2O82-水解可以得到H2O2。写出阳极上的电极反应式 。
H++ SO42-用铂电极电解硫酸氢钾溶液,在阳极上生成S2O82-,S2O82-水解可以得到H2O2。写出阳极上的电极反应式 。
(3)氧化镁处理含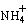 的废水会发生如下反应:
的废水会发生如下反应:
MgO+H2O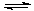 Mg(OH)2 Mg(OH)2+2NH4+
Mg(OH)2 Mg(OH)2+2NH4+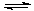 Mg2+ +2NH3·H2O。
Mg2+ +2NH3·H2O。
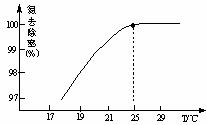 ①温度对氮处理率的影响如图所示。在25℃前,升高温度氮去除率增大的原因是 。
①温度对氮处理率的影响如图所示。在25℃前,升高温度氮去除率增大的原因是 。
②剩余的氧化镁,不会对废水形成二次污染,理由是 。
(4)滴定法测废水中的氨氮含量(氨氮以游离氨或铵盐形式存在于水中)步骤如下:①取10 mL废水水样于蒸馏烧瓶中,再加蒸馏水至总体积为175 mL②先将水样调至中性,再加入氧化镁使水样呈微碱性,加热③用25 mL硼酸吸收蒸馏出的氨[2NH3+4H3BO3=(NH4)2B4O7+5H2O]④将吸收液移至锥形瓶中,加入2滴指示剂,用c mol·L-1的硫酸滴定至终点[(NH4)2B4O7+H2SO4+5H2O=(NH4)2SO4+4H3BO3],记录消耗的体积V mL。则水样中氮的含量是 mg·L-1(用含c、V的表达式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
在V升的密闭容器中进行如下反应:,mA十nB  pC十qD,用A物质表示的平均反应速率为
pC十qD,用A物质表示的平均反应速率为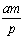 摩/(升·分),则t分钟时,D物质增加的物质的量是:
摩/(升·分),则t分钟时,D物质增加的物质的量是:
A.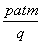 摩 B.
摩 B.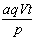 摩 C.
摩 C.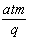 摩 D.
摩 D.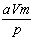 摩
摩
查看答案和解析>>
科目:高中化学 来源: 题型:
己知A(g)+B(g) C(s)+2D(g)反应的平衡常数和温度的关系如下:
C(s)+2D(g)反应的平衡常数和温度的关系如下:
| 温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
回答下列问题:
(1)该反应的平衡常数表达式K= ,△H= 0(填“<”“>”“=”);
(2)830℃时,向一个5L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反应速率v(A)=0.003mol•L﹣1•s﹣1,则6s时c(A)= mol•L﹣1。反应达到平衡时A的转化率为80%,如果这时向该密闭容器中再充入1mol氩气,达新平衡时A的转化率为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
能正确表示下列反应的离子方程式是
A.Na2O2加入水制备O2:2O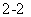 +2H2O=4OH-+O2↑
+2H2O=4OH-+O2↑
B.用稀硝酸洗涤试管内壁的银镜:Ag+2H++NO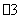 =Ag++NO↑+H2O
=Ag++NO↑+H2O
C.向Ba(OH)2溶液中滴加NaHSO4溶液至中性:Ba2++2OH-+2H++SO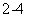 =BaSO4↓+2H2O
=BaSO4↓+2H2O
D. 向苯酚钠溶液中通入少量CO2:2C6H5O- + CO2 + H2O  2C6H5OH + CO
2C6H5OH + CO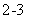
查看答案和解析>>
科目:高中化学 来源: 题型:
金属Ti(钛)是一种具有许多优良性能的较为昂贵的金属,钛和钛合金被认为是21世纪的重要金属材料。某化学兴趣小组在实验室中探究Ti、Mg、Cu的活动性顺序。他们在相同温度下,取大小相同的三种金属薄片,分别投入等体积、等浓度的足量稀盐酸中,观察现象如下:
| 金属 | Ti | Mg | Cu |
| 金属表面现象 | 放出气泡 速率缓慢 | 放出气泡 速率快 | 无变化 |
下列有关三种金属的说法正确的是( )。
A.三种金属的活动性由强到弱的顺序是Ti、Mg、Cu
B.若钛粉中混有Mg,提纯Ti时可用稀盐酸除去Mg
C.用Ti从CuSO4溶液中置换出Cu是工业制取Cu的很好途径
D.Cu和MgCl2溶液不发生化学反应
查看答案和解析>>
科目:高中化学 来源: 题型:
将CO2气体缓缓地通入到含KOH、Ba(OH)2和KAlO2的混合溶液中直至过量,生成沉淀的物质的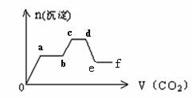 量与所通CO2的体积关系如图所示。下列关于整个反应进程中的各种描述不正确的是
量与所通CO2的体积关系如图所示。下列关于整个反应进程中的各种描述不正确的是
A.o—a段反应的化学方程式是:Ba(OH)2 + CO2 = Ba CO3↓+ H2O
B.b—c段反应的离子方程式是:
2AlO2-+ 3H2O+ CO2=2Al(OH)3↓+ CO32-
C.a—b段与c—d段所发生的反应相同
D.d—e段沉淀的减少是由于碳酸钡固体的消失所致
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com