
����Ŀ�������£���0.1molL��1NaOH��Һ�ֱ�ζ������Ϊ20mlŨ�Ⱦ�Ϊ0.1molL��1HCl��Һ��HX��Һ����Һ��pH�����NaOH��Һ����仯ͼ������˵������ȷ���ǣ� �� 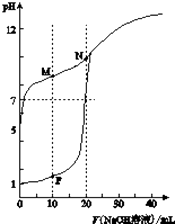
A.HX����
B.M��c��HX����c��X������c��OH������c��H+��
C.��P���N�����ҺΪ��ϣ�������
D.��N����Һ��ͨ��HCl��pH=7��c��Na+����c��HX��=c��Cl������c��X����
���𰸡�C
���������⣺A��δ�ζ�ʱ��0.1molL��1HCl��ҺpHΪ1����ͼ��֪0.1mol/L HX��Һ��pH��5����HX���ᣬ��A��ȷ��
B��M��Ϊ��Ũ��NaX��HX�����Һ������Һ�ʼ��ԣ�˵��X����ˮ��̶ȴ���HX�ĵ���̶ȣ��������غ��֪��2c��Na+��=c��X����+c��HX������ϵ���غ�c��Na+��+c��H+��=c��X����+c��OH�����������ɵã�c��X����+c��HX��+2c��H+��=2c��X����+2c��OH�����������ã�c��HX����c��X����=2c��OH������2c��H+����c��OH������c��H+������B��ȷ��
C��P����Һ��NaCl��HCl���ʵ�����ȣ�N��ΪNaX��Һ��NaX���ʵ���ΪHCl��2������Ϻ�ΪNaCl��NaX��HX�����Һ������Һ��NaX��HX��Ũ����ȣ�����X����ˮ��̶ȴ���HX�ĵ���̶ȣ��ʼ��ԣ���C����
D�����ݵ���غ㣺c��Na+��+c��H+��=c��Cl����+c��X����+c��OH��������ҺpH=7����c��Na+��=c��Cl����+c��X�������������غ��֪c��Na+��=c��X����+c��HX���������ɵ�c��HX��=c��Cl����������ҺΪNaCl��NaX��HX�Ļ����Һ����ͬŨ����X����ˮ��̶ȴ���HX�ĵ���̶ȣ�������ҺΪ���ԣ�����Һ��c��NaX����c��HX��������Һ��c��Na+����c��HX��=c��Cl������c��X��������D��ȷ��
��ѡ��C��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������Ȼ�ѧ����ʽ���ж��⻯����ȶ���˳����ȷ���ǣ� �� ![]() N2��g��+
N2��g��+ ![]() H2��g��=NH3��g����H=��46.19kJmol��1
H2��g��=NH3��g����H=��46.19kJmol��1![]() H2��g��+
H2��g��+ ![]() Cl2��g��=HCl��g����H=��92.36kJmol��1
Cl2��g��=HCl��g����H=��92.36kJmol��1![]() I2��g��+
I2��g��+ ![]() H2��g��=HI��g����H=��4.74kJmol��1 ��
H2��g��=HI��g����H=��4.74kJmol��1 ��
A.HCl��NH3��HI
B.HI��HCl��NH3
C.HCl��HI��NH3
D.NH3��HI��HCl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�����,����˵����ȷ����( )
A.44gCO2�����к��е���������ΪNA
B.��״����,11. 2LH2O����������Ϊ0.5NA
C.24gMg��������������ȫȼ��ʧȥ�ĵ�����Ϊ2NA
D.���³�ѹ��,22. 4LN2����������ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼�����La2(CO3)3�ݿ�����������ĩ���������ߵĸ�������Ѫ֢���Ʊ���Ӧԭ��Ϊ��LaC13+6NH4HCO3= La2(CO3)3����6NH4Cl+ 3CO2��+3H2O��ij��ѧ��ȤС����������װ��ʵ������ģ���Ʊ�̼���硣

��l��ʢ��ϡ���������Ϊ____________��
��2���Ʊ�̼����ʵ�������е��ܴ������ҵ�����˳��Ϊ��F��___��___ ��___ ��___ ��___ ��
��3��Y�з�����Ӧ�Ļ�ѧ��ӦʽΪ________________��
��4��X��ʢ�ŵ��Լ���_____��������Ϊ________________��
��5��Z��Ӧ��ͨ��NH3����ͨ�������CO2��ԭ��Ϊ_________��
��6��La2(CO3)3���������IJⶨ��ȷ��ȡ10.0g��Ʒ����������10.0mLϡ�����У�����10 mLNH3 ��NH4Cl������Һ������0.2g������炙��ָʾ������0.5mol/LEDTA��Na2H2Y������Һ�ζ���������ɫ��La3��+H2Y-=LaY-+2H+��������EDTA ��Һ44.0 mL�����Ʒ��La2(CO3)3������������[La2(CO3)3]=_________��
��7���û�ѧ��ȤС��Ϊ̽��La2(CO3)3��La(HCO3)3���ȶ���ǿ������������µ�ʵ��װ�ã�����Թ���ʢ�ŵ�����Ϊ_______��ʵ������У��������Թ��й�������������ʱ��Ĺ�ϵ������ͼ��ʾ��������ʵ������й۲쵽������Ϊ______________��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪2SO2(g)+O2(g)![]() 2SO3(g) ��H=-197kJ��mol-1����ͬ�¡�ͬ����������ܱ������зֱ�������壺(��)2molSO2��lmolO2��(��) lmolSO2��0.5molO2��(��)2 mol SO3�����¡������·�Ӧ��ƽ��ʱ�����й�ϵһ����ȷ����
2SO3(g) ��H=-197kJ��mol-1����ͬ�¡�ͬ����������ܱ������зֱ�������壺(��)2molSO2��lmolO2��(��) lmolSO2��0.5molO2��(��)2 mol SO3�����¡������·�Ӧ��ƽ��ʱ�����й�ϵһ����ȷ����
A. ������ѹǿP��P��=P��>2P��
B. SO3������m��m��=m��>2m��
C. c(SO2)��c(O2)֮�� k��k��=k��>k��
D. ��Ӧ�ų���������������ֵQ��Q��=Q��>2Q��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���輰�仯�����ڲ���������Ӧ�ù㷺��������������ȷ����
A. �赥�ʿ���������̫���ܵ��
B. �赥�������첣������Ҫԭ��
C. ʯӢ��SiO2����������������Ʒ
D. �����������������IJ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ȼ�������ϩ�ۺϴ�������Ҫ�ɷ֣��Ʊ���Ӧ���£�
��TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g) ��H1=+175.4KJ/mol
��C(s)+1/2O2(g)=CO(g) ��H2=-110.45 KJ/mol������˵����ȷ����

A. C��ȼ����Ϊ110.45KJ/mol
B. ��Ӧ����ʹ�ô�������Hl���С
C. ��Ӧ���е������仯��ͼ��ʾ
D. ��ӦTiO2(s)+2Cl2(g)+2C(s)=TiCl4(g)+2CO(g) ��H=-45.5KJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪Һ����������ˮ���ƣ�25��ʱ��NH3+NH3NH ![]() +NH
+NH ![]() ��NH
��NH ![]() ��ƽ��Ũ��Ϊ1��10��15molL��1 �� ������˵������ȷ���ǣ� ��
��ƽ��Ũ��Ϊ1��10��15molL��1 �� ������˵������ȷ���ǣ� ��
A.��Һ���м���NaNH2��ʹҺ�������ӻ����
B.��Һ���м���NH4Cl��ʹҺ�������ӻ���С
C.�ڴ��¶���Һ�������ӻ�Ϊ1��10��17
D.��Һ���з�������ƣ�������NaNH2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������þ����������Һ�������Ϻ�������Ũ��Ϊ0.2mol/L����������ӵ�Ũ��Ϊ0.5 mol/L��������Һ��þ����Ũ��Ϊ( )��
A. 0.15 mol/L B. 0.3 mol/L C. 0.45 mol/L D. 0.2 mol/L
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com