
【题目】锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述正确的是( )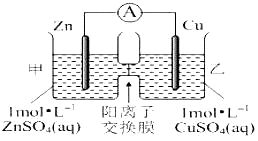
A.铜电极上发生氧化反应
B.电池工作一段时间后,甲池的C(SO42-)减小
C.电池工作一段时间后,乙池溶液的总质量增加
D.阳离子通过交换膜向正极移动,阴离子通过交换膜向负极移动,保持溶液中电荷平衡
【答案】C
【解析】A、由图像可知该原电池反应原理为Zn+Cu2+= Zn2++Cu,故Zn电极为负极失电子发生氧化反应,Cu电极为正极得电子发生还原反应,A不符合题意;
B、该装置中为阳离子交换膜只允许阳离子和水分子通过,故两池中c(SO42-)不变,B不符合题意;
C、电解过程中溶液中Zn2+由甲池通过阳离子交换膜进入乙池,乙池中Cu2++2e-= Cu,故乙池中为Cu2+~Zn2+,摩尔质量M(Zn2+)>M(Cu2+),故乙池溶液的总质量增加,C符合题意;
D、该装置中为阳离子交换膜只允许阳离子和水分子通过,电解过程中溶液中Zn2+由甲池通过阳离子交换膜进入乙池保持溶液中电荷平衡,阴离子并不通过交换膜,D不符合题意。
故答案为:C
铜锌原电池中,锌为负极、铜为正极,分别发生氧化反应和还原反应,结合阳离子交换膜的作用等进行分析即可.


科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 羟基和苯环相互影响使苯酚与苯和醇的化学性质明显不同
B. 苯酚俗称石炭酸,具有微弱的酸性,能与碳酸钠溶液反应
C. 洒落皮肤上的苯酚通常用酒精洗涤
D. 苯酚是红色晶体,70℃以上微溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知甲烷的燃烧热是890 kJ/mol,且1 mol H2O由气态变为液态时放出44 kJ的能量。请写出甲烷燃烧生成水蒸气的热化学反应方程式为:____________________________;
(2)由A、B、C、D四种金属按下表中装置进行实验。
装置 |
|
|
|
现象 | 金属A不断溶解 | C的质量增加 | A上有气体产生 |
根据实验现象回答下列问题:
①装置甲中作正极的是__________________ (填“A”或“B”) ;
②装置乙溶液中C电极反应:__________________________________;
③装置丙中金属A上电极反应属于______________(填“氧化反应”或“还原反应”);
④四种金属活动性由强到弱的顺序是___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在0.1mol/LCH3COOH溶液中存在如下电离平衡:CH3COOH ![]() CH3COO-+H+对于该平衡,下列叙述正确的是( )
CH3COO-+H+对于该平衡,下列叙述正确的是( )
A.加入水时,平衡向逆反应方向移动
B.加入少量NaOH固体,平衡向正反应方向移动
C.加入少量0.1mol·L-1 HCl溶液,溶液中c(H+)减小
D.加入少量CH3COONa固体,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃煤烟气的脱硫脱硝是目前研究的热点。
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)= 4NO(g)+CO2(g)+2H2O(g) △H= -574 kJmol-1
②CH4(g)+4NO(g)= 2N2(g)+CO2(g)+2H2O(g) △H= -1160 kJmol-1
③H2O(g) = H2O(l) △H= -44 kJmol-1
写出CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O( l ) 的热化学方程式_____________。
(2)某科研小组研究臭氧氧化--碱吸收法同时脱除SO2和NO工艺,氧化过程反应原理及反应热、活化能数据如下:
反应Ⅰ:NO(g)+ O3(g) ![]() NO2(g)+O2(g) △H1 = -200.9 kJmol-1 Ea1 = 3.2 kJmol-1
NO2(g)+O2(g) △H1 = -200.9 kJmol-1 Ea1 = 3.2 kJmol-1
反应Ⅱ:SO2(g)+ O3(g)![]() SO3(g)+O2(g) △H2 = -241.6 kJmol-1 Ea2 = 58 kJmol-1
SO3(g)+O2(g) △H2 = -241.6 kJmol-1 Ea2 = 58 kJmol-1
已知该体系中臭氧发生分解反应:2O3(g) ![]() 3O2(g)。请回答:
3O2(g)。请回答:
其它条件不变,每次向容积为2L的反应器中充入含1.0 mol NO、1.0 mol SO2的模拟烟气和2.0 mol O3,改变温度,反应相同时间t后体系中NO和SO2的转化率如图所示:

①由图可知相同温度下NO的转化率远高于SO2,结合题中数据分析其可能原因_______。
②下列说法正确的是________。
A.P点一定为平衡状态点
B.温度高于200℃后,NO和SO2的转化率随温度升高显著下降、最后几乎为零
C.其它条件不变,若缩小反应器的容积可提高NO和SO2的转化率
③假设100℃时P、Q均为平衡点,此时反应时间为10分钟,发生分解反应的臭氧占充入臭氧总量的10%,则体系中剩余O3的物质的量是________mol;NO的平均反应速率为________;反应Ⅱ在此时的平衡常数为_______________。
(3)用电化学法模拟工业处理SO2。将硫酸工业尾气中的SO2通入如图装置(电极均为惰性材料)进行实验,可用于制备硫酸,同时获得电能:

①M极发生的电极反应式为___________________。
②当外电路通过0.2 mol电子时,质子交换膜左侧的溶液质量_____(填“增大”或“减小”)____克。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化过程中,需要加入还原剂才能实现的是( )
A.MnO2→MnO4-B.AlO2-→Al(OH)3
C.AsO33-→AsO43-D.MnO2→MnCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图装置中发生反应的离子方程式为:Zn+2H+=Zn2++H2↑。下列说法错误的是( )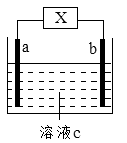
A.a、b不可能是同种材料的电极
B.X为电流计,c为稀盐酸,该装置为原电池
C.X为直流电源,c为稀硫酸,该装置为电解池
D.X为电流计,c为稀硫酸,a可能为铜电极,b可能为锌电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外兴趣小组通过实验发现钾和钠的性质相似,下列说法中能最好地解释这个事实的是( )
A.都是金属元素
B.原子半径相差不大
C.最外层电子数相同
D.最高化合价相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在关于下图所示的原电池中,正确的是
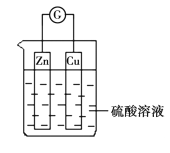
A. Zn被还原
B. 锌片上的电子经导线流向铜片
C. 该原电池运行一段时间后铜片的质量将增加
D. 该原电池将电能转变为化学能
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com